
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑3] 高中化学之离子共存问题 作者:林飞 来源:未知 日期:2012-03-02 10:13:59 点击:12346 所属专题:离子共存
[注解与辨疑3] 高中化学之离子共存问题 作者:林飞 来源:未知 日期:2012-03-02 10:13:59 点击:12346 所属专题:离子共存
离子在溶液中能否大量共存,涉及到离子的性质及溶液酸碱性等综合知识。凡能使溶液中因反应发生使有关离子浓度显著改变的均不能大量共存。如生成难溶、难电离、气体物质或能转变成其它种类的离子(包括氧化一还原反应). 下面是离子间不能共存的几种情况: 1.由于发生复分解...
 [注解与辨疑3] 化学方程式含义读法与书写 作者:马文礼 来源:未知 日期:2014-01-11 16:51:26 点击:12993 所属专题:化学反应方程式
[注解与辨疑3] 化学方程式含义读法与书写 作者:马文礼 来源:未知 日期:2014-01-11 16:51:26 点击:12993 所属专题:化学反应方程式
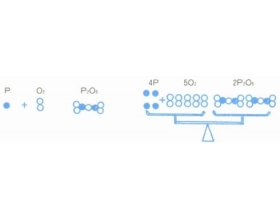
化学家用元素符号代表元素,用元素符号的组合――分子式代表各种各样的物质。我们把元素符号和分子式,分别比作英语中的字母和词汇。这比较清晰地表达了元素符号和分子式之间的关系。化学家正是依照这种思想,把分子式用适当的符号(如+,=)联结而成的句子来表示物质间...
 [注解与辨疑3] 高中化学离子共存问题常见误区 作者:刘明 来源:未知 日期:2012-03-01 18:48:15 点击:10054 所属专题:离子共存
[注解与辨疑3] 高中化学离子共存问题常见误区 作者:刘明 来源:未知 日期:2012-03-01 18:48:15 点击:10054 所属专题:离子共存
我们在书写化学方程式是会遇到很多的陷阱误区例如:题设情景,如酸碱性环境,无色透明溶液、产生气体、沉淀,发生氧化还原反应或复分解反应而不能共存, 这里还要注意以下几点: (1)、有些学生认为有色溶液不是“透明溶液”,这是错的。如果题设为无色透明溶液,则可排除含...
 [注解与辨疑3] “复分解反应条件之一是生成难溶物质”这句话对吗? 作者:蒋景耘 来源:未知 日期:2012-02-15 10:24:55 点击:2893 所属专题:复分解反应 条件
[注解与辨疑3] “复分解反应条件之一是生成难溶物质”这句话对吗? 作者:蒋景耘 来源:未知 日期:2012-02-15 10:24:55 点击:2893 所属专题:复分解反应 条件
新、旧教材在阐述复分解反应的条件时都是这样阐述的,其实这会给学生带来负面影响,不少学生甚至认为只有生成难溶物质才会有沉淀。其实只要溶质的量超过溶解度所允许值,不论难溶物质还是易溶物质都能沉淀,反应也就因此而发生了(学生往往把生成沉淀和析出晶体割离开来理解...
 [注解与辨疑3] 高中化学复杂电离方程式 作者:李文才 来源:未知 日期:2016-01-22 14:37:18 点击:4104 所属专题:电离方程式
[注解与辨疑3] 高中化学复杂电离方程式 作者:李文才 来源:未知 日期:2016-01-22 14:37:18 点击:4104 所属专题:电离方程式
两性氢氧化物: H + +AlO 2 - +H 2 O Al(OH) 3 Al 3+ +3OH - 强酸的酸式盐: NaHSO4==Na + +H + +SO 4 2- (水溶液) NaHSO4==Na + +HSO 4 2- (熔融状态) 弱酸的酸式盐: NaHCO 3 ==Na + +HCO 3 - 复盐: KAl(SO 4 ) 2 ==K + +Al 3+ +2SO 4 2- 络合物: Ag(NH 3...
 [注解与辨疑3] 过氧化钠在离子方程式中要拆开吗? 作者:许浩年 来源:未知 日期:2011-08-30 12:44:12 点击:6515 所属专题:过氧化钠 离子方程式书写
[注解与辨疑3] 过氧化钠在离子方程式中要拆开吗? 作者:许浩年 来源:未知 日期:2011-08-30 12:44:12 点击:6515 所属专题:过氧化钠 离子方程式书写
在水溶液中不能拆,因为固体的Na2O2中过氧根离子不能自由移动,所以不能拆,但在水溶液中没过氧根离子,过氧根离子遇水马上反应生成OH-和O2,所以就不存在过氧根离子在水溶液里,所以不能拆。但在熔融状态,没有水,Na2O2能电离出过氧根离子.完全电离.所以要拆.初中高中一般不讲熔融...
 [注解与辨疑3] 书写离子方程式时的“拆”与“不拆”问题 作者:袁建标 来源:未知 日期:2011-08-29 19:18:44 点击:13980 所属专题:离子方程式书写
[注解与辨疑3] 书写离子方程式时的“拆”与“不拆”问题 作者:袁建标 来源:未知 日期:2011-08-29 19:18:44 点击:13980 所属专题:离子方程式书写
写离子方程式时,强电解质一定拆,弱电解质一定不拆。水溶液中,强电解质在水中完全电离,所以肯定拆;而弱电解质不能完全电离,因此不拆。但是在非水溶液中进行时,或反应体系中水很少时,那就要看情况了。 在固相反应时,无论是强电解质还是弱电解质,无论这反应的实质是...
 [注解与辨疑3] 化学方程式书写注意事项 作者:蒋景耘 来源:未知 日期:2011-08-29 18:54:18 点击:33806 所属专题:化学反应方程式
[注解与辨疑3] 化学方程式书写注意事项 作者:蒋景耘 来源:未知 日期:2011-08-29 18:54:18 点击:33806 所属专题:化学反应方程式
化学反应方程式 一.化学方程式的书写原则 必须以客观事实为依据,不能凭空臆造事实上不存在的物质和化学反应。 遵守质量守恒定律,使等号两边原子的种类和数目必须相等。 二.化学方程式的书写步骤 书写化学方程式要按一定步骤进行,避免出现一些不必要的错误,如漏掉反应条...
 [注解与辨疑3] 物质的溶解性与溶解度的关系 作者:张修鹏 来源:未知 日期:2011-06-17 20:19:27 点击:7140 所属专题:溶解性 溶解度
[注解与辨疑3] 物质的溶解性与溶解度的关系 作者:张修鹏 来源:未知 日期:2011-06-17 20:19:27 点击:7140 所属专题:溶解性 溶解度
溶解度(20℃)/g >10 1~10 0.01~1 <0.01 溶解性 易溶 可溶 微溶 难溶...
 [注解与辨疑3] 离子反应中的不一定 作者:江已舒 来源:未知 日期:2011-06-16 18:33:27 点击:13457 所属专题:离子反应 不一定
[注解与辨疑3] 离子反应中的不一定 作者:江已舒 来源:未知 日期:2011-06-16 18:33:27 点击:13457 所属专题:离子反应 不一定
在离子反应这一节中知识点很多,但也有很多的不一定。 1、电解质不一定导电。 判断一种化合物是否为电解质,要看其在水溶液或在熔融状态下能否导电,也就是说电解质导电要有条件,在水溶液中或在熔融状态下。例如氯化钠是电解质,固体形式不导电,但其在水溶液中或在熔...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。离子方程式书写的核心难点之一,在于 “特殊物质的拆分判断”―― 部分物质因结构、溶...
电离方程式是表征物质在水溶液或熔融态电离过程的化学用语,常规强电解质(如 NaCl、HS...
离子方程式书写四大原则之一关键是拆分问题 1、 溶解性规律 常规 K + 、 Na + 、 NH 4...
1.警惕“颜色陷阱”: ①若限定溶液无色,则Cu 2+ 、Fe 3+ 、Fe 2+ 、Cr 2 O 7 2 ...
用化学式 和 离子符号等来表示物质离解成自由移动离子过程的式子叫做电离方程式。 书...
一句话总结:熔融态就是 固体加热熔化后的状态 。 在某个层面上,它和液态是一回事 (...
AgOH 是经常被忽略其存在的一种化合物,那是因为AgOH的热稳定性极差,室温就能分解,...
金属导电是自由电子的定向移动。电解质溶液导电是阴阳离子的定向移动。电解质溶液是指...