
|
学习小专题 |

|
学习小专题 |
 [探讨与扩展3] 自偶电离概念对中学化学教学的影响 作者:化学自习室 来源:未知 日期:2025-09-29 15:24:57 点击:859 所属专题:自偶电离
[探讨与扩展3] 自偶电离概念对中学化学教学的影响 作者:化学自习室 来源:未知 日期:2025-09-29 15:24:57 点击:859 所属专题:自偶电离
电离概念是中学一个基本概念,用以区分电解质和非电解质、共价化合物和离子化合物。其中电离的结果产生自由移动的离子。从高一学生掌握物质分类开始,一直到高二深入学习 电离平衡 的观念,这个概念始终贯穿整个高中化学,可以说是高中化学基本概念的一个基石。 最近刷...
 [探讨与扩展3] 纯硫酸等共价化合物的导电原因 作者:关平 来源:未知 日期:2021-11-29 19:34:50 点击:7553 所属专题:硫酸 共价化合物 自耦电离
[探讨与扩展3] 纯硫酸等共价化合物的导电原因 作者:关平 来源:未知 日期:2021-11-29 19:34:50 点击:7553 所属专题:硫酸 共价化合物 自耦电离
一、问题的提出 由于离子化合物如氯化钠其自身就含有离子,不论在熔融状态还是在水溶液中都能产生自由移动的离子,这些自由离子在外加电场的作用下能定向移动,因而能导电。液态氯化氢由于自身没有离子的存在故不能导电,只有在水溶液中才能产生自由离子而导电。因此人...
 [注解与辨疑j] 盐都是强电解质吗? 作者:甑炳杨 来源:未知 日期:2017-04-18 11:26:16 点击:15929 所属专题:强电解质
[注解与辨疑j] 盐都是强电解质吗? 作者:甑炳杨 来源:未知 日期:2017-04-18 11:26:16 点击:15929 所属专题:强电解质
在中学化学教学中,我们认为盐一般都是强电解质。盐类大多数形成离子晶体,它们的电离程度都很大。一些难溶的盐,如BaSO 4 、CaCO 3 等,溶于水的部分电离程度都很大,也被称为强电解质。 但是,有些盐的阳离子和阴离子所带电荷数较大,半径又小,阴、阳离子间的相互作用较...
 [探讨与扩展3] 水溶液中为什么不可能存在氧离子? 作者:何清松 来源:未知 日期:2017-04-18 10:59:30 点击:7614 所属专题:离子共存
[探讨与扩展3] 水溶液中为什么不可能存在氧离子? 作者:何清松 来源:未知 日期:2017-04-18 10:59:30 点击:7614 所属专题:离子共存
首先这是因为,首先O原子的第一电离能为正值,也就是说O(g)原子结合一个电子变成O - (g)离子是放出能量的。但O - (g)离子再结合一个电子生成O 2- 离子则是吸热的。 且I 2 的绝对值远大于I 1 ,这就是说O 2- 的能量远比O - 和O要高,O 2- 从能量的观点看,远不如O -...
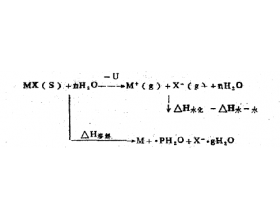 [探讨与扩展3] 浅议物质溶解过程的能量变化 作者:玉素甫 来源:未知 日期:2016-03-10 18:20:01 点击:2689 所属专题:物质溶解过程
[探讨与扩展3] 浅议物质溶解过程的能量变化 作者:玉素甫 来源:未知 日期:2016-03-10 18:20:01 点击:2689 所属专题:物质溶解过程
初中化学课本中解释溶解过程的热效应时写道:“怎样解释物质溶解时,有的吸热,而有的放热呢?这是因为,物质溶解在水里,通常发生两种过程:一种是溶质 的分子(或离子)的扩散过程,这种过程吸收热量,是物理过程;另一种是溶质的分子 (或离子) 和水分子作用,形成水合分...
 [探讨与扩展3] 弱碱阳离子与弱酸根一定不能大量共存吗? 作者:万胜 来源:未知 日期:2013-03-07 10:43:29 点击:4727 所属专题:离子共存 双水解反应
[探讨与扩展3] 弱碱阳离子与弱酸根一定不能大量共存吗? 作者:万胜 来源:未知 日期:2013-03-07 10:43:29 点击:4727 所属专题:离子共存 双水解反应
分析:弱碱阳离子与弱酸很能不能大量共存,不能一概而论。而在中学不少资料上的离子能否共存习题中都认为:弱碱阳离子与弱酸根不能大量共存,这是错误的。如醋酸铵、碳酸氢铵等就是弱碱阳离子与弱酸根可以大量共存的例子。而有些弱碱阳离子与弱酸根互促水解程度大,甚至...
 [探讨与扩展3] 复分解反应条件之一是生成难溶物质吗? 作者:潘祥泰 来源:未知 日期:2013-03-07 10:30:25 点击:3007 所属专题:复分解反应
[探讨与扩展3] 复分解反应条件之一是生成难溶物质吗? 作者:潘祥泰 来源:未知 日期:2013-03-07 10:30:25 点击:3007 所属专题:复分解反应
分析: 新、旧教材在阐述复分解反应的条件时都是这样阐述的,其实这会给学生带来负面影响,不少学生甚至认为只有生成难溶物质才会有沉淀。其实只要溶质的量超过溶解度所允许值,不论难溶物质还是易溶物质都能沉淀,反应也就因此而发生了(学生往往把生成沉淀和析出晶体割离...
 [注解与辨疑j] 透析电解质中的八大关系 作者:舒龙昌 来源:未知 日期:2016-02-02 20:34:29 点击:32030 所属专题:电解质判断 弱电解质判断
[注解与辨疑j] 透析电解质中的八大关系 作者:舒龙昌 来源:未知 日期:2016-02-02 20:34:29 点击:32030 所属专题:电解质判断 弱电解质判断
一.电解质、非电解质概念间的关系 电解质是指在水溶液中或熔化状态下能够导电的化合物;非电解质是指在水溶液中和熔化状态下都不能够导电的化合物。显然电解质和非电解质是对化合物的一种分类,因此混合物既不是电解质也不是非电解质。此外“不是电解质”与非电解质不...
 [探讨与扩展3] 为什么有些固体物质溶解度随温度升高而下降 作者:刘心宇 来源: 日期:2026-01-13 20:59:18 点击:13212 所属专题:溶解度 溶解热
[探讨与扩展3] 为什么有些固体物质溶解度随温度升高而下降 作者:刘心宇 来源: 日期:2026-01-13 20:59:18 点击:13212 所属专题:溶解度 溶解热
大多数固体物质溶于水时吸收热量,根据平衡移动原理,当温度升高时,平衡有利于向吸热的方向移动,所以,这些物质的溶解度随温度升高而增大,例如KNO 3 、NH 4 NO 3 等。有少数物质,溶解时有放热现象,一般地说,它们的溶解度随着温度的升高而降低,例如 Ca(OH) 2 等...
 [探讨与扩展3] 溶解过程的探析 作者:陈恒 来源: 日期:2007-07-18 07:55:30 点击:11786 所属专题:物质溶解过程
[探讨与扩展3] 溶解过程的探析 作者:陈恒 来源: 日期:2007-07-18 07:55:30 点击:11786 所属专题:物质溶解过程
溶解过程是一个复杂的物理化学过程,在此列举几例供参考。 实验事实与生活经验 理解与解释 提升 Fe 、 CaCO 3 不溶于水,而溶于盐酸 前者是物理性溶解,后者是化学性溶解 化学性质 少量的氧气溶于水,二氧化碳气体溶于水 前者得到很稀的溶液,后者得到的是碳酸溶液 质...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
大多数固体物质溶于水时吸收热量,根据平衡移动原理,当温度...
电离概念是中学一个基本概念,用以区分电解质和非电解质、共...
HI 10 11 HBr 10 9 HCl 10 7 HClO 4 10 7 HClO 3 10 3 H 2 SO 4 10 2 HNO 3 20 H 3 O +...
一、问题的提出 由于离子化合物如氯化钠其自身就含有离子,不...
我们通常把在水溶液中或熔化状态下能导电的化合物叫做电解质...
在中学化学教学中,我们认为盐一般都是强电解质。盐类大多数...
首先这是因为,首先O原子的第一电离能为正值,也就是说O(g)原...
氯化铜溶液跟碳酸钠溶液进行反应时,实验的结果是除有蓝色沉...