
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!

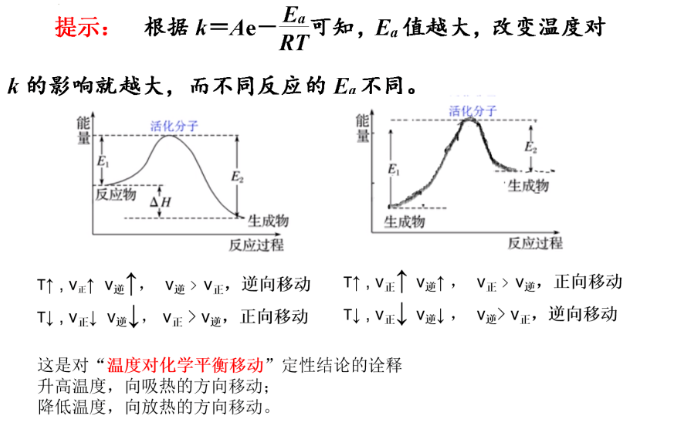

本题考查了阿伦尼乌斯公式中温度和速率常数的关系,即温度升高,速率常数变大。
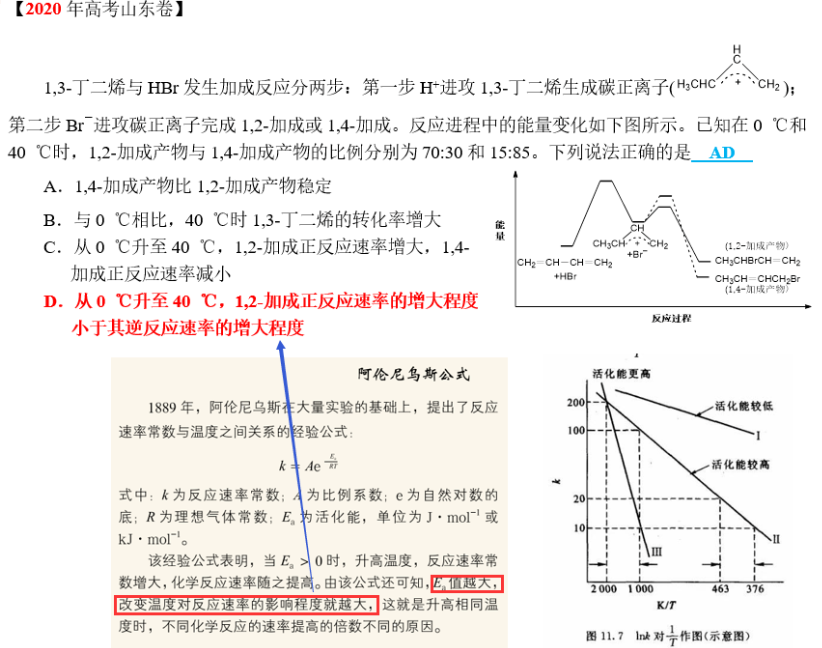
本题考查了阿伦尼乌斯公式中活化能大小决定了温度对速率影响程度的关系,即活化能越大,温度对反应速率的影响程度越大。
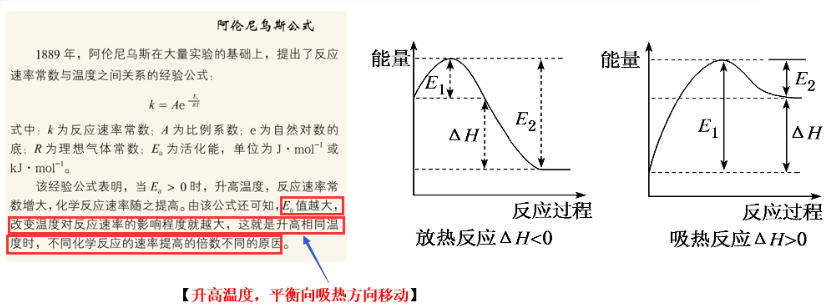
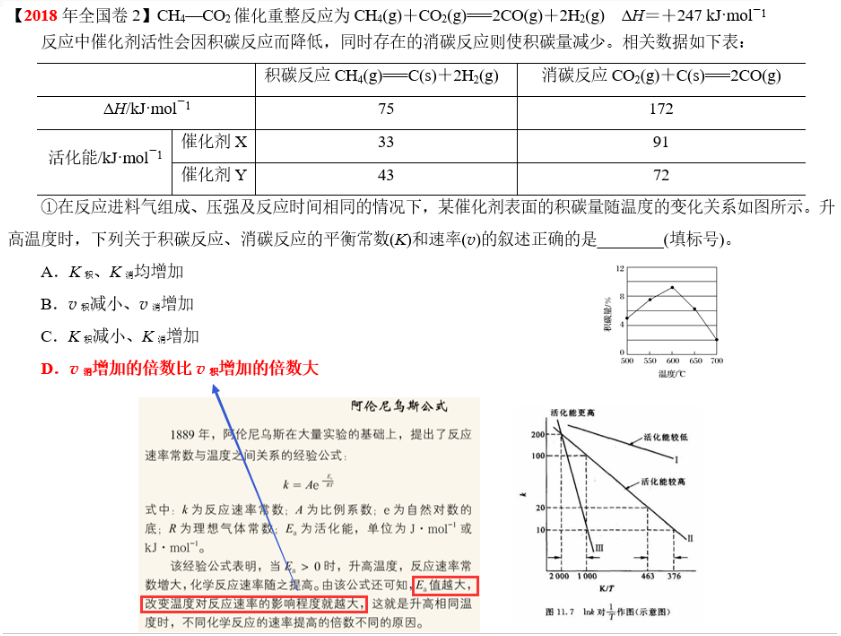
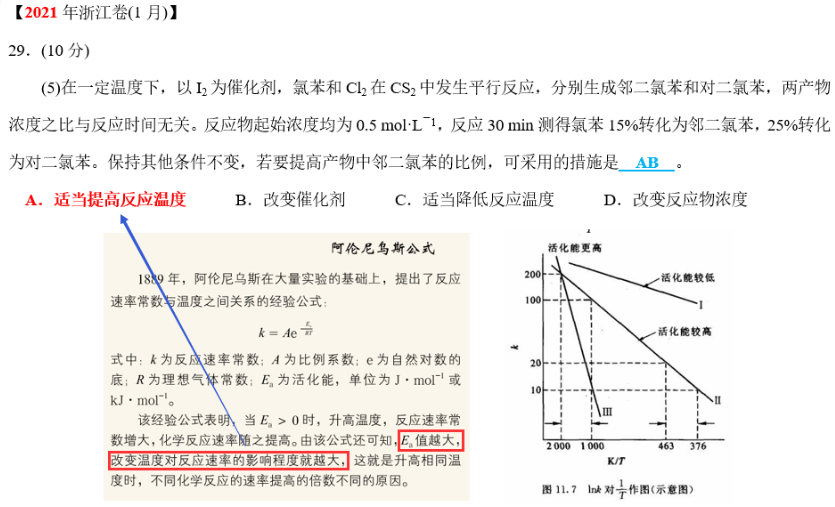
本题依据平行反应活化能的不同,通过调控温度来不同程度改变平行反应的速率,以及利用催化剂的选择性以提高合邻二氯苯的比例。
小结:在以上高考题中,应用阿伦尼乌斯公式解释了温度与速率的关系以及利用温度与速率的关系进行生产条件的调控:
(1)温度升高,速率常数增大;
(2)温度对活化能大的反应速率的影响程度要大,所以升高温度,平衡向吸热反应的方向移动;
(3)利用温度对活化能不同的反应速率影响程度不同,通过调控温度来提高目标产品的选择性。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
在化学反应中,驱动力指的是推动反应进行的内在因素,它决定...
一.核心概念辨析 中间体:寿命长于分子振动的瞬态物种,多步...
活化分子百分数和活化分子数,理解它对掌握化学反应速率至关...
化学反应的焓变越大,代表这个反应受温度变化的影响越大吗?...
在化学热力学和分析化学中,我们常常听到这样的说法:“如果...
...