
|
学习小专题 |

|
学习小专题 |
 [方法与规律i] 多重平衡体系化学平衡常数计算题的两种解法 作者:化学自习室 来源:未知 日期:2025-11-18 16:11:03 点击:371 所属专题:多重平衡 平衡计算
[方法与规律i] 多重平衡体系化学平衡常数计算题的两种解法 作者:化学自习室 来源:未知 日期:2025-11-18 16:11:03 点击:371 所属专题:多重平衡 平衡计算
...
 [方法与规律i] 阿伦尼乌斯经验公式:连接温度与化学反应速率的桥梁 作者:化学自习室 来源:未知 日期:2025-10-26 18:12:50 点击:1377 所属专题:阿伦尼乌斯公式
[方法与规律i] 阿伦尼乌斯经验公式:连接温度与化学反应速率的桥梁 作者:化学自习室 来源:未知 日期:2025-10-26 18:12:50 点击:1377 所属专题:阿伦尼乌斯公式
一、公式提出的背景 19世纪末,化学家们逐渐意识到温度对化学反应速率具有显著影响,但缺乏一个普适的定量描述方法。1889年,瑞典化学家斯万特·阿伦尼乌斯(Svante Arrhenius)在研究电解质溶液导电性及反应速率时,提出了一个革命性的观点:只有具备足够能量的分子才...
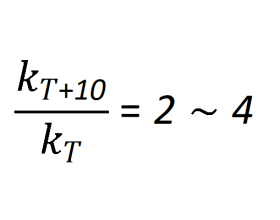 [方法与规律i] 范特霍夫方程在高考中的应用 作者:化学自习室 来源:未知 日期:2025-10-26 17:48:57 点击:542 所属专题:范特霍夫方程
[方法与规律i] 范特霍夫方程在高考中的应用 作者:化学自习室 来源:未知 日期:2025-10-26 17:48:57 点击:542 所属专题:范特霍夫方程
前言:范特霍夫方程是荷兰化学家雅各布斯·亨里克斯·范托夫(VantHoff equation)于1884年提出的。用于描述温度对化学反应平衡常数的影响。该方程可用来计算化学反应在不同温度下的平衡常数,从而预测化学反应的热力学行为。 范特霍夫方程在高考中虽不作为核心考点考查,...
 [方法与规律i] 浓度平衡常数,压强平衡常数之间的换算 作者:化学自习室 来源:未知 日期:2025-10-24 10:46:52 点击:655 所属专题:平衡常数
[方法与规律i] 浓度平衡常数,压强平衡常数之间的换算 作者:化学自习室 来源:未知 日期:2025-10-24 10:46:52 点击:655 所属专题:平衡常数
假设对于反应 a A(g) + b B(g) g G(g) + h H(g) 中各物质均为理想气体,那么则有平衡常数:浓度平衡常数Kc、分压平衡常数Kp和物质的量分数平衡常数Kx。 我们知道浓度平衡常数Kc是温度的函数,只与温度有关。而分压平衡常数Kp与浓度平衡常数Kc有什么换算关系?Kx是否也是...
 [方法与规律i] 恒温恒容条件下,压强平衡常数快速解法 作者:化学自习室 来源:未知 日期:2025-08-13 10:38:13 点击:416 所属专题:分压平衡常数
[方法与规律i] 恒温恒容条件下,压强平衡常数快速解法 作者:化学自习室 来源:未知 日期:2025-08-13 10:38:13 点击:416 所属专题:分压平衡常数
例:某温度、起始压强为100 kPa下,若将2mol SO 2 和1molO 2 ,通入恒容密闭容器中,达到平衡时,测得SO 3 的分压是60kPa,则该温度下,反应的平衡常数K p 解析:...
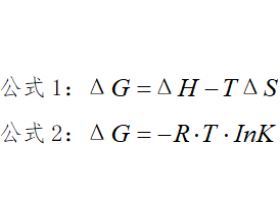 [方法与规律i] 范特霍夫方程在高中化学中有三个应用 作者:化学自习室 来源:未知 日期:2025-08-07 08:06:56 点击:1028 所属专题:范特霍夫方程
[方法与规律i] 范特霍夫方程在高中化学中有三个应用 作者:化学自习室 来源:未知 日期:2025-08-07 08:06:56 点击:1028 所属专题:范特霍夫方程
公式推导 一、公式推导 公式1是大家都熟悉的吉普斯自由能公式,用来判断反应能否自发进行以及自发进行的温度。 公式2(常常出现在题目的已知信息中)相同温度下,K越大,ΔG越小,反应的趋势越大,反应越完全。 ΔG:吉普斯自由能 R: 摩尔气体常量,8.314J/(mol·K) K: ...
 [方法与规律i] 高考题中有关范特霍夫方程的考查 作者:化学自习室 来源:未知 日期:2025-08-07 07:57:43 点击:370 所属专题:范特霍夫方程
[方法与规律i] 高考题中有关范特霍夫方程的考查 作者:化学自习室 来源:未知 日期:2025-08-07 07:57:43 点击:370 所属专题:范特霍夫方程
...
 [方法与规律i] 能垒、活化能及化学反应机理 作者:化学自习室 来源:未知 日期:2024-01-02 08:50:44 点击:6143 所属专题:能垒 活化能 化学反应机理
[方法与规律i] 能垒、活化能及化学反应机理 作者:化学自习室 来源:未知 日期:2024-01-02 08:50:44 点击:6143 所属专题:能垒 活化能 化学反应机理
什么是活化能、能垒? 1 、能垒 活化分子含有的能参加化学反应的最低限度的能量,称为化学反应的能垒,或称能阈或能障。 对于一个化学反应,要想从反应物变成产物必须要 “ 翻山越岭 ” 。能垒,则是反应物变成产物所必须克服的能量障碍。能垒的高度表示了反应物转变为...
 [方法与规律i] “虚拟路径法”在化学学习中的妙用 作者:化学自习室 来源:未知 日期:2023-10-30 08:27:46 点击:889 所属专题:等效法
[方法与规律i] “虚拟路径法”在化学学习中的妙用 作者:化学自习室 来源:未知 日期:2023-10-30 08:27:46 点击:889 所属专题:等效法
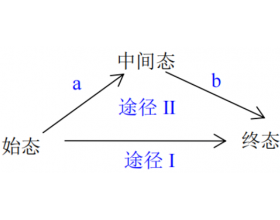
化学学习过程中,我们经常碰到这样一类问题,如图一,由始态经途径I直接到终态,理解或解决起来很困难,而且这类问题往往与过程无关,只与始、终态有关。此时,我们不妨“迂回”一下,重新规划一下路径,按途径II进行,途径II分若干步,每一步是很容易理解或者操作起来很方...
 [方法与规律i] 判断基元反应思维过程 作者:董拥军 来源:未知 日期:2023-10-13 17:59:40 点击:467 所属专题:基元反应
[方法与规律i] 判断基元反应思维过程 作者:董拥军 来源:未知 日期:2023-10-13 17:59:40 点击:467 所属专题:基元反应
第一页 第二页 第三页...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
...
一、公式提出的背景 19世纪末,化学家们逐渐意识到温度对化学...
假设对于反应 a A(g) + b B(g) g G(g) + h H(g) 中各物质均为理想气体,...
例:某温度、起始压强为100 kPa下,若将2mol SO 2 和1molO 2 ,通入恒...
...
什么是活化能、能垒? 1 、能垒 活化分子含有的能参加化学反应...
化学学习过程中,我们经常碰到这样一类问题,如图一,由始态...
第一页 第二页 第三页...