
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、等效平衡的概念
在一定条件(恒温恒容或恒温恒压)下,只是起始加入情况不同的同一可逆反应达到平衡后,任何相同组分的百分含量(体积分数、物质的量分数等)均相同,这样的化学平衡互称等效平衡(包括“等同平衡”)。
概念的理解:
(1)外界条件相同:通常可以是①恒温、恒容(同T同V),②恒温、恒压(同T同P),读题时注意勾画出这些条件。
(2)相同的平衡状态:通常是指平衡混合物各组分的百分含量相同,但各组分的物质的量、浓度可能不同。
(3)平衡状态(终态)只与始态有关,而与途径无关,(如:①无论反应从正反应方向开始,还是从逆反应方向开始②投料是一次还是分成几次③反应容器经过扩大—缩小或缩小—扩大的过程,)只要起始浓度相当,就达到相同的平衡状态。
概念的理解:
(1)外界条件相同:通常可以是①恒温、恒容(同T同V),②恒温、恒压(同T同P),读题时注意勾画出这些条件。
(2)相同的平衡状态:通常是指平衡混合物各组分的百分含量相同,但各组分的物质的量、浓度可能不同。
(3)平衡状态(终态)只与始态有关,而与途径无关,(如:①无论反应从正反应方向开始,还是从逆反应方向开始②投料是一次还是分成几次③反应容器经过扩大—缩小或缩小—扩大的过程,)只要起始浓度相当,就达到相同的平衡状态。
二、等效平衡的判断及处理
1、步骤
(1) 进行等效转化—— 一边倒法,即按照反应方程式的计量数之比转化到同一边的量,与题干所给起始投料情况比较。
(2) 判断起始浓度是否相当。
2、三种类型:
I类:恒温恒容下对于反应前后气体体积发生变化的反应来说(即△n≠0的体系):等效转化后,对应各物质起始投料的物质的量与原平衡起始态相同。
II类:恒温恒容下对于反应前后气体体积没有变化的反应来说(即△n=0的体系):等效转化后,只要反应物(或生成物)的物质的量的比例与原平衡起始态相同,两平衡等效。
III类:恒温恒压下对于气体体系等效转化后,要反应物(或生成物)的物质的量的比例与原平衡起始态相同,两平衡等效。
其口诀可概括为:等压比相等;等容量相等,但若系(气体系数)不变,可为比相等【三种情况前提:等T】。
解题的关键,在读题时分清类别,用相应的方法求解。
题型1:反应前后气体体积变化的可逆反应在恒温、恒容条件下建立等效平衡
【例题】1、在t℃时,向2L密闭容器中放入1molA和1molB,发生下列反应:A(g)+B(g)![]() C(g)+2D(g),平衡时C的含量为m%,保持其他条件不变,若按下列配比将物质放入容器中达到平衡时,C的含量仍为m%的是 ( C )
C(g)+2D(g),平衡时C的含量为m%,保持其他条件不变,若按下列配比将物质放入容器中达到平衡时,C的含量仍为m%的是 ( C )
A、2molA和1molB B、2molD和A、B、C各1mol C、1molC和2molD D、1molC和1molD
例2、在一定温度下,把2mol SO2和1mol O2通入一个一定容积的密闭容器里,发生如下反应:2SO2 +O2 ![]() 2SO3,当此反应进行到一定程度时,反应混合物就处于化学平衡状态。现在该容器中维持温度不变,令a、b、c分别代表初始加入的SO2、O2和SO3的物质的量(mol)。如a、b、c取不同的数值,它们必须满足一定的相互关系,才能保持达到平衡时,反应混合物中三种气体的体积分数仍和上述平衡时的完全相同。请填写下列空白:
2SO3,当此反应进行到一定程度时,反应混合物就处于化学平衡状态。现在该容器中维持温度不变,令a、b、c分别代表初始加入的SO2、O2和SO3的物质的量(mol)。如a、b、c取不同的数值,它们必须满足一定的相互关系,才能保持达到平衡时,反应混合物中三种气体的体积分数仍和上述平衡时的完全相同。请填写下列空白:
⑴若a=0,b=0,则c= _____________。
⑵若a=0.5,则b= _________ 和c= __________。
⑶a、b、c必须满足的一般条件是(请用两个方程式表示,其中一个只含a和c,另一个只含b和c):_____________。
答案:(1)2mol
(2)b=0.25mol,c=1.5mol
(3)a+c=2 b+c/2=1(或2b+c=2)
【练习】
1、在一个固定体积的密闭容器中,加入2mol A和1mol B,发生反应:2A(g)+B(g) ![]() 3C(g)+D(g) 达平衡时,c (C)=W mol/L。若维持容器内体积和温度不变,按下列四种配比作起始物质,达平衡后,C浓度仍为W mol/L的是( AD )
3C(g)+D(g) 达平衡时,c (C)=W mol/L。若维持容器内体积和温度不变,按下列四种配比作起始物质,达平衡后,C浓度仍为W mol/L的是( AD )
(A)1mol A+0.5mol B+1.5mol C+0.5 D
(B)2mol A+1mol B+3mol C+1mol D
(C)3mol C+1mol D+1mol B
(D)3mol C+1mol D
2、(变式)将2molSO2和2molSO3 气体混合于固定体积的密闭容器中,在一定条件下发生反应:2SO2(气)+O2(气) ![]() 2SO3 (气),平衡时SO3为n mol。相同温度下,分别按下列配比在相同体积的密闭容器中加入起始物质,平衡时SO3的物质的量大于n mol的是( CD )
2SO3 (气),平衡时SO3为n mol。相同温度下,分别按下列配比在相同体积的密闭容器中加入起始物质,平衡时SO3的物质的量大于n mol的是( CD )
A、2mol SO2+1 molO2 B、4molSO2+1molO2
C、2molSO2+1molO2+2molSO3 D、3molSO2+1molO2+1molSO3
3、某温度下,向某密闭容器中加入1molN2和3molH2,使之反应合成NH3,平衡后测得NH3的体积分数为m。若T不变,只改变起始加入量,使之反应平衡后NH3的体积分数仍为m,若N2、H2、NH3的加入量用X、Y、Z表示应满足:
(1)恒定T、V:
[1]若X=0,Y=0,则Z= 。
[2]若X=0.75,Y=,Z= 。
[3]X、Y、Z应满足的一般条件是 。
(2)恒定T、P:
[1]若X=0、Y=0,则Z 。
[2]若X=0.75,则Y ,Z 。
[3]X、Y、Z应满足的一般条件是 。
题型2:反应前后气体体积不变的可逆反应在恒温、恒容条件下建立等效平衡
[例题1]在一恒温恒容密闭容器中,A、B气体可建立如下平衡: 2A(g)+2B(g) ![]() C(g)+3D(g)现分别从两条途径建立平衡:Ⅰ. A、B的起始量均为2mol;Ⅱ. C、D的起始量分别为2mol和6mol。下列叙述不正确的是:(B)
C(g)+3D(g)现分别从两条途径建立平衡:Ⅰ. A、B的起始量均为2mol;Ⅱ. C、D的起始量分别为2mol和6mol。下列叙述不正确的是:(B)
A、Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成相同
B、Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成不同
C、达到平衡时,途径Ⅰ的和途径Ⅱ体系内混合气体平均相对分子质量相同
D、达到平衡时,途径Ⅰ的气体密度为途径Ⅱ密度的1/2
例2、在一个固定体积的密闭容器中,保持一定温度,进行以下反应: H2(g)+Br2(g)![]() 2HBr(g),已知加入1molH2和2molBr2时,达到平衡后生成amolHBr(见下表“已知项”)。在相同条件下,且保持平衡时各组分的百分含量不变,对下列编号(1)-(3)的状态,填写表中空白:
2HBr(g),已知加入1molH2和2molBr2时,达到平衡后生成amolHBr(见下表“已知项”)。在相同条件下,且保持平衡时各组分的百分含量不变,对下列编号(1)-(3)的状态,填写表中空白:
编号 | 起始状态(mol) | 平衡时HBr的 物质的量(mol) | ||
H2 | Br2 | HBr | ||
已知 | 1 | 2 | 0 | a |
(1) | 2 | 4 | 0 |
|
(2) |
|
| 1 | 0.5a |
(3) | m | n(n≥2m) |
|
|
(1)2a (2)0 0.5 (3)2n-4m (n-m)a
【练习】1、在一个1L的密闭容器中,加入2molA和1molB ,发生下述反应:2A(g)+2B(g) ![]() 3C(g)+D(g),达到平衡时,C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L的是 ( D )
3C(g)+D(g),达到平衡时,C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L的是 ( D )
A、3mol C+1mol D B、1mol A+0.5mol B+1.5mol C+0.5mol D
C、1mol A+0.5mol B+1.5mol C D、4mol A+2mol B
2、在一固定容积的密闭容器中充入2molA和1molB,发生反应:2A(气)+B(气) ![]() xC(气),达到平衡后,C的体积分数为W%。若维持容器体积和温度不变,按0.6molA、0.3molB和1.4molC为起始物质,达到平衡后,C的体积分数仍为W%,则x值为 ( BC )
xC(气),达到平衡后,C的体积分数为W%。若维持容器体积和温度不变,按0.6molA、0.3molB和1.4molC为起始物质,达到平衡后,C的体积分数仍为W%,则x值为 ( BC )
A、1 B、2 C、3 D、4
题型3:可逆反应在恒温、恒压条件下建立等效平衡
【例题】1、
[思考]若将题型2例1中的容积固定容器改成压强不变容器,同样分析4个选项,则情形又如何?(参考答案:AC)
【例题】2、
[思考]若将题型1例2中的容积固定容器改成压强不变容器,同样回答上述问题(第3小问括号内文字去掉),则情形又如何?(参考答案:①c>0;② b=0.25,c≥0;③a:b=2:1,c≥0或a=b=0,c>0)
⑴若a=0,b=0,则c= _____________。
⑵若a=0.5,则b= _________ 和c= __________。
⑶a、b、c必须满足的一般条件是: __________________________________________________。
【例题】3、【2003年江苏高考试题】恒温、恒压下,在一个可变容积的容器中发生如下反应: A(g)+B(g)![]() C(g)
C(g)
(1)若开始时放入1 mol A和1 mol B,到达平衡后,生成a mol C,这时A的物质的量为 mol。
(2)若开始时放入3 mol A和3mol B ,到达平衡后,生成C的物质的量为 mol。
(3)若开始时放入x molA,2molB和1molC,到达平衡后,A和C的物质的量分别是y mol和3a mol,则x= ,y= 。平衡时,B的物质的量 (选填一个编号)
(A)大于2 mol (B)等于2 mol (C)小于2mol (D)可能大于、等于或小于2mol
作出判断的理由是 。
(4)若在(3)的平衡混合物中再加入3mol C,待再次到达平衡后,C的物质的量分数是 。
(5)若维持温度不变,在一个与(1)反应前起始体积相同、且容积固定的容器中发生上述反应。开始时放入1mol A和1molB到达平衡后生成b mol C。将b与(1)小题中的a进行比较 (选填一个编号)。
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和b的大小
作出此判断的理由是 。
解析 恒温恒压下,只要A和B的投入量与起始成比例,则A、B、C的百分含量均不变,平衡时各物质的量和开始成比例,据此(1)、(2)、(3)、(4)问很容易作答;当改变条件,使成为恒温恒容时,由于该反应是一分子数目减少的反应,随着反应的进行,容器内的压强在减少,(5)相对于(1)而言,可以等效看成(1)达到平衡后,再将容器体积扩大,则平衡向左移动,C的百分含量降低,故b<a
![]() [答案](1)(1-a) (2)3a (3)2 3-3a 丁 若3a>1,B的物质的量小于2mol;若3a=1,B的物质的量等于2mol;若3a<1,B的物质的量大于2mol;
[答案](1)(1-a) (2)3a (3)2 3-3a 丁 若3a>1,B的物质的量小于2mol;若3a=1,B的物质的量等于2mol;若3a<1,B的物质的量大于2mol;
(4)a/(2-a) (5)乙;因为(5)小题中容器容积不变,而(1)小题中容器的容积缩小,所以(5)小题的容器中的压强小于(1)小题容器中的压强,有利于逆向反应,故反应达到平衡后a>b。
【练习】
1、在一个1L的密闭容器中,加入2molA和1molB ,发生下述反应:2A(g)+B(g) ![]() 3C(g)+D(g)达到平衡时,C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的压强和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L(或C的体积分数仍是a%)的是 ( ABD )
3C(g)+D(g)达到平衡时,C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的压强和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L(或C的体积分数仍是a%)的是 ( ABD )
A、3mol C+1mol D B、1mol A+0.5mol B+1.5mol C+0.5mol D
C、1mol A+0.5mol B+1.5mol C D、4mol A+2mol B
2、在恒温、恒压的条件下,向可变容积的密闭容器中充入3LA和2LB,发生如下反应:3A(气)+2B(气)![]() xC(气)+yD(气)
xC(气)+yD(气)
达到平衡时,C的体积分数为m%。若维持温度压强不变,将0.6LA 、0.4LB、4LC、0.8LD作为起始物质充入密闭容器中,达到平衡时C的体积分数仍为m%,则X、Y的值分别为 ( CD )
A x=3 y=1 B x=4 y=1 C x=5 y =1 D x=10 y=2
3、 (★★★★★)在一定温度下,把2.0体积N2和6.0体积H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通,如图所示。容器中发生的反应如下:
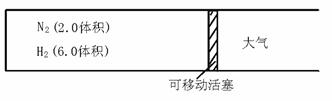
N2+3H2![]() 2NH3(正反应放热) 若反应达到平衡后,测得混合气体为7.0体积。试回答:
2NH3(正反应放热) 若反应达到平衡后,测得混合气体为7.0体积。试回答:
(1)保持上述反应温度不变,设a、b、c(a∶b=1∶3)分别代表初始加入的N2、H2和NH3的体积,如果反应达到平衡后,混合气体中各物质的体积分数仍与上述平衡完全相同。那么:
①若a=1.0,c=2.0,则b=___________。在此情况下,反应起始时将向___________方向进行(填“正”或“逆)。
②若规定起始时反应向逆方向进行,则c的范围是__________________。(用含a、b的式子表示)。
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是__________,原因是_________________。
解析:(1)题设反应是在恒温恒压下进行的,恒温恒压建立等效平衡的条件是:相同物质的投料比相等(若投料物质不一样,可依化学方程式转化后再作比较)。就本题而言,不论向原平衡体系中充入任意体积的NH3,还是充入任意体积的比例符合V(N2)∶V(H2)=2.0∶6.0=1∶3的N2和H2的混合气体,建立新平衡后,混合气体中各气体的体积分数都与原平衡体系中同种物质的体积分数相同。
先求原平衡体系中N2、H2、NH3的体积:V(N2)、V(H2)、V(NH3)
N2 + 3H2 ![]() 2NH3 ~ ΔV
2NH3 ~ ΔV
1 3 2 1+3-2
2.0-V(N2) 6.0-V(H2) V (NH3) 2.0+6.0-7.0
V(N2)=1.5,V(H2)=4.5,V(NH3)=1.0
则a=1.0,c=2.0时,b的求法为
N2 + 3H2 ![]() 2NH3
2NH3
V平 1.5 4.5 1.0
① 1.0 b 2.0
因为NH3投入的多少对等效平衡无影响,所以
![]() b=3.0
b=3.0
若求起始时,反应向逆反应方向进行的c的范围,须先求加入多少c平衡不移动,即在已充入a体积N2和b体积H2的前提下,先求c的平衡不动量。当然,这时a、b应为已知量。设平衡不移动时充入NH3的体积为x
N2 + 3H2 ![]() 2NH3
2NH3
V平 1.5 4.5 1.0
② a b x
则当
![]() 时,平衡不移动,
时,平衡不移动,
解得:x=![]() (或x=
(或x=![]() )
)
所以,当c>![]() (或c>
(或c>![]() )时;起始时反应逆向进行。
)时;起始时反应逆向进行。
答案:(1)①3.0逆 ②c>![]() (或c>
(或c>![]() ) (2)适当降温或加压 降温或加压,平衡向正反应方向移动,气体总物质的量减少
) (2)适当降温或加压 降温或加压,平衡向正反应方向移动,气体总物质的量减少
题型Ⅶ:通过建立等效平衡的中间状态,比较反应物转化率的大小以及平衡时某物质体积分数、浓度的大小
【例题】
体积相同的甲、乙两个容器中,分别充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2![]() 2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为( B )
2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为( B )
A.等于p% B.大于p% C.小于p% D.无法判断
【例题】
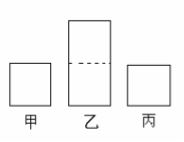
在相同温度下,有相同体积的甲、乙两容器,甲容器中充入1g N2和1g H2,乙容器中充入2g N2和2g H2。下列叙述中,正确的错误的是( )
A.化学反应速率:乙>甲 B.平衡后N2的浓度:乙>甲
C.H2的转化率:乙>甲 D.平衡混合气中H2的体积分数:乙>甲
练习:
1、在一个容积固定的密闭容器中充入1molHI,建立如下平衡:H2(g)+I2 (g)![]() 2HI(g),测得HI的转化率为a%。其他条件不变,在上述平衡体系中再充入1molHI,待平衡建立时HI的转化率为b%,则a、b的关系为 (C )
2HI(g),测得HI的转化率为a%。其他条件不变,在上述平衡体系中再充入1molHI,待平衡建立时HI的转化率为b%,则a、b的关系为 (C )
A.a>b B.a<b C.a=b D.无法确定
2、一个真空密闭恒容容器中盛有1molPCl5,加热到200℃发生如下反应:PCl5(g) ![]() PCl3 (g)+Cl2 (g),反应达到平衡时,混合气体中PCl5,所占体积分数为M%,。若同一温度的同一容器中,最初投入2 molPCl5,反应达平衡时,混合气体中PCl5,所占体积分数为N%。则M和N的关系是 ( C )
PCl3 (g)+Cl2 (g),反应达到平衡时,混合气体中PCl5,所占体积分数为M%,。若同一温度的同一容器中,最初投入2 molPCl5,反应达平衡时,混合气体中PCl5,所占体积分数为N%。则M和N的关系是 ( C )
(A) M>N (B) M=N (C) M < N (D)无法确定
3、(05年南通调研)已知甲为恒温恒压容器,乙为恒温恒容容器。两容器中均充入2mol SO2、1mol O2,初始时两容器的温度体积相同。一段时间后反应达到平衡,为使两容器中的SO2在平衡混合物的物质的量分数相同,下列措施中可行的是 (AB)
A.向甲容器中充入一定量的氦气 B.向乙容器中充入一定量的SO3气体
C.升高乙容器的温度 D.增大甲容器的压强
4、有两个密闭容器A和B,A容器内有一个移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入等量
的体积比为2:1的SO2和O2的混合气体,并使A和B的容积相等。在保持4000C的条件下使之发生如下反应:2 SO2+O2 ![]() 2SO3。
2SO3。
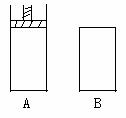
(1)达到平衡时所需要的时间A容器比B容器 ,A容器中SO2的转化率比B容器 。
(2)达到(1)所述平衡后,若向两容器中通入数量不多的等量氩气,A容器化学平衡 移动,B容器化学平衡 移动。
(3)达到(1)所述平衡后,若向两容器中通入等量的原反应气体,达到平衡时,A容器SO3物质的量分数 ;B容器中SO3的物质的量分数 。(填增大、减小、不变)
答案(1)短、大(2)逆向、不(3)不变、增大

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
...
一、公式提出的背景 19世纪末,化学家们逐渐意识到温度对化学...
假设对于反应 a A(g) + b B(g) g G(g) + h H(g) 中各物质均为理想气体,...
例:某温度、起始压强为100 kPa下,若将2mol SO 2 和1molO 2 ,通入恒...
...
什么是活化能、能垒? 1 、能垒 活化分子含有的能参加化学反应...