
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑j] 盐类水解反应的离子方程式书写 作者:刘玉林 来源:未知 日期:2012-05-16 15:11:42 点击:17428 所属专题:盐类水解方程式
[注解与辨疑j] 盐类水解反应的离子方程式书写 作者:刘玉林 来源:未知 日期:2012-05-16 15:11:42 点击:17428 所属专题:盐类水解方程式
正确书写盐类水解反应的离子方程式之一 书写盐类水解的反应的离子方程式的关键是写出弱酸根阴离子或不活泼金属阳离子(包括铵离子)与水反应生成相应弱酸或弱碱的反应式.书写盐类水解反应的离子方程式应注意以下几点: (1)写盐类水解的离子方程式时,应遵循书写离子方程...
 [注解与辨疑j] 盐类的水解反应进行的程度 作者:刘明 来源:未知 日期:2016-02-02 20:16:49 点击:8402 所属专题:盐类水解规律
[注解与辨疑j] 盐类的水解反应进行的程度 作者:刘明 来源:未知 日期:2016-02-02 20:16:49 点击:8402 所属专题:盐类水解规律
酸碱中和和盐类水解在一定条件下互为可逆,构成矛盾的两个方面,这对矛盾有时这方面成为主要方面,有时候另一方面成为矛盾的主要方面.如何正确理解中和反应和盐类的水解反应的进行程度问题?现分以下几类情况来谈. (1)盐类的水解进行的程度很小:由于中和反应有极弱...
 [注解与辨疑j] 由于双水解在溶液中不能大量共存的离子组总结 作者:张澳 来源:未知 日期:2016-02-02 20:17:51 点击:7753 所属专题:双水解反应 离子共存
[注解与辨疑j] 由于双水解在溶液中不能大量共存的离子组总结 作者:张澳 来源:未知 日期:2016-02-02 20:17:51 点击:7753 所属专题:双水解反应 离子共存
弱酸根离子与弱碱阳离子在水溶液中 不能 大量 共存 的情况常见的有:...
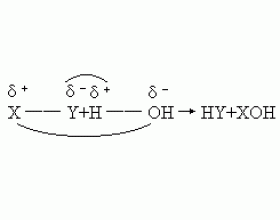 [有机化学] 水解反应面面观 作者:周广 来源:未知 日期:2016-01-08 22:24:24 点击:11671 所属专题:水解反应 有机反应
[有机化学] 水解反应面面观 作者:周广 来源:未知 日期:2016-01-08 22:24:24 点击:11671 所属专题:水解反应 有机反应
所谓水解反应,即物质跟水发生的相互变换成分的反应.用通式可表示为: 反应的机理可简单地认为是:共价键(X—Y键、H—O键)断裂(一般地,一个水分于中只有一个H—O键断裂),再按异电相吸原则,重新组合成新键即得产物.至于离子键则视为共价键的极限情形.各类水解...
 [注解与辨疑j] 酸式盐水溶液的酸碱性概括小结 作者:徐志宏 来源:未知 日期:2012-05-16 09:43:40 点击:8034 所属专题:酸式盐 酸碱性判断
[注解与辨疑j] 酸式盐水溶液的酸碱性概括小结 作者:徐志宏 来源:未知 日期:2012-05-16 09:43:40 点击:8034 所属专题:酸式盐 酸碱性判断
(1)强碱强酸酸式盐 由于在水溶液中只能进一步电离出H + ,不会发生水解,所以只具备酸性,可代替一元强酸使用,如: NaHSO 4 +NaHCO 3 =Na 2 SO 4 +H 2 O+CO 2 ↑ NaHSO 4 +NaCl Na 2 SO 4 +HCl↑ (2)强碱弱酸酸式盐 由于强碱弱酸酸式盐中含有弱酸酸式根,既可以进一步...
 [注解与辨疑j] FeCl3溶液与Na2S溶液反应生成什么? 作者:张劲辉 来源:未知 日期:2012-05-16 09:22:31 点击:9690 所属专题:氯化铁 双水解反应
[注解与辨疑j] FeCl3溶液与Na2S溶液反应生成什么? 作者:张劲辉 来源:未知 日期:2012-05-16 09:22:31 点击:9690 所属专题:氯化铁 双水解反应
问:“在FeCl 3 溶液中加入Na 2 S溶液发生的反应有两种说法,一是: 2Fe 3+ +S 2- =2Fe 2+ +S↓; 又一为: 2Fe 3+ +3S 2- +6H 2 O=2Fe(OH) 3 ↓+3H 2 S↑ 这两种说法哪个正确? 答:一般说来,Fe 3+ 具有较强的氧化性,而S 2- 则具有还原性,因此当Fe 3+ 与S 2- 相遇时,Fe...
 [注解与辨疑j] 影响电离度的因素 作者:吴传鹏 来源:未知 日期:2012-05-16 09:19:41 点击:12162 所属专题:电离度 电离平衡
[注解与辨疑j] 影响电离度的因素 作者:吴传鹏 来源:未知 日期:2012-05-16 09:19:41 点击:12162 所属专题:电离度 电离平衡
①电解质的结构 具有离子键或强极性的分子在水溶液中的电离度均很大,几乎是100%。弱极性或非极性分子在水中呈微弱电离甚至不电离。电解质中键的极性越大,其电离度也越大。离子化合物的电离度取决于离子电荷及离子半径。离子电荷越高,半径越小,则其电离度越...
 [注解与辨疑j] 电离常数和电离度有什么关系? 作者:羊绍敬 来源:未知 日期:2012-05-16 08:41:29 点击:40708 所属专题:电离平衡常数 电离度
[注解与辨疑j] 电离常数和电离度有什么关系? 作者:羊绍敬 来源:未知 日期:2012-05-16 08:41:29 点击:40708 所属专题:电离平衡常数 电离度
(1)弱电解质的电离是一种可逆过程。以醋酸的电离为例,醋酸溶于水后,它的分子即电离为H+离子和CH 3 COO - 离子,这是正过程,同时逆过程是H + 离子和CH 3 COO - 离子重新结合成醋酸分子。 CH 3 COOH H + +CH 3 COO - 在这个过程中,CH 3 COOH分子电离的速率(正反应的速率)...
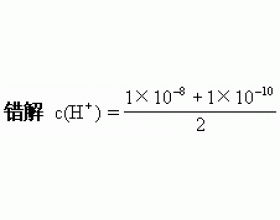 [注解与辨疑j] pH拾零 作者:潘祥泰 来源:未知 日期:2016-02-02 19:49:52 点击:9049 所属专题:ph值 ph计算
[注解与辨疑j] pH拾零 作者:潘祥泰 来源:未知 日期:2016-02-02 19:49:52 点击:9049 所属专题:ph值 ph计算
一、pH与酸碱性 1.溶液酸碱性的强弱由pH决定,与温度、溶质无关。如:pH均为2的硫酸溶液与醋酸溶液酸度相同。 2.pH等于7的溶液不一定呈中性。(“pH=7为中性”习惯上指常温时) 二、 pH的计算 1.计算时先确定溶液的酸碱性,计算顺序为:酸性→c(H + )→pH;碱性→c(O...
 [注解与辨疑j] 为什么要引入“pH” 作者:罗翊轩 来源:未知 日期:2016-03-09 21:47:08 点击:3168 所属专题:ph值
[注解与辨疑j] 为什么要引入“pH” 作者:罗翊轩 来源:未知 日期:2016-03-09 21:47:08 点击:3168 所属专题:ph值
溶液的酸碱度,可用[H + ]或[OH - ]表示。但我们常碰到的某些溶液的酸度或碱度很...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
什么是“软硬酸碱理论”,1963 年,拉尔夫・皮尔逊提出软硬酸...
水溶液中NH水解显酸性,CO、HCO水解显碱性,二者会发生“相互促...
在基础化学中,我们常被告知:盐类水解通常是微弱且可逆的。...
一般来说,溶解度大的物质易转化为溶解度小的物质。那反过来...
一.定义 1.pH pH=–log[H] pH是衡量溶液整体酸碱度的指标,具体指溶...
溶解度(Solubility)与溶度积常数(Solubility Product Constant, ksp密切...
【导读】与第一电离能定义相反(并非严格互逆过程),第一电子...
【导读】 根据 质子酸碱 理论: 酸是 质子的给予体 , 给出质子...