
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
1.判断元素的种类
一般情况下,电负性大于1.8,为非金属元素,电负性小于1.8,为金属元素。
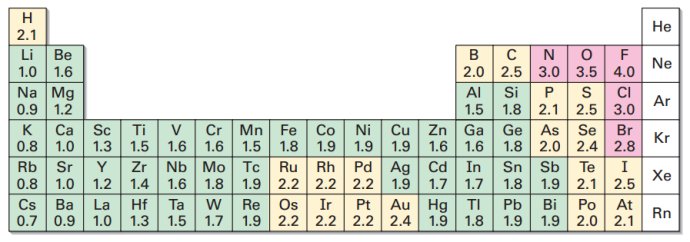
2.判断化学键类型
一般情况下,两元素电负性差值大于1.7时,形成离子键,两元素电负性差值小于1.7时,形成共价键。
例如:Na电负性0.9,Cl电负性3.0,二者之间的差值为2.1大于1.7,形成离子键。
H电负性2.1,Cl电负性3.0,二者之间的差值为0.9小于1.7,形成共价键。
3.判断元素价态的正负
化合物中电负性大的元素为负价,电负性小的元素为正价。
例如:Na电负性0.9,Cl电负性3.0,形成NaCl,钠离子为正一价,氯离子为负一价
4.判断金属性、非金属性强弱
电负性越大,其非金属性越强,电负性越小,其金属性越强。
例题:电负性的大小也可以作为判断金属性和非金属性强弱的尺度,下列关于电负性的变化规律正确的是(
A.周期表中同周期元素从左到右,元素的电负性逐渐增大
B.周期表中同主族元素从上到下,元素的电负性逐渐增大
C.电负性越大,金属性越强
D.电负性越小,非金属性越强
解析:非金属性越强,电负性越大。同周期自左向右,非金属性逐渐增强,电负性逐渐增强;同主族自上而下,非金属性逐渐较弱,电负性逐渐降低,所以正确的答案选A。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、为啥杂化轨道s成分越大,电负性越强? 电负性不是固定不...
一、人教版 二、鲁科版 三、苏教版 四、沪科版 五、练习 (该...
电负性是描述元素原子在化合物中吸引键合电子能力的标度,是...
1.对角线规则 对比周期系中元素性质,发现: 左上~右下,对角线元...
一、为何氮不像磷,氧不像硫? 在元素周期表中,同族元素自上...
...