
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑i] 催化剂中毒和催化剂活性降低 作者:化学自习室 来源:未知 日期:2025-12-11 11:00:05 点击:416 所属专题:催化剂中毒
[注解与辨疑i] 催化剂中毒和催化剂活性降低 作者:化学自习室 来源:未知 日期:2025-12-11 11:00:05 点击:416 所属专题:催化剂中毒
一、 催化剂中毒 催化剂中毒是指微量或少量的外来物质(毒物)与催化剂的活性中心发生强烈的化学作用,导致活性中心被永久或半永久地占据、堵塞或改变,从而急剧降低或完全丧失催化剂活性的现象。 核心原理:毒物与活性中心的结合力远强于反应物,从而“霸占”了位置,使反...
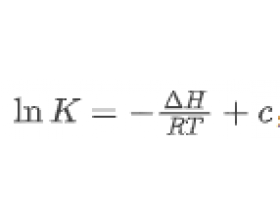 [注解与辨疑i] 范特霍夫方程:从理论解析到工业实践 作者:化学自习室 来源:未知 日期:2025-12-01 16:31:39 点击:469 所属专题:范特霍夫方程
[注解与辨疑i] 范特霍夫方程:从理论解析到工业实践 作者:化学自习室 来源:未知 日期:2025-12-01 16:31:39 点击:469 所属专题:范特霍夫方程
在化学热力学与工业生产的交叉领域,范特霍夫方程将平衡常数与温度的抽象关系转化为可量化、可应用的实用工具。它不仅是理解化学平衡移动规律的核心理论,更是工业生产中优化工艺参数的科学依据,同时也是高考化学考查学生综合应用能力的高频考点。 范特霍夫方程的理论...
 [注解与辨疑i] 一文搞懂什么是“吸附”和“脱附”? 作者:化学自习室 来源:未知 日期:2025-11-21 17:12:14 点击:360 所属专题:催化剂原理及应用
[注解与辨疑i] 一文搞懂什么是“吸附”和“脱附”? 作者:化学自习室 来源:未知 日期:2025-11-21 17:12:14 点击:360 所属专题:催化剂原理及应用
这些生活场景,全是 “吸附” 在干活! 打开冰箱闻到异味,放一包除味剂就好 —— 它靠什么 “吃掉” 臭味? 沙漠里的集水装置,能从干燥空气中 “抓” 出水来 —— 这又是什么操作? 其实答案都是同一个:吸附。而当除味剂失效、集水装置释放水时,另一股力量在发力 —...
 [注解与辨疑i] 加压和加水(稀释)的逻辑相同 作者:化学自习室 来源:未知 日期:2025-11-14 18:45:53 点击:194 所属专题:等效法
[注解与辨疑i] 加压和加水(稀释)的逻辑相同 作者:化学自习室 来源:未知 日期:2025-11-14 18:45:53 点击:194 所属专题:等效法
在化学平衡的学习中,压强对气体平衡的影响与水溶液中“越稀越电离、越稀越水解”的规律,看似是不同场景的知识点,实则有着相同的核心逻辑。这背后,是 速率方程 与浓度变化的精妙关联,让我们一同一探究竟。 简言之,加压和加水(稀释),都是通过改变浓度,利用正逆...
 [注解与辨疑i] 基元反应与反应速率方程:化学动力学的核心关联 作者:化学自习室 来源:未知 日期:2025-11-07 10:05:40 点击:368 所属专题:基元反应 速率方程
[注解与辨疑i] 基元反应与反应速率方程:化学动力学的核心关联 作者:化学自习室 来源:未知 日期:2025-11-07 10:05:40 点击:368 所属专题:基元反应 速率方程
在化学动力学研究中,基元反应是理解反应机理的 “最小单元”,而反应速率方程则是描述反应速率与反应物浓度关系的 “数学语言”。二者紧密关联 —— 基元反应的速率方程可直接由反应本身推导,而非基元反应的速率方程需通过实验测定并结合基元反应步骤(反应机理)解释。深入...
 [注解与辨疑i] 多重平衡中的平衡浓度要代哪个数值? 作者:化学自习室 来源:未知 日期:2025-11-07 09:55:58 点击:145 所属专题:多重平衡
[注解与辨疑i] 多重平衡中的平衡浓度要代哪个数值? 作者:化学自习室 来源:未知 日期:2025-11-07 09:55:58 点击:145 所属专题:多重平衡
在多重平衡体系中,各物质在达到平衡状态时的浓度。多重平衡体系是指一个化学反应体系中存在多个相互关联的化学反应,且至少有一种物质同时参与几个相互关联的平衡。 核心原则:在同一个体系中,同一个物质,无论它参与了多少个平衡反应,它在平衡时的浓度只有一个确定...
 [注解与辨疑i] 什么是催化剂吸附机理? 作者:化学自习室 来源:未知 日期:2025-10-29 10:14:15 点击:256 所属专题:催化剂原理及应用
[注解与辨疑i] 什么是催化剂吸附机理? 作者:化学自习室 来源:未知 日期:2025-10-29 10:14:15 点击:256 所属专题:催化剂原理及应用
催化反应的核心始于吸附机理——分子通过物理吸附(范德华力)或化学吸附(化学键重组)“锚定”在催化剂表面,直接决定反应物的富集、活化与选择性。DFT计算作为原子尺度的“虚拟显微镜”,从四维度解析吸附本质。 结构优化揭示分子构型变化(如甲醇在金表面C-O键拉伸);...
 [注解与辨疑i] 究竟有几个基元反应? 作者:化学自习室 来源:未知 日期:2025-10-29 10:12:23 点击:321 所属专题:基元反应
[注解与辨疑i] 究竟有几个基元反应? 作者:化学自习室 来源:未知 日期:2025-10-29 10:12:23 点击:321 所属专题:基元反应
武汉市九月调考试题 解析 一般来说,有几个 过渡态就有几个基元反应。 那么吸附或脱附过程是否属于基元反应呢? 山东胡老师分析认为 物理吸附脱附的每个基元步骤是不能视为 “基元反应”的但可以称作“基元物理过程”,化学吸附脱附的每个基元步骤则可以视为“基元反应...
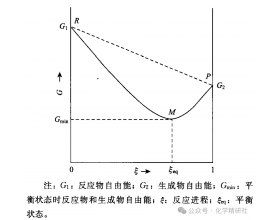 [注解与辨疑i] 可逆反应的自发性能否用吉布斯自由能变(ΔG)判断 作者:化学自习室 来源:未知 日期:2025-10-16 09:59:58 点击:421 所属专题:吉布斯自由能
[注解与辨疑i] 可逆反应的自发性能否用吉布斯自由能变(ΔG)判断 作者:化学自习室 来源:未知 日期:2025-10-16 09:59:58 点击:421 所属专题:吉布斯自由能
在化学热力学中,吉布斯自由能变(ΔG)是判断反应自发性的核心判据,其核心规律 “ΔG0 时反应自发,ΔG0 时反应非自发,ΔG=0 时反应达平衡” 已成为判断不可逆反应自发性的经典依据。然而,可逆反应 “同一条件下正、逆反应可同时进行” 的特性,常使学习者产生困惑...
 [注解与辨疑i] 工业合成氨反应条件的调控 作者:化学自习室 来源:未知 日期:2025-09-28 11:18:19 点击:706 所属专题:合成氨 工业条件选择
[注解与辨疑i] 工业合成氨反应条件的调控 作者:化学自习室 来源:未知 日期:2025-09-28 11:18:19 点击:706 所属专题:合成氨 工业条件选择
核心思想: 多、快、好、省, 四大关键条件的分析与调控 1. 温度 (Temperature) · 热力学(平衡)角度: 反应放热,根据 勒夏特列原理 ,降低温度有利于反应向生成氨的正方向移动,提高平衡转化率。 · 动力学角度: 降低温度会显著降低反应速率,导致达到平衡所需的时间非...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
在化学反应中,驱动力指的是推动反应进行的内在因素,它决定...
一.核心概念辨析 中间体:寿命长于分子振动的瞬态物种,多步...
活化分子百分数和活化分子数,理解它对掌握化学反应速率至关...
化学反应的焓变越大,代表这个反应受温度变化的影响越大吗?...
在化学热力学和分析化学中,我们常常听到这样的说法:“如果...
...
一、 什么是活化能? 活化能,通常用符号Ea表示,其标准单位为...
一、基本定义 (一)中间体 1、根据国际纯粹与应用化学联合会...