
|
学习小专题 |
 化学反应的焓变越大,代表这个反应受温度变化的影响越大吗?
日期:2026-01-14 16:00:09
点击:221
好评:0
化学反应的焓变越大,代表这个反应受温度变化的影响越大吗?
日期:2026-01-14 16:00:09
点击:221
好评:0
化学反应的焓变越大,代表这个反应受温度变化的影响越大吗? 反应受温度影响的核心是「焓变与熵变的综合作用」,而非焓变单独决定 结论: 反应受温度变化的影响大小,是焓变、熵变(影响反应自发性 / 平衡)和活化能(影响反应速率) 共同决定的,不能单独用焓变大小判...
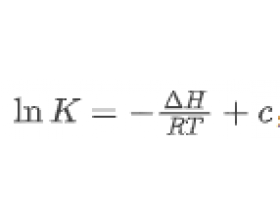 范特霍夫方程:从理论解析到工业实践
日期:2025-12-01 16:31:39
点击:407
好评:0
范特霍夫方程:从理论解析到工业实践
日期:2025-12-01 16:31:39
点击:407
好评:0
在化学热力学与工业生产的交叉领域,范特霍夫方程将平衡常数与温度的抽象关系转化为可量化、可应用的实用工具。它不仅是理解化学平衡移动规律的核心理论,更是工业生产中优化工艺参数的科学依据,同时也是高考化学考查学生综合应用能力的高频考点。 范特霍夫方程的理论...
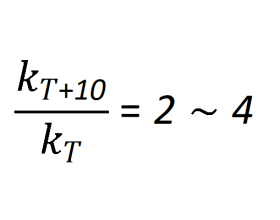 范特霍夫方程在高考中的应用
日期:2025-10-26 17:48:57
点击:372
好评:0
范特霍夫方程在高考中的应用
日期:2025-10-26 17:48:57
点击:372
好评:0
前言:范特霍夫方程是荷兰化学家雅各布斯·亨里克斯·范托夫(VantHoff equation)于1884年提出的。用于描述温度对化学反应平衡常数的影响。该方程可用来计算化学反应在不同温度下的平衡常数,从而预测化学反应的热力学行为。 范特霍夫方程在高考中虽不作为核心考点考查,...
 范特霍夫方程与阿伦尼乌斯公式在高中化学的作用
日期:2025-08-07 08:19:54
点击:634
好评:0
范特霍夫方程与阿伦尼乌斯公式在高中化学的作用
日期:2025-08-07 08:19:54
点击:634
好评:0
一、范特霍夫方程:化学反应的“平衡指挥家” 在可逆反应里,化学平衡常数(K)能衡量反应进行的程度。K越大,意味着反应正向进行得越彻底。范特霍夫方程就揭示了K和温度(T)之间的关系,它的核心就是:平衡常数随温度的变化,取决于反应是吸热还是放热。 二、阿伦尼乌...
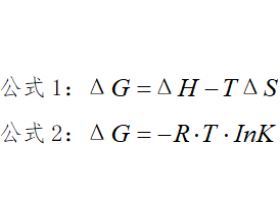 范特霍夫方程在高中化学中有三个应用
日期:2025-08-07 08:06:56
点击:941
好评:0
范特霍夫方程在高中化学中有三个应用
日期:2025-08-07 08:06:56
点击:941
好评:0
公式推导 一、公式推导 公式1是大家都熟悉的吉普斯自由能公式,用来判断反应能否自发进行以及自发进行的温度。 公式2(常常出现在题目的已知信息中)相同温度下,K越大,ΔG越小,反应的趋势越大,反应越完全。 ΔG:吉普斯自由能 R: 摩尔气体常量,8.314J/(mol·K) K: ...
 高考题中有关范特霍夫方程的考查
日期:2025-08-07 07:57:43
点击:320
好评:0
高考题中有关范特霍夫方程的考查
日期:2025-08-07 07:57:43
点击:320
好评:0
...
 化学反应平衡常数K值与温度是什么关系?
日期:2025-08-07 07:47:26
点击:2898
好评:0
化学反应平衡常数K值与温度是什么关系?
日期:2025-08-07 07:47:26
点击:2898
好评:0
【导读】范特霍夫方程很好的描述了可逆反应的化学平衡常数(K)与温度(T)的关系,其核心规律:平衡常数随温度的变化取决于反应的热效应(Δ H )。 ①吸热反应(Δ H >0): K随温度升高而增大; ②放热反应(Δ H <0): K随温度升高而减...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。