
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
在“原电池”概念的教学中,学生经常会问到一些有关干电池的实际问题,笔者在此列举几个并加以粗浅地解释。
1、干电池的电动势是怎样产生的
如图所示为常见的干电池示意图
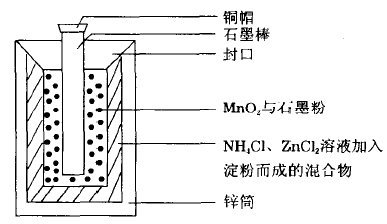
其中正极为MnO2、石墨粉的混合物及中央的石墨棒,负极为锌筒且兼作容器,电解质溶液为NH4Cl、ZnCl2溶液,加入淀粉成糊状使电解液不能流出来所以叫做干电池。
正、负极都与NH4Cl、ZnCl2溶液相接触,在外电路接通前:
负极:因为Zn在金属晶体中所具有的能量比它在溶液中成为水合离子的能量高,由于能量越低越稳定,那Zn2+就会进入溶液而把电子留在锌筒上,从而使溶液带正电而锌筒带负电。Zn2+进入溶液后由于受锌极上电子吸引便聚集在锌筒附近,因而使锌筒和溶液之间产生了从溶液指向锌筒的电场,这个电场将阻碍z继续由锌筒进入溶液,当溶液和锌极之间的电场力与化学力平衡时,锌停止溶解,此时负极电势低于溶液,生成的Zn2+在溶液中发生水解:
Zn2++2H2O=Zn(OH)2+2H+及一系列反应:Zn(OH)2=ZnO+H2O,ZnO+2NH4Cl=Zn(NH3)2Cl2+H20
溶液中的H+由于受Zn2+排斥所以不容易直接从锌极上得电子,这也就解释了化学课上原电池溶液中的H+不能就近在锌极上得电子而非得要舍近求远跑到铜极上得电子的疑问。
正极:溶液中H受Zn2+排斥而驰向正极,因为石墨是良好的导体,所以H可将石墨中自由电子吸出而使石墨带正电,带正电的石墨将吸引溶液中负离子而形成从石墨指向溶液的电场,这个电场将阻碍H继续驰向正极,最后达到平衡状态H停止移动,此时正极电势高于溶液电势,溶液中各点电势都相等,而负极电势低于溶液,则正、负极之间就产生了电势差,这个电势差就是干电池的电动势。
2、正极材料中MnO2,有什么作用
如果接通外电路,由于正、负极之间有电势差则负极上多余的电子将经导线流向正极,从而使锌与溶液之间原来电场减弱则锌又开始溶解,Zn2+又开始由锌进入溶液。同理,正极得到电子也会使正极与溶液之间的电场减弱则H+继续驰向正极。
H在正极得到电子:2H++2e-=H2
生成的H2附着于正极上,从而使正极逐渐被H覆盖而与溶液隔绝,这将增加电池内阻,叫做极化内阻。而加入MnO2就可以有效避免,这是因为H+与MnO2,可以发生以下反应:2MnO2+2H++2E=2MnOOH(水锰石),所以MnO2,叫做“退极化剂”。
3、为何连续放电时间久了,内阻会增大电动势会减小
电池内阻等于电池内部欧姆电阻与极化电阻之和,随着放电进行,产生的Zn(OH)2、Zn(NH3)2Cl2、MnOOH等为难溶物不导电则增加了欧姆电阻。
化学电动势的大小决定于金属的性质F容易产生离子及失去电子的性质)以及电解液的浓度,由于溶液中NH4Cl被消耗生成Zn(NH3)2Cl2而使其浓度降低,锌负极电势因Cl一浓度下降而向正方向移动,正极电势因MnOOH积累而下降,所以两极间电势差即电动势要减小。
4、为何能间歇放电
干电池间歇工作电压可以恢复,要比连续放电好,这是普通干电池的一大特性,这主要与MnO2这种电极材料有关,MnO2是半导体,导电性能不良为粉状电极,电极反应在MnO2颗粒表面进行,MnO2晶格是由Mn与O交错排列而成,H+必须进入晶格内才能发生反应,随着放电进行,在MnO2表面来不及进入晶格的H+对以后到来的H+产生阻碍作用,影响反应速率,使极化内阻变大,导致电压下降,而在间歇时间内MnO2颗粒表面的H有充足的时间向晶格内部扩散,使表面和内部的H+浓度趋于均匀,从而减少了极化内阻使电压回升。
5、市面上干电池有碳性、碱性之分。这是怎么回事
上面所分析的干电池就是碳性电池,这种电池使用过程中电压不断下降不能提供稳定电压,且放电电流小。后来人们发现当电解质溶液用KOH溶液代替时(正负极材料不变)电池的各项性能都得到显著提高,这种电池就是碱性电池,由于碱性电池容量大,能大电流放电,各方面特性均优于碳性电池,自然价格也较贵一些。
6、废旧干电池里究竟是什么东西污染环境
无论碳性还是碱性干电池都存在自放电,主要是锌负极自放电,自白消耗了活性物质,缩短了电池的使用寿命,所以干电池都有“有效期”。引起锌负极自放电原因主要是电池内部形成腐蚀微电池,我们知道溶液中的H+由于受Zn2+排斥不容易直接从锌极上得电子,但仍有少量的H被Zn置换成H2,为了抑制锌的腐蚀,可在电解液中加入微量HgCl2,因为Hg2+比H+更易得电子,所Hg2+被置换,在锌表面生成一薄层叫做锌汞齐,因而可以抑制锌的腐蚀。废旧干电池的危害主要就来源于这些微量的汞,汞是严重污染环境的元素,有明显的神经毒性,对内分泌系统、免疫系统等都有严重影响,上世纪五十年代发生在日本的震惊中外的水俣病就是由于汞污染造成的,所以我国规定凡进入国内市场的国内外电池均须标注汞含量(如注明“低汞”或“无汞”)。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
化学能是内能中与化学键相关的一部分;而焓是一个包含内能,...
加热一般是指使用酒精灯提供的热量使反应持续进行; 高温是指...
先说说放热反应和吸热反应。有同学错误地认为: “ 吸热反应...
先说说放热反应和吸热反应。有同学错误地认为: “ 吸热反应...
化学平衡理论是中学化学最重要的基础理论之一,是研究可逆反...
1 . KClO 3 分解制 O 2 ,为什么加入一些 MnO 2 ? 因为 MnO 2 对 KC...