
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
炔烃是含有叁键的不饱和烃,它们比相同碳类的烯烃少两个 氢,比烷烃少四个氢。因此它们的通式是CnH2n-2。在炔烃系列中 最简单也是最重要的成员是乙炔(C2H2)。炔烃的结构特征就是在 分子中有两个相邻的碳原子以叁键相连接起来。炔烃的同分异构 现象和烯烃相似。
第一节:乙炔的结构
根据化学键的电子概念,组成叁键的碳原子的外层电子,由 2s22p2跃迀为2s12p3后,由一个S轨道和一个P轨道进行杂化(sp杂化),形成两个等同的杂化轨道,两个杂化轨道分布在一条直线 上,另外的两个P轨道保持原样并分别垂直于杂化轨道,相当于空间直角坐标的关系。
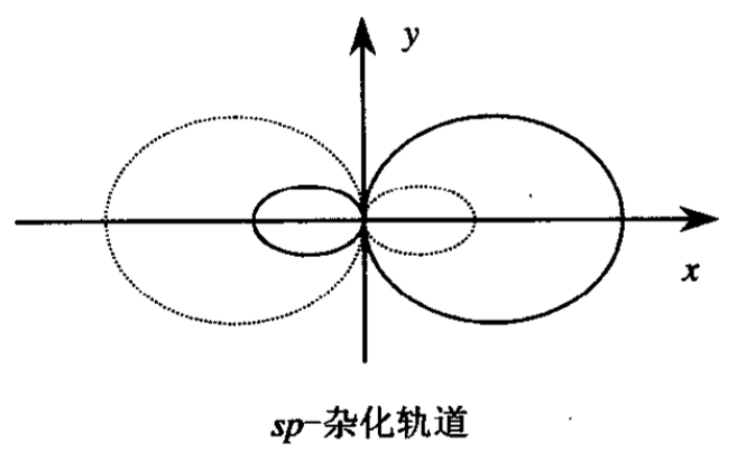
杂化后的两个碳原子各提供一个杂化轨道形成σ键,其余的杂化轨道与氢结合,所以乙炔分子中的两个碳原子和两个氢原子 都处在一条直线上。这时,两个碳原子上的四个P轨道处于两两平行的状态,进行平行交盖,组成两个π键。
总之,在乙炔分子中,两个碳原子以三对电子对组成叁键, 其中一对杂化价电子组成σ键,两对P电子组成两个π键。
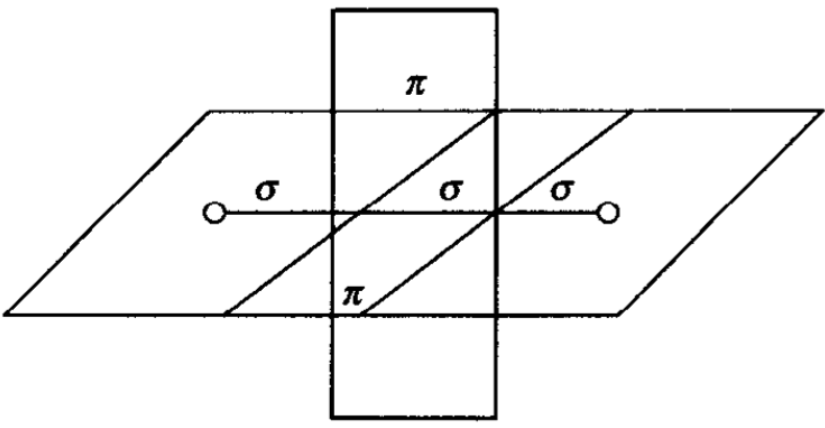
在乙炔分子中两个碳原子之间的距离比在乙烯分子中两个碳 原子之间的距离要近些,叁键的键长为0.12nm,但是叁键的键能 并不等于单键的三倍。乙炔分子中叁键的键能为835.7kJ/mol,比 三倍的单键的键能(345.8kJ/mol)要小得多,比双键键能略大些 (610.4kJ/mol)。这说明键和键是不能同等看待的。
第二节:乙炔的来源
煤气和石油裂解气中含有少量乙炔,但不作为生产乙炔的来 源。工业上大量制备乙炔的方法有两种,即电石水解法和烷烃热 解法。
一、电石水解法
碳化钙(电石)与水作用产生乙炔和氢氧化钙:
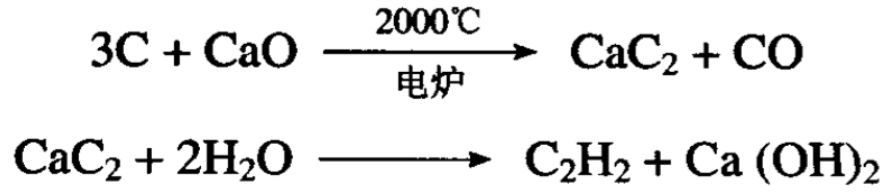
这个方法需要大量电能,适合于电力供应方便的地方,目前 乙炔生产中电石水解法在我国仍占主要地位。,
二、烷烃热解法
另一种方法是使天然气热解。甲烷短时间内加热到高温 (1400~1600°C)后立即冷却,可得产量相当高的乙块。
![]()
这是一个有发展前途的乙炔工业制法。
油田或炼厂气的石油气中含有甲烷以外的其他C2〜C4烷烃, 这些高碳烃在高温下短时间受热也能生成乙炔,在产物中除乙炔 外也有乙烯等,需要分离才能得到纯乙块。
第三节:乙炔的物理性质
纯的乙炔为无色气体,由电石制得的乙炔由于含有磷化氢、 硫化氢等杂质而有臭味,对人体有害。乙炔的沸点为-83.4°C。由 于乙炔在高压下容易爆炸,所以乙炔很少压缩在钢瓶中储藏。
乙块微溶于水,而易溶于丙酮。在通常情况下,1体积丙酮能 溶解25体积的乙炔,在12个大气压下能溶解300倍体积的乙炔。 用浸有丙酮的石棉来吸收乙炔,储藏在压缩钢瓶中就比较安全了。
第四节:乙炔的化学性质
炔烃加成能放氢
加氢催化变烯烃
高温催化氢被换
产物变成卤烯烃
水合反应炔变醛
高温环化成芳烃
加卤炔氢被取代
反应产物卤烯烷
锰盆氧化炔分解
醋酸高温炔变酯
氯盐铵盐炔聚合
一、炔烃加成能放氢,加氢催化变烯烃,高温催化氢 被换,产物变成卤烯烃
乙炔和乙烯一样,能与很多试剂进行加成反应。反应分两步进行,先加上一分子试剂生成含双键的化合物,然后再加第二分子试剂生成烷烃的衍生物。第一步反应的速度比第二步快得多, 因此控制反应条件,可以使反应基本上停留在第一步。
(1)加氢。
在适当催化剂存在下(钯和铂等),乙炔可以加 一分子氢而得乙稀:
![]()
(2)加卤化氢。
乙炔在氯化汞的催化下,可与一分子氯化氢加成得氯乙烯,这是工业上制氯乙烯的方法。通常是用载在活性炭上的氯化汞作催化剂,在常压下等物质的量的乙炔和氯化氢通 过170~200℃加热的催化剂,即能得到氯乙烯:
![]()
二、水合反应炔变醛
一般情况下,乙炔与水不发生化学作用,当有汞盐存在时, 乙炔与硫酸的水溶液作用,生成乙醛。
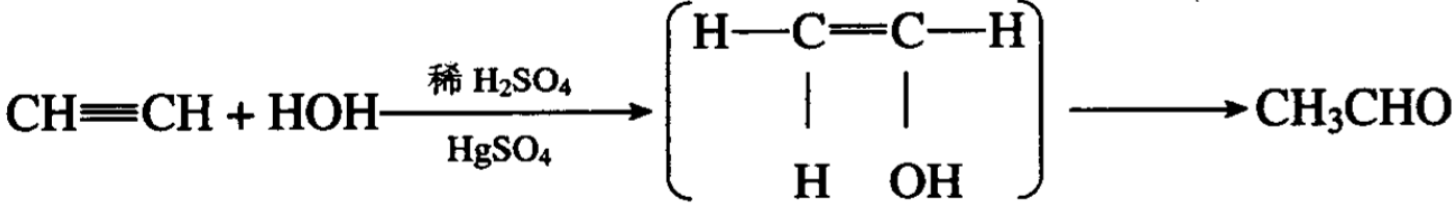
在反应中间过程中先是生成乙烯醇,但是乙烯醇是不稳定的, 立即发生分子的内部变化,即一个羟基上的氢较移到不饱和碳上 去,最后在水溶液中获得乙醛。
三、高温环化成芳烃
将乙炔通过赤热的铁管子(500°C)时,发生三聚生成少量苯, 如果把乙炔通过热到600~650°C的活性炭,可以得到更多的苯。

四、加卤炔氢被取代,反应产物卤烯烷
氯和溴容易与炔烃发生加成反应。在光或催化剂的影响下, 氯与乙炔发生剧烈的反应,甚至能引起爆炸,生成氯化氢和碳。 如果用氮气使气体稀释,或用氯仿作溶剂,最终反应按下列方式 进行:
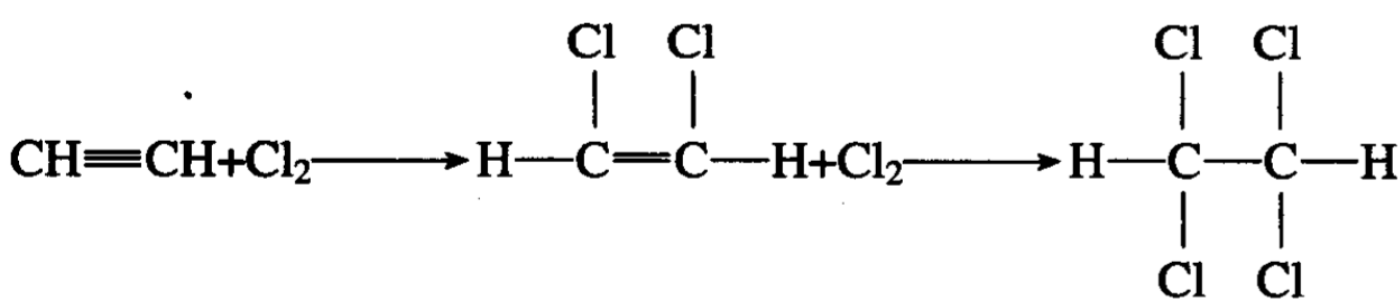
碘与乙炔加成只得到1,2-二碘乙烯。
五、锰盐氧化炔分解
炔烃由于是一种不饱和烃,所以和烯烃的性质相似,许多氧化剂也可与炔烃发生反应。如高锰酸钾的水溶液就能氧化炔烃,而本身的紫红色褪去,这个反应也可作为炔烃的鉴定反应。
![]()
六、醋酸高温炔变醋
乙炔和醋酸也需要在催化剂影响下才能发生加成。醋酸和乙 炔在气相,170~190°C,载在活性炭上的醋酸锌催化剂作用下加成 得醋酸乙烯酯。
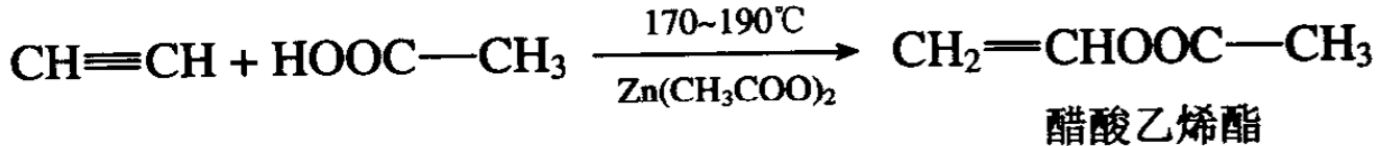
所得醋酸乙烯酯容易发生聚合,这是制造“维尼纶”等的 原料。
七、氯盐铵盐炔聚合
乙炔能发生聚合反应,在不同条件下,可以得到不同的产物。 例如在氯化亚铜及氯化铵的强酸性溶液中,两个乙炔分子聚合成 乙烯基乙炔。
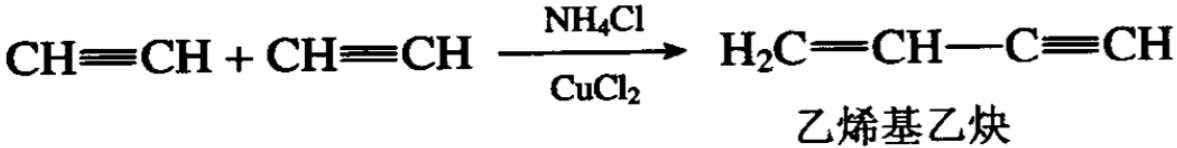

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
在高考中考查: 近几年新高考中最早出现非苯环芳香烃相关考查...
立体结构差异 椅式环己烷结构中,碳原子构成的环近似于一个三...
电子效应,在大多数反应中,由于取代基(与氢原子相比)倾向...
一、芳香烃的定义 具有芳香性的烃称为芳香烃,一般是指分子中...
一、一些特殊反应 1、醇解反应: 卤代烃与醇钠的醇溶液反应,...
烷的取代反应主要是自由基反应。比如: Cl 2 →2Cl· CH 4 →CH 3...