
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
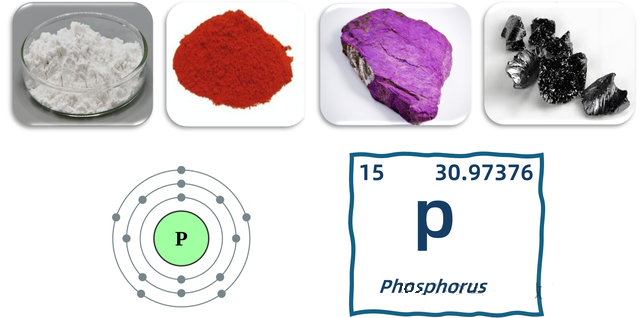
今天咱们来聊一个我们每天都会接触到的奇异元素:磷。它像被施了魔法的变形怪一样,以截然不同的四个面貌出现在人类面前。——白磷、红磷、紫磷、黑磷。没错,它们都是纯粹的磷单质,所以它们的化学式也是一样的。但是由于它们的原子排列结构不同,它们四个的化学和物理性质却截然不同。磷这个元素可以说是自然界的变脸大师,这就导致了人们对于它的认识和理解也在不断变化,前后一共经历了300年:从炼金术士,到工业革命,再到现在的能源革命,磷,都扮演着重要角色。
百年发现史
白磷,炼金术的“冷火与魔鬼”
亨尼格·布兰德是一个破产的商人,也是一个狂热的业余炼金术士。当时的医学和炼金理论认为,人体内蕴含着某种神圣的本质。那么如何从人体排泄物中提炼出能将贱金属转化为黄金的“贤者之石”呢?布兰德注意到人类的尿液是金黄色的,他极其天真地推测:尿液中或许隐藏着黄金的种子。
1669年,布兰德收集了大约五十桶人类尿液(据传主要来自士兵),将其放在地窖里腐烂发酵,然后开始没日没夜地熬煮。当水分蒸发殆尽,尿液变成一种黑色的粘稠浓缩物时,他用极高的温度在沙炉中对这种渣滓进行干馏。很遗憾,布兰德没有看到黄金,但他看到冷凝管的末端滴下了一种如同蜡状的白色固体。当地下室陷入黑暗时,这种物质竟然在没有任何热量的情况下,散发出幽幽的淡蓝绿色荧光。

布兰德将其命名为“冷火”。他无意中成为了历史上有记录而来的第一个化学元素发现者,这也是自古代人类知道金、银、铜、铁等元素以来,第一个有确切发现记录的化学元素。布兰德的发现起初被作为一种昂贵的奇观在欧洲宫廷间巡回展览。罗伯特·波义耳后来破解了这个秘密并改进了提取方法,将磷带入了科学的大门。磷的发现被认为是标记着炼金术的结束,以及化学作为一门科学的开始。

然而,白磷是一头难以驯服的野兽。它具有极高的毒性:白磷剧毒,误食0.1克即可致命,且在空气中极易自燃(燃点仅为30°C左右)必须保存在水中。到了19世纪,白磷被广泛用于制造火柴。这不仅催生了火柴工业的繁荣,也带来了一场公共卫生的浩劫。在通风不良的火柴工厂里,工人们(大多是女工和童工)长期吸入白磷蒸汽,导致了一种极其恐怖的职业病——“磷毒性颌骨坏死”。患者的牙齿会脱落,下颌骨在剧痛中坏死腐烂,甚至能在暗处发出绿光,最终痛苦地死去。

不仅如此,在常温下,白磷就能在空气中缓慢氧化并自燃,因此无法在自然界中稳定存在。白磷在战争中被制成燃烧弹,成为一种极其残忍的武器。白磷,这个意为“带来光”的元素,彻底变成了“魔鬼的元素”。在第一次世界大战中,白磷弹因其可怕的杀伤力而被使用。
红磷,来自维也纳的救赎
到了19世纪中叶,科学界已经开始意识到白磷带来的深重灾难,但由于资本的逐利性,白磷火柴依然大行其道。 白磷火柴导致的“磷毒性颌骨坏死”正在摧毁无数工人的生命,工业界急需一种安全、稳定的替代品。化学家们面临着一个紧迫的问题:能否改变磷的性质?
奥地利化学家安东·冯·施勒特尔在维也纳的实验室里找到了答案。他开始研究磷在不同条件下的热力学行为。1845年,施勒特尔进行了一项大胆的实验。他将极易爆炸自燃的白磷放入一个密闭的玻璃烧瓶中,抽空空气并充入惰性气体(氮气或二氧化碳)以防止其燃烧,然后将其加热到250°C左右。
几个小时后,烧瓶冷却。施勒特尔发现,剧毒且透明的白磷消失了,取而代之的是一种暗红色的粉末。这种红色的物质不仅没有毒性,而且非常稳定,在240°C以上才会燃烧,在室温下根本不会自发发光,也不会自燃。该成果在1847年发表。这是一种全新的同素异形体:红磷。

施勒特尔证明了白磷和红磷的化学式都是P,但分子排列方式完全不同。白磷由4个磷原子组成的P₄分子构成,结构不稳定,而红磷则是一种聚合物,原子以网状相连,结构稳固。完全相同的原子,仅仅是原子排列方式的改变,就彻底抹去了它的剧毒和暴戾。化学家深深的体会到了”结构决定性质“的基本规律
红磷的发现彻底改变了世界工业史。英国实业家亚瑟·奥尔布赖特将施勒特尔的实验室成果转化为大规模的工业生产。随后,瑞典人约翰·爱德华·伦德斯特伦利用红磷发明了“安全火柴”——将红磷涂在火柴盒的摩擦面上,而将氯酸钾等氧化剂涂在火柴头上。只有两者摩擦,才会点燃。
这一发明迅速终结了白磷火柴的统治地位,消灭了恐怖的“磷毒性颌骨坏死”。安东·冯·施勒特尔的一个小小加热实验,不仅是对物质结构的深刻洞见,更是一场挽救了成千上万底层工人生命的伟大救赎。
紫磷, 晶体里的深邃宇宙
在红磷拯救了火柴工业之后,磷的故事并没有结束。德国物理学家和化学家约翰·威廉·希托夫将目光投向了更深微的晶体结构。希托夫是一位极其细致的科学家,他深知我们所见到的红磷其实是一种无定形体,这意味着它的内部原子排列是杂乱无章的。希托夫思考的问题是:如果给这些杂乱的原子足够的能量和时间,它们能否排列成完美规则的晶体?
1865年,希托夫将红磷与铅一起放入一个密封的管子中,加热到惊人的550°C的高温,然后让其在极其缓慢的过程中冷却,过程大概持续数天甚至数周。在这个过程中,用铅作溶剂,让磷原子在其中重新排列。随后,用稀硝酸将铅溶解掉。留在试管底部的,不再是暗红色的粉末,而是一种闪耀着金属光泽的、紫黑色的单斜晶体:紫磷。
希托夫通过详细的物理和化学分析,确认这是一种新的磷同素异形体,并系统记录了其性质。紫磷具有复杂的五边形管状结构。这些由磷原子组成的空心管以特定方式排列堆积,形成独特的晶体结构。其外观具有金属光泽的紫色或紫铜色晶体,这也是其名称的由来。紫磷化学性质比白磷惰性得多,在空气中不会自燃。但仍可在加热条件下与氧气等物质反应。其毒性远低于剧毒的白磷。这就是紫磷,在很长一段时间里,它也被科学界尊称为“希托夫金属磷”。

紫磷的发现是一个纯粹的基础科学胜利。它比红磷更加稳定,是磷的层状聚合物结构。虽然紫磷在当时并没有像红磷那样立即带来巨大的工业应用,但它向科学界证明了,元素同素异形体的复杂性远远超出了人们的想象。它就像是磷家族中的一位隐士,静静地躲在结晶学的教科书里,等待着量子力学时代的到来。直到2019年,科学家们才首次通过现代手段成功剥离出单层的紫磷二维材料(紫磷烯)。
黑磷,物理学的“跨界玩家”
时间进入20世纪,哈佛大学的物理实验室里经常会响起了液压机的轰鸣声。物理学家珀西·威廉姆斯·布里奇曼(后来因此获得诺贝尔物理学奖)被称作“高压暴君”。他不满足于化学家们只在温度和化学试剂上做文章,他想用纯粹的物理暴力——“压力”——来逼迫原子发生改变。
1914年,布里奇曼将剧毒的白磷放入他自己设计的超高压装置中,同时施加了200°C的温度和高达1.2万个大气压(相当于深海一万米的压力)的恐怖压力。在这样极端的物理压迫下,白磷分子的四面体结构彻底崩溃,原子被强行压实,被迫重新组合成一种极其紧密的瓦楞状层状结构。当布里奇曼打开压力舱时,奇迹再现:白磷消失了,他得到了一种外观极其类似石墨的黑色片状晶体:黑磷。

黑磷的结构更加奇特,它的磷原子排列成层状结构,类似石墨。这使得它在某些方向上具有特殊的电学性质。它是磷的同素异形体中最致密、在热力学上最稳定的一种。它不会自燃,极其难溶,甚至具有了导电的半导体性质。2014年后,科学家发现,当黑磷被剥离成单原子层(磷烯)时,它展现出了优异的半导体性能,在柔性电子、传感器领域潜力巨大,被称为“梦幻材料”。
黑磷的诞生标志着人类开始拥有通过改变空间物理维度来创造新材料的能力。在被发现后的近一个世纪里,黑磷一直默默无闻。但历史的齿轮在2014年发生了转折。
磷的应用
说完了磷的发现史,我们再来聊聊磷的应用。磷位于元素周期表第三周期,第五主族。磷是典型的非金属元素。磷原子最外层有5个电子(电子构型为 3s²3p³),它更倾向于获得3个电子形成-3价的阴离子(P³⁻),或者通过共用电子对形成共价化合物,以达到稳定的稀有气体电子构型。这驱使它极易与其他元素(尤其是电负性高的氧)发生反应。因此,磷在日常生活和人体中主要以化合物的形式存在,而不是单质磷。其中磷酸和磷酸盐是磷元素存在的最常见,也是最稳定的形式
身体中最坚硬的堡垒
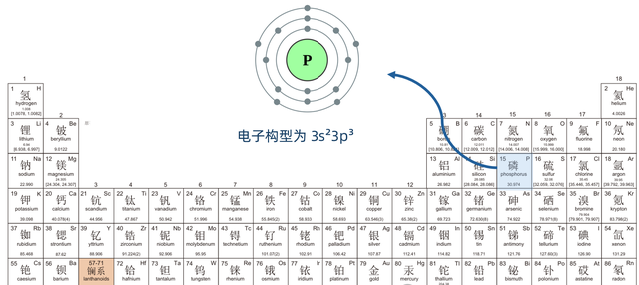
人体内约85%的磷以羟基磷灰石的形式存在于骨骼和牙齿中,是维持其硬度的主要矿物质。可以说,脊椎动物最坚硬的堡垒就是通过磷来构筑的。我们通常认为骨骼是钙的杰作,但事实上,没有磷,钙只是一盘散沙。
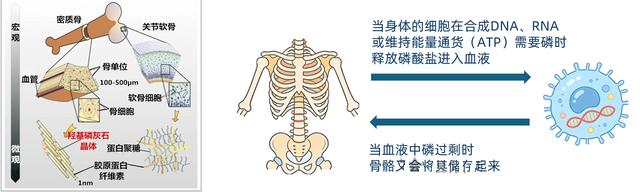
羟基磷灰石,这种晶体像钢筋一样嵌入在胶原蛋白构成的“水泥”网络中,赋予了骨骼极高的抗压强度和韧性。此外,骨骼还是人体巨大的“磷酸盐银行”——当身体的细胞在合成DNA、RNA或维持能量通货(ATP)需要磷时,骨骼会释放磷酸盐进入血液;当血液中磷过剩时,骨骼又会将其储存起来。
现代医学利用合成的羟基磷灰石涂层覆盖在钛合金人工关节或种植牙的表面。因为这种成分与人体天然骨骼几乎一致,它能欺骗人体的免疫系统,促进周围的真实骨细胞在假体上生长、融合(即骨结合),极大地提高了人工关节的使用寿命。许多现代高端抗敏牙膏中加入了微纳级的羟基磷灰石,它们能够直接填补牙齿表面微小的釉质裂纹。这个过程也被称作“仿生自我修复”
餐桌上的魔术师
在我们的餐桌上,磷扮演着多重角色:它既是维持生命运转的绝对必需品,又是现代食品加工业中不可或缺的“化学魔术师”。
酸度调节剂和酸味剂:提供清爽、尖锐的酸味。磷酸常用于可乐、雪碧等碳酸饮料,是其标志性酸味的主要来源。磷酸也用于某些果酱、果冻、糖果中调节酸度和口感。需要注意的是碳酸饮料(尤其是可乐类)中的磷酸可能会通过两种机制影响钙的平衡。一方面,磷酸与钙在肠道中可能形成不易吸收的磷酸钙盐,从而减少钙的吸收。另一方面,高磷摄入可能干扰体内钙磷代谢平衡,为维持血液中钙磷浓度的恒定,身体可能从骨骼中动用钙质,长期如此可能降低骨密度。

螯合剂和稳定剂:食品中的金属离子(如Fe²⁺/Fe³⁺,铜离子)能极大地促进油脂的自动氧化,产生醛、酮等有异味的物质;金属离子也会催化水果、蔬菜酚类物质的氧化聚合,导致颜色变深、变褐(如苹果、土豆切面变黑)。磷酸盐的分子结构中有多个带负电的氧原子,这些带负电的氧原子能与金属离子结合,防止其催化氧化反应,从而起到防腐、保色、稳定的作用。例如,在加工肉制品(如火腿、香肠)中,磷酸盐(如三聚磷酸钠)可以:提高肉的持水性,使产品更嫩、更多汁。整合金属离子,抑制脂肪氧化,保持风味。
养活世界的基石与清洁的代价
如果说前两项是关于个体的生存,那么磷在农业和工业中的应用,则直接决定了人类文明的人口上限和生活质量。
植物的根系发育、开花结果和光合作用极其依赖磷。自然土壤中的磷通常被固定在矿物中,植物难以吸收。水溶性的磷酸盐化肥能够直接为植物提供“速效营养”。
1840年代, 德国化学家尤斯图斯·冯·李比希提出了“最小因子定律”,指出植物的生长取决于土壤中最稀缺的那种养分,并明确指出磷是关键瓶颈。这标志着现代农业化学的开端。

之前,我们提到欧洲掀起的疯狂的“鸟粪热”。他们争夺的不仅仅是N元素,鸟粪中也含有磷元素。随着鸟粪枯竭,人类转向开采地下不可再生的磷矿石,并用硫酸将其处理成“过磷酸钙”等高效化肥。
三聚磷酸钠(STPP)曾是洗衣粉中的核心成分。它的原理是作为“水软化剂”,能够螯合(抓住)硬水中的钙镁离子,防止它们与表面活性剂结合形成沉淀,从而让洗衣粉在硬水中也能产生丰富的泡沫并将污垢悬浮起来。磷酸盐洗衣粉大行其道。但未经处理的生活污水排入湖泊,导致了极其严重的富营养化,最终导致蓝藻疯狂繁殖,耗尽水中氧气,使得大面积湖泊变成死水。随后,全球各国陆续颁布了“禁磷令”,推广无磷洗涤剂。
在日用工业中,磷酸酯被广泛用作塑料和电子产品外壳的阻燃剂。近年来,磷酸铁锂(LiFePO4)成为了新能源汽车动力电池的核心正极材料,它比三元锂电池更安全、寿命更长,再次将磷元素推上了新能源革命的中心。
结束语
以上就是关于磷的发现史和日常的应用。单质磷有四种不同的同素异形体,它们有截然不同的性质。同时磷的化合物又有广泛的应用,从人体的骨骼,日常的餐桌,再到清洁剂和新能还原,导出都有磷的身影。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
今天咱们来聊一个我们每天都会接触到的奇异元素:磷。它像被...
硫酸被称为 “工业之母” 的原因主要有以下三点: ① HSO 作为...
早在19世纪以前,一些有远见的化学家就指出:考虑到将来的粮...
Fritz Haber 1868一1934 翻阅诺贝尔化学奖的记录,就能看到1916一 1...
黑火药是我国古代四大发明之一,它是用硝酸钾、木炭粉和硫黄...
在葡萄酒的中文背标上,在原料与辅料一栏中会标示有:葡萄汁...