
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
实验证明,只有发生碰撞的分子的能量等于或超过某一定的能量Ec(可称为临界能)时,才可能发生有效碰撞。具有能量大于或等于Ec的分子称为活化分子。
在一定温度下,将具有一定能量的分子百分数对分子能量作图,如图1所示。从图1可以看出,原则上来说,反应物分子的能量可以从0到∞,但是具有很低能量和很高能量的分子都很少,具有平均能量Ea的分子数相当多。这种具有不同能量的分子数和能量大小的对应关系图,叫做一定温度下分子能量分布曲线图。
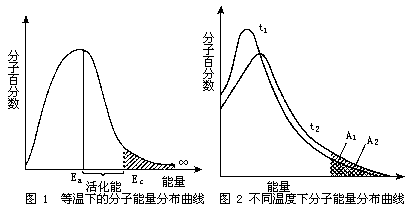
图1中,Ea表示分子的平均能量,Ec是活化分子具有的最低能量,能量等于或高于Ec的分子可能产生有效碰撞。活化分子具有的最低能量Ec与分子的平均能量Ea之差叫活化能。
不同的反应具有不同的活化能。反应的活化能越低,则在指定温度下活化分子数越多,反应就越快。
不同温度下分子能量分布是不同的。图2是不同温度下分子的能量分布示意图。当温度升高时,气体分子的运动速率增大,不仅使气体分子在单位时间内碰撞的次数增加,更重要的是由于气体分子能量增加,使活化分子百分数增大。图2中曲线t1表示在t1温度下的分子能量分布,曲线t2表示在t2温度下的分子能量分布(t2>t1)。温度为t1时活化分子的多少可由面积A1反映出来;温度为t2时,活化分子的多少可由面积A1+A2反映出来。从图中可以看到,升高温度,可以使活化分子百分数增大,从而使反应速率增大。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
在化学反应中,驱动力指的是推动反应进行的内在因素,它决定...
一.核心概念辨析 中间体:寿命长于分子振动的瞬态物种,多步...
活化分子百分数和活化分子数,理解它对掌握化学反应速率至关...
化学反应的焓变越大,代表这个反应受温度变化的影响越大吗?...
在化学热力学和分析化学中,我们常常听到这样的说法:“如果...
...