
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
【原理】氨冷却到—33.4℃就能凝聚成无色液体。储存在钢瓶里的液态氨处于700~800kPa压强下,因此把液态氨封存在玻璃的封管里是不安全的。把氯化二氨合银[Ag(NH3)2Cl]封存在封管里,可以利用它的热离解平衡实现氨和氨合物之间的转换。
![]()
从以上化学方程式可以看出,加热氨合物,封管内的压强会随着氨气的增加而变大。撤去热源,氨能有效地被氯化银“吸收”。如果一面加热氨合物,一面使生成的氨冷却,就能顺利地使氨在受压和冷却的条件下转变成液态。如果取消上述反应条件,随着液氨的气化,氨又跟氯化银结合而恢复原状。
【操作】
(1)称取3g氯化钠和5g硝酸银,分别溶于蒸馏水中配成溶液,然后在避光条件下使两种溶液混合。过滤所得的溶液,并把氯化银沉淀烘干,研碎后待用。
(2)把氯化银移入25×200mm的试管中,用一根长玻管插入到氯化银固体的下方,缓慢通入干燥的氨气。这时可以从试管外壁感到氨跟氯化银反应的热效应。10~15分钟后,热效应已不明显,氯化银的氨合即告完成。
(3)取一根长约200mm,内径约8mm的硬质玻璃管,把一端熔封起来,然后在中部加热并弯成直角。冷却后装入氯化二氨合银,并使它集中在已封口的一端,长达30mm左右。接着小心地把玻管的另一端也熔封住,制成一支特制的直角封管。
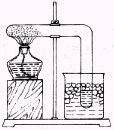
(4)如右图所示,把直角封管的一端浸没在冰盐混合冷却剂中,微微加热封管装有氯化二氨合银的一端。很快就能看到冷却端有无色液态氨形成。
【说明】
(1)当封管内产生液氨时,管内压强较大,所以决不可加热液氨,也不要撞击封管,以免发生炸裂。让液氨在自然升温条件下逐步跟氯化银结合,管内就恢复常压。
(2)该封管也可反复多次使用,不用时要包上黑纸,防止光照。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
人教版必修二教材P18课后习题: 第一个实验现象:溶液变蓝。水...
在化学课本里有这样一段话:在稀释浓硫酸时,只能把浓硫酸慢...
浓硫酸稀释放热原因 1.浓硫酸溶于水时,硫酸分子克服分子间的...
浓硫酸稀释操作不当会引发喷溅、爆炸?今天用最直观的方式教...
在很多教辅书中,硫沉淀一般被描述成淡黄色沉淀,而在人教版...
一、铁离子的催化作用 审题点1:对比催化效果时,注意浓度是...