
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
碳位于第二周期ⅣA,氮位于第二周期VA,根据同周期元素气态氢化物的稳定性从左到右依次增强的变化规律,可得出甲烷的稳定性小于氨气的稳定性。查《高级中学课本化学(必修)第一册》148页表5一5得:碳氢键C一H键能为413kJ/mol,氮氢键N一H键能为39IkJ/mol,N一H键能小于C一H键能。在本页13、14行中有这样一段叙述:键能越大,表示化学键越牢固,含有该键的分子越稳定。由此又可得出:甲烷的稳定性大于氨气的稳定性。以上两种分析结果截然相反,不少学生感到疑惑。那么,甲烷与氨气的稳定性到底谁大呢?
在1.01×105Pa和25℃的条件下,将lmol理想气态分子AB中的键打开,成为理想气态的A+B原子,所需要的能量叫做AB的离解能(单位kJ/mol),常用符号D表示。对双原子分子来讲,离解能D就是键能(用符号E表示),而多原子分子的离解能与键能就不同了。多原子分子含有多个键,键的离解是分级的,分子中有几个键,离解就分几级,每一级离解都有一个离解能,即使分子中的键完全相同(等价键),其各级离解能也是不同的,分子中所有等价键离解能的平均值即为键能。每一级离解能的大小标志着分子进行该级离解的难易程度,而键能,则标志着分子中的所有等价键离解的平均难易程度。分子只要发生第一级离解,就被破坏,所以分子稳定性大小是由第一级离解能大小决定的。第一级离解能越大,分子越稳定。对于大多数分子来说,第一级离解能的大小顺序与键能的大小顺序是一致的,故可通过比较键能的大小判断分子稳定性的强弱。但少数分子第一级离解能的大小顺序与键能的大小顺序是不一致的(如CH4与NH3),这就需要通过比较第一级离解能的大小判断分子稳定性的大小。
CH4的分级离解情况如下:
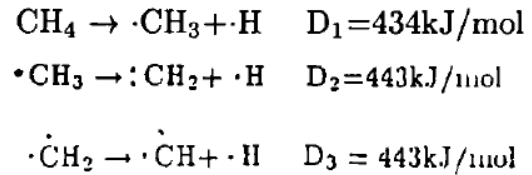

·
虽然E'<E,但D'1>D1,故NH3的稳定性要大于CH4的稳定性。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
电子、中子、质子的质量测量是贯穿经典物理到近代物理的重要...
【定义】又称离子有效半径,是通过实验测定的。一般认为的离...
关于117号元素是金属元素还是非金属元素的讨论以下几种意见:...
氢是元素周期表中的第一号元素,元素名来源于希腊文,原意是...
在我们身边的物质世界中,有气体,有液体,也有固体。他们都...
...