
|
学习小专题 |

|
学习小专题 |
 [课题与实验t] 苯酚钠溶液中加入 FeCl₃ 溶液后,到底发生了怎 作者:化学自习室 来源:未知 日期:2026-03-01 18:06:10 点击:200 所属专题:苯酚
[课题与实验t] 苯酚钠溶液中加入 FeCl₃ 溶液后,到底发生了怎 作者:化学自习室 来源:未知 日期:2026-03-01 18:06:10 点击:200 所属专题:苯酚
苯酚的酸性极弱, 苯酚钠 在水溶液中会发生水解,溶液呈碱性:C₆H₅O⁻ + H₂O ⇌ C₆H₅OH + OH⁻如果在这样的溶液中加入少量 FeCl₃ 溶液,溶液中的 Fe³⁺ 在强碱性环境中会以 Fe(OH)₃ 的形式析...
 [试剂药品] 乙醇在实验中的作用 作者:化学自习室 来源:未知 日期:2025-09-09 16:36:57 点击:909 所属专题:醇析 沉淀洗涤
[试剂药品] 乙醇在实验中的作用 作者:化学自习室 来源:未知 日期:2025-09-09 16:36:57 点击:909 所属专题:醇析 沉淀洗涤
一、乙醇的结构 首先,和水(H-OH)相比,乙醇(CHCH-OH)分子中的-CH 2 CH 3 是推电子基团,使得CH 3 CH 2 OH中-OH的极性变弱,是弱极性分子。 所以水(H-OH)中加入乙醇(CHCH-OH),极性减弱。 当乙醇与非极性溶剂(如环己烷)混合时,会提高混合溶剂的极性。 或者说,乙...
 [课题与实验t] 银氨溶液为什么不能久置 作者:化学自习室 来源:未知 日期:2025-05-27 16:24:47 点击:989 所属专题:银氨
[课题与实验t] 银氨溶液为什么不能久置 作者:化学自习室 来源:未知 日期:2025-05-27 16:24:47 点击:989 所属专题:银氨
银氨溶液中的成分要从微粒的角度看,二氨合银络离子、铵根离子、硝酸根离子、氢氧根离子在溶液中自由移动,不必纠结银氨络离子跟那个阴离子在一起,即不必纠结银氨溶液的溶质是氢氧化二氨合银还是硝酸二氨合银。 银镜反应中使用的银氨溶液(通常为硝酸银的氨水溶液)需...
 [课题与实验t] 实验考点系列:醛基检验 作者:化学自习室 来源:未知 日期:2025-05-19 17:02:06 点击:2120 所属专题:醛类
[课题与实验t] 实验考点系列:醛基检验 作者:化学自习室 来源:未知 日期:2025-05-19 17:02:06 点击:2120 所属专题:醛类
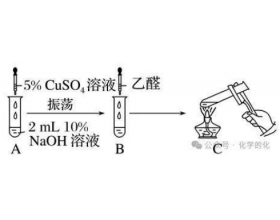
一、检验醛基的方法及原理 检验方法1:新制氢氧化铜溶液 实验现象:A中出现蓝色絮状沉淀,滴入乙醛,加热至沸腾后,C中有砖红色沉淀产生 有关方程式: A 中: C 中: 检验方法2:银氨溶液 实验现象:向A中滴加氨水,现象为先产生白色沉淀,继续滴加氨水沉淀溶解,溶液变...
 [课题与实验t] 实验考点系列:苯酚性质 作者:化学自习室 来源:未知 日期:2025-05-19 16:02:47 点击:1018 所属专题:苯酚
[课题与实验t] 实验考点系列:苯酚性质 作者:化学自习室 来源:未知 日期:2025-05-19 16:02:47 点击:1018 所属专题:苯酚
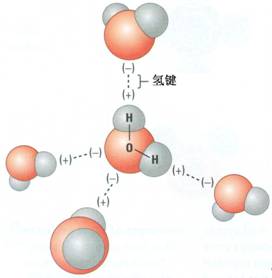
一、 苯酚的溶解性 审题注意1:苯酚遇水后熔点降低(纯苯酚是固体,但是苯酚遇水呈液态) 苯酚分子之间能够形成氢键(O-HO),导致纯苯酚熔点高,呈现固。水分子介入以后,也可与苯酚的羟基形成氢键(O-HO),破坏苯酚子间的氢键,有序结构被破坏以后,固态苯酚的稳定性...
 [课题与实验t] 为什么苯酚会使酸性高锰酸钾褪色? 作者:化学自习室 来源:未知 日期:2023-05-17 21:31:48 点击:2595 所属专题:苯酚
[课题与实验t] 为什么苯酚会使酸性高锰酸钾褪色? 作者:化学自习室 来源:未知 日期:2023-05-17 21:31:48 点击:2595 所属专题:苯酚
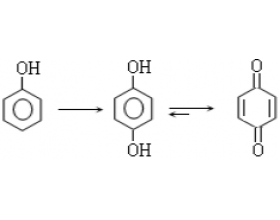
高中课本中提到苯酚在空气中放置会被氧化成粉红色物质,由此可以说明苯酚具有还原性,能被空气中的氧气氧化。那苯酚在遇到酸性高锰酸钾溶液时是否同样被氧化成粉红色物质呢?笔者通过实验验探究了苯和酸性高锰酸钾溶液反应的本质,具体实验流程如下。 1.实验过程: 1.1 ...
 [课题与实验t] 细说氢氧化铜与新制氢氧化铜 作者:段昌平 来源:未知 日期:2021-04-23 09:44:00 点击:12197 所属专题:新制氢氧化铜
[课题与实验t] 细说氢氧化铜与新制氢氧化铜 作者:段昌平 来源:未知 日期:2021-04-23 09:44:00 点击:12197 所属专题:新制氢氧化铜
高中教材中的新制Cu(OH) 2 是一个特定试剂名称, 认为新制Cu(OH) 2 就 是Cu(OH) 2 的悬浊液。但事实上新制 Cu(OH) 2 又不同于Cu(OH) 2 , 学生在观察演示实验和做实验时已经注意到这一点。为了区别Cu (OH) 2 与新制Cu(OH) 2 , 以及实验时为什么要制取新制Cu(OH) 2 , 谈谈...
 [课题与实验t] 乙醛的氧化反应实验说明 作者:化学自习室 来源:未知 日期:2019-11-13 09:09:12 点击:3215 所属专题:乙醛 银镜反应
[课题与实验t] 乙醛的氧化反应实验说明 作者:化学自习室 来源:未知 日期:2019-11-13 09:09:12 点击:3215 所属专题:乙醛 银镜反应
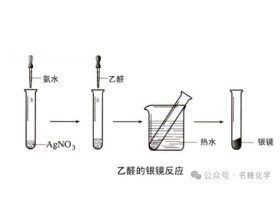
一、与Tollens (托林试剂)反应 CH 3 CHO+2 [Ag(NH 3 ) 2 ] + + 2 OH - CH 3 COO - +2 Ag + NH 4 + +H 2 O + 3 NH 3 此实验反应又名银镜反应 ①Tollens 又名银氨溶液 Ag + +NH 3 ·H 2 O=AgOH+ NH 4 + AgOH+2 NH 3 H 2 O = [Ag(NH 3 ) 2 ] + +OH - +2 H 2...
 [课题与实验t] 醛基与新制Cu(OH)2的反应疑难问题探析 作者:化学自习室 来源:未知 日期:2019-06-14 15:13:43 点击:5939 所属专题:乙醛
[课题与实验t] 醛基与新制Cu(OH)2的反应疑难问题探析 作者:化学自习室 来源:未知 日期:2019-06-14 15:13:43 点击:5939 所属专题:乙醛
高中化学常用氢氧化铜检验醛基的存在,教材强调使用新制的氢氧化铜,主要是因为从溶液中新沉淀生成的氢氧化铜微显两性,能溶于过量的氢氧化钠溶液形成易溶于水的四羟基铜酸钠: Cu( OH) 2 + 2NaOH = Na 2 [Cu( OH) 4 ] 且溶液中存在如下平衡:[Cu( OH) 4 ] 2 - 2OH ...
 [课题与实验t] 导学与导图:醛类的银镜反应及与新制氢氧化铜悬浊液反应实验 作者:化学自习室 来源:未知 日期:2021-04-23 11:04:45 点击:2487 所属专题:银镜反应 乙醛与氢氧化铜
[课题与实验t] 导学与导图:醛类的银镜反应及与新制氢氧化铜悬浊液反应实验 作者:化学自习室 来源:未知 日期:2021-04-23 11:04:45 点击:2487 所属专题:银镜反应 乙醛与氢氧化铜
氨水量宜试管净, 水浴温热出银 镜。 液稀碱多升温慢, 喜观液中沉淀红。 解释: 1、氨水量宜试管净,水浴温热出银镜:这句的意思是点明了关于银镜反应实验应注意的 问题。“氨水量宜”的意思是说在配制银氨溶液的时候,氨水不能过量,以沉淀恰好溶解为宜(若氨水过量,...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
苯酚的酸性极弱, 苯酚钠 在水溶液中会发生水解,溶液呈碱性...
硝酸银溶液中滴加氨水先析出AgOH: AgNO 3 +NH 3 ·H 2 O=AgOH↓+N...
在做醛基的检验实验银镜反应中,实验的成败与否与配制的银氨...
银氨溶液中的成分要从微粒的角度看,二氨合银络离子、铵根离...
一、检验醛基的方法及原理 检验方法1:新制氢氧化铜溶液 实验...
一、 苯酚的溶解性 审题注意1:苯酚遇水后熔点降低(纯苯酚是...
高中课本中提到苯酚在空气中放置会被氧化成粉红色物质,由此...
银镜反应是一个重要的有机化学反应,一个有趣的实验,一个很...