
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
什么叫杂化?同一原子的能量相近的原有的原子轨道“混杂”起来,重新组合形成新轨道的过程,叫做杂化。
什么叫杂化轨道?新组合的原子轨道叫做杂化轨道。
为什么要杂化?杂化轨道形成的化学键的强度更大,体系的能量更低。
杂化的动力:受周围原子的影响。
为什么杂化后成键,体系的能量降低?杂化轨道在一个方向上更集中,便于轨道最大重叠。
杂化轨道的构型决定了分子的几何构型:杂化轨道有利于形成σ键,但不能形成π键。由于分子的空间几何构型是以σ键为骨架,故杂化轨道的构型就决定了其分子的几何构型。
一.杂化轨道理论的基本要点
(1)概念:原子在形成分子时,为了增强成键能力,同一原子中能量相近的不同类型(S、P、D…)的几个原子轨道可以相互叠加进行重新组合,形成能量、形状和方向与原轨道不同的新的原子轨道。这种原子轨道重新组合的过程称为原子轨道的杂化,所形成的新的原子轨道称为杂化轨道。
(2)注意事项:
①只有在形成分子的过程中,中心原子能量相近的原子轨道才能进行杂化,孤立的原子不可能发生杂化。
②只有能量相近的轨道才能互相杂化。常见的有:ns np nd,(n-1)d ns np;
③杂化前后,总能量不变。但杂化轨道在成键时更有利于轨道间的重叠,即杂化轨道的成键能力比未杂化的原子轨道的成键能力增强,形成的化学键的键能大。这是由于杂化后轨道的形状发生了变化,电子云分布集中在某一方向上,成键时轨道重叠程度增大,成键能力增强。
④杂化所形成的杂化轨道的数目等于参加杂化的原子轨道的数目,亦即杂化前后,原子轨道的总数不变。⑤、杂化轨道的空间构型取决于中心原子的杂化类型。不同类型的杂化,杂化轨道的空间取向不同,即一定数目和一定类型的原子轨道间杂化所得到的杂化轨道具有确定的空间几何构型,由此形成的共价键和共价分子相应地具有确定的几何构型。
二.最常见的杂化轨道类型简介
杂化轨道基本类型 | sp | sp2 | sp3 |
参加杂化的原子轨道 | 1个s和1个p | 1个s和2个p | 1个s和3个p |
杂化轨道数目 | 2个sp杂化轨道 | 3个sp2杂化轨道 | 4个sp3杂化轨道 |
每个杂化轨道的成分 |
|
|
|
杂化轨道间的夹角 | 180° | 120° | 109°28′ |
几何构型 | 直线型 | 平面三角形 | 正四面体形 |
实例 | BeCl2,HgCl2 | BF3 | CH4,SiF4 |
中心原子 | Be,Hg | B | C,Si |




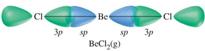
①sp杂化轨道:是1个ns轨道与1个np轨道杂化形成2个sp杂化轨道。BeCl2的成键过程,Be原子的杂化。两个sp杂化轨道的夹角为180º,空间构型:直线型。
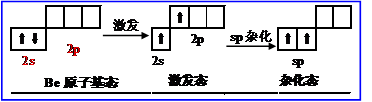
![]()
②sp2杂化轨道:是一个原子的1个ns轨道和2个np轨道之间进行杂化,形成3个等价的sp2杂化轨道。3个sp2杂化轨道互成120°,sp2杂化形成平面正三角形分子。例如BCl3的成键过程,b原子的杂化。
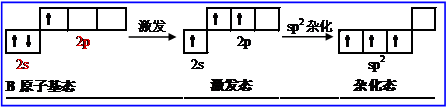
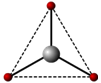
③sp3杂化轨道:是一个原子的1个s轨道和3个p轨道之间进行杂化,形成4个等价的sp3杂化轨道。4个sp3杂化轨道互成109.5°,sp3杂化形成正四面体结构分子。例如CH4的成键过程,C原子的杂化。
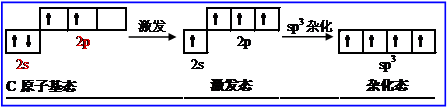
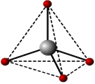
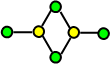
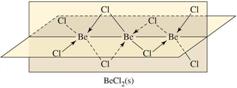
特殊:BeCl2是共价化合物,在气态为双聚分子(BeCl2)2(在773~873K下),温度再高时,二聚体解离为单体BeCl2,在1273K完全离解。固态BeCl2具有无限长链结构。在BeCl2(g)中Be为sp杂化,直线型。在双聚体(BeCl2)2(g)中Be为sp2杂化。在固态BeCl2中Be为sp3杂化。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。1mol 氨中氢键数量分析 一、氢键形成机制 NH分子结构 H原子作为氢键供体(需与高电负性...
二氧化氮(NO)中氮原子的杂化类型为 sp杂化,具体分析如下: 1.计算 n (的价层电子对数...
...
【导读】 以下是快速判定氢键强弱的基本原则,实际案例中经常会进一步考虑综合因素的...
根据价电子互斥理论, ClO 2 中氯原子周围的价电子对数计算为 3.5,理论上应倾向于 sp...
【导读】分子间作用力(范德华力)的来源是取向力、诱导力和色散力。 ①一般情况下,极...