
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、超分子的定义
超分子是由两种或多种分子通过非共价键相互作用(如氢键、静电作用、疏水作用、范德华力等)形成的分子聚集体。例如冠醚、DNa双螺旋结构、杯酚等都属于超分子。
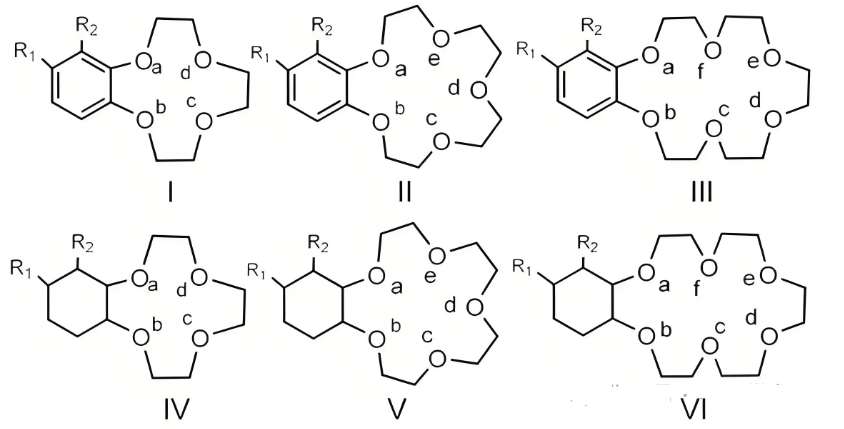
冠醚,是分子中含有多个-氧-亚甲基-结构单元的大环多醚。常见的冠醚有15-冠-5、18-冠-6,冠醚的空穴结构对离子有选择作用,在有机反应中可作催化剂。冠醚有一定的毒性,必须避免吸入其蒸气或与皮肤接触。
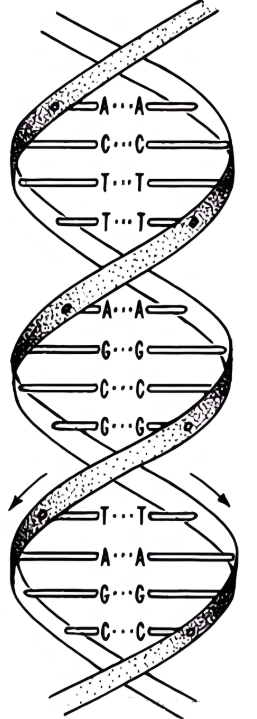
DNA双螺旋(外文名DNA Double Helix)指的是一种核酸的构象,在该构象中,两条反向平行的多核苷酸链相互缠绕形成一个右手的双螺旋结构。
再如:

二、超分子的性质
1、分子识别
主体分子对客体分子有选择性结合的能力,如冠醚通过空穴尺寸匹配特定金属离子(如K⁺),形成超分子;杯酚通过分子间作用力分离C60和C70。
DNA的碱基互补配对通过氢键实现分子识别。
2、自组装
表面活性剂在水中形成胶束(疏水基团向内,亲水基团向外),用于去污。
细胞膜的双层磷脂结构(极性头部向外,非极性尾部向内)。
3、弱相互作用的协同效应
单个弱作用力(如氢键)较弱,但多种作用力协同可形成稳定的超分子结构。
三、高中化学对超分子的考查方式
1、基础概念判断
直接考查定义,例如:“超分子通过共价键/非共价键形成?”(正确答案为非共价键)。
典型超分子实例分析
冠醚:常结合有机反应考查其作用(如增加高锰酸钾在苯中的溶解度),并辨析是否涉及配位键(冠醚与金属离子为弱相互作用,非配位键)。
杯酚:分离富勒烯(C60和C70)的原理(分子识别)。
DNA双螺旋:通过氢键形成超分子结构。
2、实际应用与现象解释
洗涤剂去污原理(胶束包裹油渍)。
冠醚作为相转移催化剂的作用(如提高高锰酸钾氧化烯烃的效率)。
3、辨析超分子与配合物
超分子依赖弱相互作用,而配合物通过配位键结合(如冠醚与K⁺属于超分子,而[Fe(SCN)]ⁿ⁺属于配合物)。
四、备考建议
掌握教材中冠醚、杯酚、DNA等核心案例,理解其作用原理。
区分超分子与配合物的作用力类型(非共价键 vs 配位键)。
结合实验或生活现象(如洗涤剂去污、细胞膜结构)理解超分子的自组装特性。
五、超分子与配合物的区分要点
1. 作用力类型不同
超分子:通过非共价键(如氢键、范德华力、静电作用、疏水作用等)形成,作用力较弱且可逆。
例:冠醚与金属离子通过空穴尺寸匹配结合,依赖静电作用而非配位键。
配合物:通过配位键(一方提供孤电子对,另一方提供空轨道)结合,属于较强且稳定的化学键。
例:[Cu(NH3)4]2+中,NH3的N原子提供孤电子对,Cu2+提供空轨道形成配位键。
2. 结构特征差异
超分子:
结构灵活,依赖分子识别与自组装形成动态聚集体(如胶束、DNA双螺旋)。
无明确的内外界划分,通常由多种弱相互作用协同稳定。
配合物:
具有明确的内外界结构,中心原子与配体通过配位键结合,外界为抗衡离子。
例:[Cu(NH3)4]SO4中,[Cu(NH3)4]2+为内界,SO42-为外界。
3. 稳定性与可逆性
超分子:
稳定性低,易受温度、溶剂等外界条件影响而解离(如胶束在高浓度下才稳定)。
结合过程可逆,适合动态功能(如分子运输、识别)。
配合物:
配位键稳定性较高,解离需要较高能量(如破坏Fe(SCN)3需强酸或强配位剂)。
结构固定,常用于催化、金属离子检测等需要稳定性的场景。
4. 典型应用场景
超分子:
分子识别:杯酚分离C60和C70。
自组装:表面活性剂形成胶束去污,细胞膜双层磷脂结构。
配合物:
检测与分离:硫氰化铁(Fe(SCN)3)用于Fe3+的显色反应。
催化与生物功能:血红素(Fe2+配合物)参与氧气运输。
5、快速区分方法
看作用力:非共价键→超分子;配位键→配合物。
看结构:动态聚集体→超分子;明确内外界→配合物。
看稳定性:易解离→超分子;难解离→配合物。
例如:冠醚与K⁺通过静电作用结合(超分子),而[Cu(NH3)4]2+通过配位键形成(配合物)。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、为什么“摩擦”能加快结晶? 你可以把溶液里的溶质分子想...
一、物质的聚集状态的存在形式 1.通常物质有三态:固态、液...
物质熔点越高,沸点一定也越高吗? 答:不一定。熔点强调的是...
在常见元素中,硼注定是那特别的一个——价层电子只有3个,却...
...
...