
|
学习小专题 |

|
学习小专题 |
 [方法与规律e] 复杂配合物中中心原子化合价的判断 作者:化学自习室 来源:未知 日期:2025-09-12 15:52:45 点击:284 所属专题:配合物化合价
[方法与规律e] 复杂配合物中中心原子化合价的判断 作者:化学自习室 来源:未知 日期:2025-09-12 15:52:45 点击:284 所属专题:配合物化合价
判断中心原子的化合价,我们首先确定 配位原子 是否达到了稳定结构,只有达到稳定结构的原子才能提供孤电子进行配位。例如,氧原子最外层6个电子,满足8电子稳定结构才能配位,所以,除了配位键,氧原子先必需成2个键,如果没有成2个键,说明这个O原子显-1价。由此判断...
 [方法与规律e] 为何二氟化碘离子离子的空间构型为直线形,键角为90°,120°? 作者:化学自习室 来源:未知 日期:2025-08-07 11:09:55 点击:256 所属专题:分子空间结构判断
[方法与规律e] 为何二氟化碘离子离子的空间构型为直线形,键角为90°,120°? 作者:化学自习室 来源:未知 日期:2025-08-07 11:09:55 点击:256 所属专题:分子空间结构判断
分析: 依据价层电子对数计算公式分析, 可得价层电子对数=5=[2+3],故有2个配位原子F,形成2对成键电子对( 键),剩余3对孤电子对,其分子的空间构型可能如下三种情况; 依据孤对电子对不参加成键,只受到一个核的吸引,电子云比成键电子对更“肥大”,故电子对间斥力...
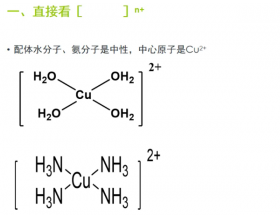 [方法与规律e] 配合物中心原子化合价判断 作者:化学自习室 来源:未知 日期:2025-06-24 07:00:26 点击:151 所属专题:配合物化合价
[方法与规律e] 配合物中心原子化合价判断 作者:化学自习室 来源:未知 日期:2025-06-24 07:00:26 点击:151 所属专题:配合物化合价
...
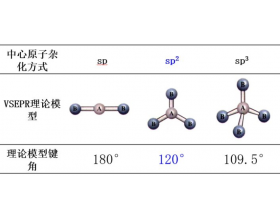 [方法与规律e] 键角比较规律 作者:化学自习室 来源:未知 日期:2025-05-27 16:00:52 点击:909 所属专题:键角
[方法与规律e] 键角比较规律 作者:化学自习室 来源:未知 日期:2025-05-27 16:00:52 点击:909 所属专题:键角
比较键角大小分析思路: 参照以下顺序来判断键角大小 ①先从中心原子的杂化类型来入手。因为杂化类型决定了分子的基本构型。 ②在中心原子杂化类型相同的情况下,应从孤电子对的数目来考虑问题。 ③在中心原子杂化类型相同,且孤电子对数目也相同时,再用中心原子或配原...
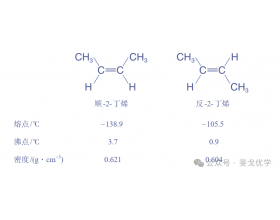 [方法与规律e] 如何判定顺反异构中分子的对称性、极性以及熔点和沸点的差异? 作者:化学自习室 来源:未知 日期:2025-02-18 17:05:36 点击:3296 所属专题:顺反异构
[方法与规律e] 如何判定顺反异构中分子的对称性、极性以及熔点和沸点的差异? 作者:化学自习室 来源:未知 日期:2025-02-18 17:05:36 点击:3296 所属专题:顺反异构
顺反异构中,分子的对称性、极性以及熔点和沸点存在以下差异: 1.对称性比较 反式异构体的对称性较好,原子排列较为对称,分子能更规则地排入晶体结构中 ,例如反 - 丁烯二酸,其分子呈对称结构. 顺式异构体的对称性相对较差,两个相同的原子或基团在双键的同侧,分子的...
 [方法与规律e] 如何比较分子的极性大小? 作者:化学自习室 来源:未知 日期:2025-02-18 16:18:13 点击:2052 所属专题:分子极性
[方法与规律e] 如何比较分子的极性大小? 作者:化学自习室 来源:未知 日期:2025-02-18 16:18:13 点击:2052 所属专题:分子极性
化学键学习过程中我们会遇到一个概念,就是化学键的极性,如何判断化学键的极性以及分子的极性也是高种化学考察的一个重要知识点。 STEP1 共价键的极性判断 化学键有无极性,是相对于共价键而言的。从本质上讲,共价键有无极性取决于共用电子对是否发生偏移,有电子对偏...
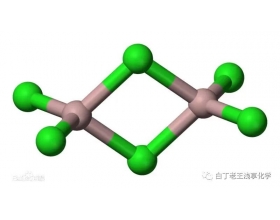 [方法与规律e] 判断配合物的配位数 作者:化学自习室 来源:未知 日期:2025-01-10 07:47:50 点击:931 所属专题:配合物 配位数
[方法与规律e] 判断配合物的配位数 作者:化学自习室 来源:未知 日期:2025-01-10 07:47:50 点击:931 所属专题:配合物 配位数
配合物的配位数是指直接同中心离子(或原子)配位的原子数目。高中化学配合物的配位数可按如下方法判断: 1.配合物的配位数等于配位原子及配位体的数目 有两种情况: (1)配位原子数目、配位体数目、中心离子与配位原子形成的配位键键数均相等 例如[Ag(NH3)2]NO3、[Cu(N...
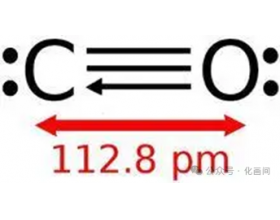 [方法与规律e] 例析大π键中电子数计算方法 作者:化学自习室 来源:未知 日期:2025-01-06 11:52:10 点击:1444 所属专题:大π键
[方法与规律e] 例析大π键中电子数计算方法 作者:化学自习室 来源:未知 日期:2025-01-06 11:52:10 点击:1444 所属专题:大π键
01 ― 概念 在多原子分子(就是三个或三个以上的原子构成的分子)中,如有相互平行的p轨道, 它们连贯地“肩并肩”地重叠在一起构成一个整体,p电子在多个原子间运动形成π型化学键,这种不局限在两个原子之间的π键称为离域π键或共轭大π键,或者简简单单就叫大π键。...
 [方法与规律e] 分子间作用力有三种,你知道吗? 作者:化学自习室 来源:未知 日期:2024-08-19 17:01:21 点击:678 所属专题:分子间作用力
[方法与规律e] 分子间作用力有三种,你知道吗? 作者:化学自习室 来源:未知 日期:2024-08-19 17:01:21 点击:678 所属专题:分子间作用力
分子间作用力的种类 分子间作用力 按其实质来说是一种电性的作用力,因此考察分子间作用力的起源就得研究物质分子的电性及分子结构。 分子间作用力可以分为以下三种力。 (1)取向力 取向力 发生在极性分子与极性分子之间。 由于极性分子的电性分布不均匀,一端显正电性...
 [方法与规律e] 四种方法比较物质中的键角大小 作者:化学自习室 来源:未知 日期:2024-08-19 14:20:00 点击:2088 所属专题:键角
[方法与规律e] 四种方法比较物质中的键角大小 作者:化学自习室 来源:未知 日期:2024-08-19 14:20:00 点击:2088 所属专题:键角
含有共价键的物质中相邻两键之间的夹角称为键角。键角是决定物质分子空间构型的主要因素之一。根据价层电子对互斥理论的分析,在高中阶段学习中,影响键角大小的因素主要有三: 一是中心原子的杂化类型; 二是中心原子的孤电子对数; 三是中心原子的电负性大小等。 现通过例...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。分析: 依据价层电子对数计算公式分析, 可得价层电子对数=5=[2+3],故有2个配位原子...
...
比较键角大小分析思路: 参照以下顺序来判断键角大小 ①先从中心原子的杂化类型来入手...
顺反异构中,分子的对称性、极性以及熔点和沸点存在以下差异: 1.对称性比较 反式异构...
01 ― 概念 在多原子分子(就是三个或三个以上的原子构成的分子)中,如有相互平行的p...
含有共价键的物质中相邻两键之间的夹角称为键角。键角是决定物质分子空间构型的主要因...
1.非环状小分子和离子中的大π键:大多数满足AB n 型,可以计算杂化类型。 首先:参与...
1.σ键与π键 σ键:原子轨道沿着轨道对称轴的方向“头碰头”重叠形成的共价键。 π键...