
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
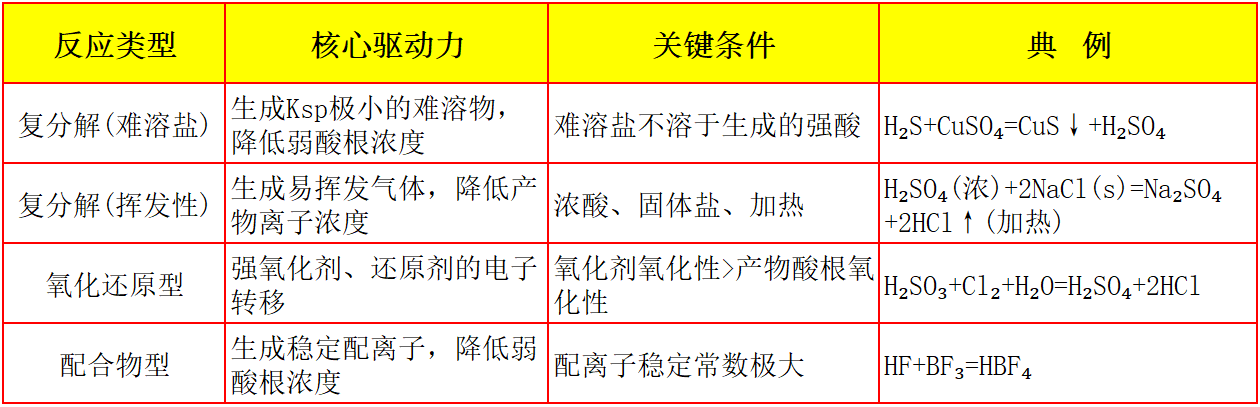
【导读】“强酸制弱酸”是复分解反应的常见规律,其本质是强酸电离出的H⁺更易与弱酸根结合,形成电离程度更小的弱酸。但在特定条件下也能发生“弱酸制强酸”,反应能够发生的根本原因在于反应的驱动力不再是简单的酸碱质子转移,而是引入了其他更强的热力学趋势,常见的驱动力有四类如下:
①生成难溶沉淀驱动反应;
②发生氧化还原反应,通过改变元素的化合价驱动反应;
③生成挥发性物质,通过加热移走气体生成物驱动反应;
④生成稳定的络合物,通过稳定的络合作用降低某种离子浓度驱动反应。
这些因素都改变了体系的自由能(ΔG),使得总反应得以自发进行,从而实现了“弱酸制强酸”这一看似反常的现象。
一、通过生成难溶性盐实现反应,其核心是利用极小的Ksp
当弱酸与强酸盐反应时,若能生成溶度积(Ksp)极小的难溶性盐,会使弱酸根离子(如S²⁻、CO₃²⁻、F⁻)浓度急剧降低,促使弱酸不断电离出H⁺,从而生成强酸。
例1:H₂S与CuSO₄反应
H₂S+CuSO₄=CuS↓+H₂SO₄
H₂S是极弱的酸(Ka1很小),H₂SO₄是强酸。这个反应能够向右进行,其根本动力是生成了溶解度极低的CuS沉淀(Ksp=6.3×10⁻³⁶)。
由于CuS沉淀的生成,极大地降低了溶液中Cu²⁺和S²⁻的离子浓度,使得平衡强烈向右移动,从而“迫使”弱酸H₂S不断电离出H⁺和S²⁻,S²⁻又与Cu²⁺结合,最终生成了强酸。
例2:H₂S与Pb(NO₃)₂反应
H₂S+Pb(NO₃)₂=PbS↓+2HNO₃
与上面反应类似,PbS的溶度积极小(Ksp≈9.0×10⁻²⁹),Pb²⁺能与H₂S电离出的S²⁻结合生成难溶沉淀,促使H₂S持续电离出H⁺,最终与NO₃⁻形成强酸HNO₃。
二、通过生成挥发性气体实现反应,其核心是气体逸出降低离子浓度。
当弱酸或中强酸与强酸盐反应时,若能生成易挥发性强的酸气体,加热条件下气体逸出会降低产物离子浓度,推动平衡正向进行,从而获得强酸。
例3:H₃PO₄与NaCl加热反应
H₃PO₄(浓)+NaCl(s)=NaH₂PO₄+HCl↑(加热)
H₃PO₄是中强酸(酸性H₃PO₄<HCl),是“相对弱酸”;NaCl与浓磷酸混合时可提供Cl⁻。产物HCl是挥发性强酸,加热时HCl气体不断逸出,导致溶液中Cl⁻浓度显著降低。
勒夏特列原理推动H₃PO₄的电离平衡(H₃PO₄⇌H⁺+H₂PO₄⁻)正向移动,H⁺持续生成并与Cl⁻结合为HCl逸出,最终制得HCl。
实现反应的关键条件:
①必须用浓磷酸,提供高浓度H⁺;若用稀磷酸,H⁺浓度不足;
②必须用固体NaCl,避免提供的Cl⁻浓度过低,抑制HCl逸出;
③必须加热,促进HCl挥发,常温下反应进行很缓慢;
④产物是NaH₂PO₄(H₃PO₄分步电离,第一步电离最强,难以进一步生成Na₂HPO₄或 Na₃PO₄)。
三、通过强氧化剂、还原剂参与实现反应,其核心是电子转移驱动反应。
若弱酸(或其对应酸根)具有强还原性,且与强氧化性物质反应时,氧化还原反应的自发性(电极电势差足够大)会打破“强酸制弱酸”规律,通过电子转移生成强酸。
例4:H₂SO₃与Cl₂水反应
H₂SO₃+Cl₂+H₂O=H₂SO₄+2HCl
H₂SO₃的Ka₁≈1.3×10⁻²、Ka₂≈6.3×10⁻⁸,其酸根SO₃²⁻具有强还原性;Cl₂是强氧化剂(电极电势φ(Cl₂/Cl⁻)=1.36V),氧化性远强于SO₄²⁻(φ(SO₄²⁻/SO₃²⁻)=0.17V),能将SO₃²⁻中S的+4价氧化为+6价的SO₄²⁻,自身被还原为Cl⁻,生成HCl。
反应的驱动力是氧化还原反应的自发性(电势差足够大),而非复分解的离子浓度变化,最终生成H₂SO₄和HCl。
例5:2H₂SO₃+O₂=2H₂SO₄
四、通过生成稳定配离子实现反应,其核心是配离子降低离子浓度。
当弱酸与路易斯酸反应时,若能生成稳定的配合离子,会降低弱酸根离子浓度,促使弱酸电离出H⁺,从而生成强酸。
例6:HF与BF₃反应生成氟硼酸HBF₄
HF+BF₃=HBF₄
HF是弱酸(Ka≈6.6×10⁻⁴),电离平衡为HF⇌H⁺+F⁻;BF₃是路易斯酸,能接受电子对,与HF电离出的F⁻结合形成稳定的四氟合硼配离子BF₄⁻(配离子稳定常数极大),导致溶液中F⁻浓度急剧降低。根据勒夏特列原理推动HF持续电离出H⁺,生成强酸HBF₄,HBF₄完全电离,酸性与盐酸相当。
五、热分解型(氧化还原反应)
例7:HNO₂热分解
3HNO₂=HNO₃+2NO↑+H₂O(加热)
例8:HClO光分解
2HClO(光照)=2HCl+O₂↑
HNO₂、HClO不稳定,受热或光照通过氧化还原反应分解生成强酸和气体,熵增驱动反应。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。少量、适量、足量和过量,这几个词是化学实验和计算中的核心定量描述,区别主要在于反...
一、基础概念:从 “温度强度” 看五者的核心差异 首先需明确:这五种操作本质都是 “...
【导读】“强酸制弱酸”是复分解反应的常见规律,其本质是强酸电离出的H更易与弱酸根...
在高中化学中,很多同学从初中就学习了复分解反应, 都知道复分解反应中“强酸制弱酸...
1.水银:汞Hg 2.过氧一硫酸:过氧硫酸过硫酸 H 2 SO 5 3.白金:主要成分铂 Pt 4.苯:C...
...