
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
在高中化学中,很多同学从初中就学习了复分解反应,都知道复分解反应中“强酸制弱酸”,也因此经常判断错误,搞不清楚一些反应是否可以自发发生。比如“弱酸制强酸”,这个在一定的条件下也是可以发生的。这就需要我们理解复分解反应的本质,离子之间的有效反应,通过反应使体系中某类离子浓度急剧下降,无元素化合价变化。
所以,“弱酸制强酸”的复分解反应是在特殊条件下,比如生成难溶物、挥发性物质等方式,实现体系中离子浓度大幅降低,从而推动反应发生。
一、在高中化学,常见的“弱酸制强酸”复分解反应有两种场景
1.生成极难溶性盐,降低阳离子浓度
当弱酸与强酸的盐反应时,若能生成溶度积极小的难溶性盐,则盐中的阳离子会与弱酸的阴离子结合,形成几乎不溶于水(甚至不溶于酸)的沉淀,导致阳离子浓度急剧降低,从而推动反应进行,最终生成强酸。
比如,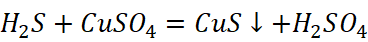
2.利用挥发性差异,生产挥发性强酸
当弱酸(或中强酸)具备“难挥发性”,而目标强酸具备“强挥发性”时,可通过加热+固体反应的条件,使挥发性强酸以气体形式从体系中逸出,降低其离子浓度,从而实现“弱酸制强酸”。
比如,
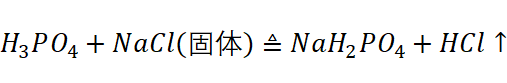
当磷酸与氯化钠按1:1摩尔反应时,生产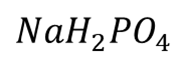 ,
,
当氯化钠过量且温度较高,可生成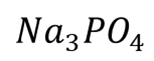 ,但高温磷酸可能部分脱水生成焦磷酸。
,但高温磷酸可能部分脱水生成焦磷酸。
二、在高中化学,常见的“弱酸制强酸”氧化还原反应
1.硫化氢与浓硝酸的反应
硫化氢的还原性与浓硝酸的强氧化性发生反应
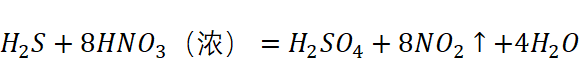
硫化氢为弱酸,生产了强酸硫酸,发生氧化还原反应
2.亚硫酸与氯水
亚硫酸具有还原性,与氯水中的Cl2反应,生产盐酸和硫酸
比如,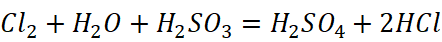
3.氢碘酸与浓硫酸的反应
氢碘酸的强还原性与浓硫酸的强氧化性反应
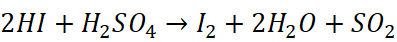
4.浓硝酸的加热分解反应
浓硝酸加热生成二氧化氮,氧气和水
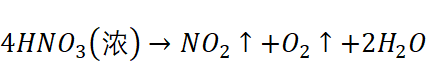
5.次氯酸与氢碘酸的反应
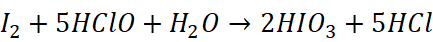
6.草酸与亚硝酸的反应
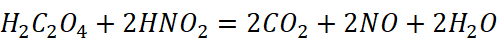
7.亚硫酸与过氧化氢反应
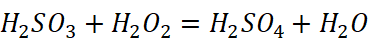
8.氢硫酸与氯气的反应
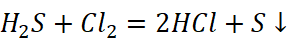
9.氢氰酸与氯水的反应
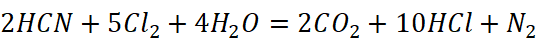
弱酸制强酸的氧化还原反应在高考中并非独立考点,而是结合元素化合物性质、反应规律、方程式书写、计算等核心模块考查。
三、常见的考查方式有:
1.区分“氧化还原型”与“复分解型”弱酸制强酸(高频选择题)
高考常给出反应,要求判断是否为“氧化还原驱动的弱酸制强酸”,关键是对比“常规复分解规律”(强酸制弱酸,无化合价变化)。
判断依据:看反应是否有化合价变化――有则为氧化还原型(不遵循酸性强弱规律),无则为复分解型(必须遵循强酸制弱酸)。
2.反应方程式的书写与配平(必考点,非选择题)
高考常要求书写典型反应的方程式,重点考查产物判断、化合价配平、符号标注(气体↑、沉淀↓、条件)
3.解释“为何能打破强酸制弱酸规律”(非选择题问答)
高考会要求用“氧化还原反应本质”解释此类反应的可行性,核心答法固定:
答题模板:反应物中存在强氧化剂(或强还原剂),通过电子转移(氧化还原反应) 提供了更强的反应驱动力,强制打破了“强酸制弱酸”的复分解规律,最终生成强酸。
4.结合反应判断氧化性/还原性(元素化合物推断题)
此类反应常作为“推断题突破口”,通过“弱酸→强酸”的转化,反推物质的氧化/还原性:
考查逻辑:若弱酸a能反应生成强酸B,且为氧化还原反应,
5.反应现象描述与实验应用(实验题)
高考实验题可能涉及此类反应的“现象观察”或“实际应用”(如除杂、检验)

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。少量、适量、足量和过量,这几个词是化学实验和计算中的核心定量描述,区别主要在于反...
一、基础概念:从 “温度强度” 看五者的核心差异 首先需明确:这五种操作本质都是 “...
【导读】“强酸制弱酸”是复分解反应的常见规律,其本质是强酸电离出的H更易与弱酸根...
在高中化学中,很多同学从初中就学习了复分解反应, 都知道复分解反应中“强酸制弱酸...
1.水银:汞Hg 2.过氧一硫酸:过氧硫酸过硫酸 H 2 SO 5 3.白金:主要成分铂 Pt 4.苯:C...
...