
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
【2025黑吉辽蒙等级考】17. 某实验小组采用如下方案实现了对甲基苯甲酸的绿色制备。
反应:
步骤:
Ⅰ.向反应管中加入0.12g对甲基苯甲醛和1.0mL丙酮,光照,连续监测反应进程。
Ⅱ.5h时,监测结果显示反应基本结束,蒸去溶剂丙酮,加入过量稀NaOH溶液,充分反应后,用乙酸乙酯洗涤,弃去有机层。
Ⅲ.用稀盐酸调节水层pH=1后,再用乙酸乙酯萃取。
Ⅳ.用饱和食盐水洗涤有机层,无水Na2SO4干燥,过滤,蒸去溶剂,得目标产物。
回答下列问题:
(1)相比KMnO4作氧化剂,该制备反应的优点为_______、_______(答出2条即可)。
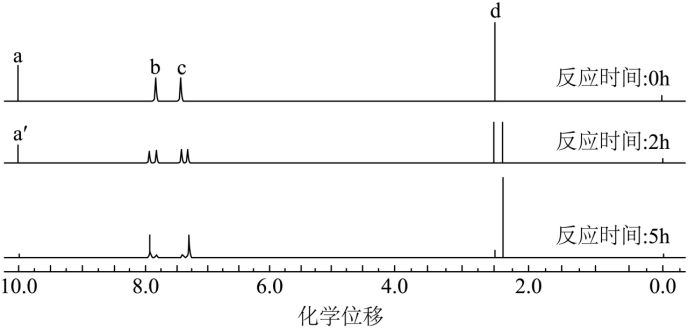
(2)根据反应液的核磁共振氢谱(已去除溶剂H的吸收峰,谱图中无羧基H的吸收峰)监测反应进程如下图。已知峰面积比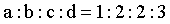 ,
,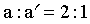 。反应2h时,对甲基苯甲醛转化率约为_______%。
。反应2h时,对甲基苯甲醛转化率约为_______%。
(3)步骤Ⅱ中使用乙酸乙酯洗涤的目的是_______。
(4)步骤Ⅲ中反应的离子方程式为_______、_______。
(5)用同位素示踪法确定产物羧基O的来源。丙酮易挥发,为保证18O2气氛,通18O2前,需先使用“循环冷冻脱气法”排出装置中(空气中和溶剂中)的18O2,操作顺序为:①→②→_______→_______→_______(填标号),重复后四步操作数次。
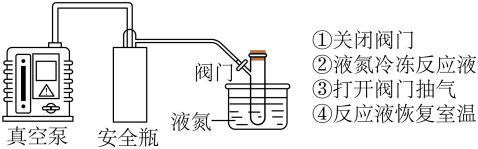
同位素示踪结果如下表所示,则目标产物中羧基O来源于醛基和_______。
反应条件 | 质谱检测目标产物相对分子质量 |
太阳光,18O2,室温,CH3COCH3,5h | 138 |
太阳光,空气,室温,CH3C18OCH3,5h | 136 |
【答案】(1) ①. 绿色环保 ②. 减少副产物的生成
(2)50 (3)除去未反应完的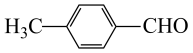
(4) ①.H++OH-=H2O ②. 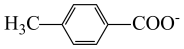 +H+
+H+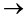
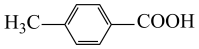
(5) ①. ③ ②. ① ③. ④ ④. 氧气
【解析】
【分析】0.12g对甲基苯甲醛和1.0mL丙酮在有空气存在、光照条件下反应,反应基本结束后,蒸去溶剂丙酮,加入过量稀NaOH溶液,充分反应后,用乙酸乙酯洗涤,弃去有机层,然后用稀盐酸调节水层pH=1后,再用乙酸乙酯萃取,用饱和食盐水洗涤有机层,无水Na2SO4干燥,过滤,蒸去溶剂,得目标产物。
【小问1详解】
KMnO4作氧化剂时可将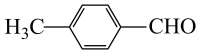 氧化为对苯二甲酸,即有副反应发生,该制备反应在有空气存在、光照条件下发生时,以空气中氧气为氧化剂,既绿色环保,又没有对苯二甲酸生成,所以反应的优点为绿色环保,减少副产物的生成;
氧化为对苯二甲酸,即有副反应发生,该制备反应在有空气存在、光照条件下发生时,以空气中氧气为氧化剂,既绿色环保,又没有对苯二甲酸生成,所以反应的优点为绿色环保,减少副产物的生成;
【小问2详解】
起始0h时只有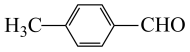 ,5h时只有
,5h时只有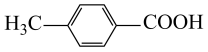 ,
,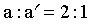 ,则2h时反应液中既有
,则2h时反应液中既有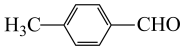 又有
又有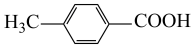 ,且两者物质的量之比为1:1,即对甲基苯甲醛转化率约为50%;
,且两者物质的量之比为1:1,即对甲基苯甲醛转化率约为50%;
【小问3详解】
蒸去溶剂丙酮后,加入过量稀NaOH溶液将对甲基苯甲酸转化为对甲基苯甲酸钠进入水层,则充分反应后,用乙酸乙酯洗涤的目的是除去未反应完的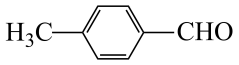 ;
;
【小问4详解】
步骤Ⅱ加入过量稀NaOH溶液将对甲基苯甲酸转化为对甲基苯甲酸钠,步骤Ⅲ中加稀盐酸调节水层pH=1反应的离子方程式为:H++OH-=H2O、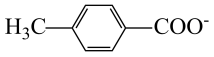 +H+
+H+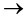
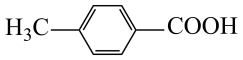 ;
;
【小问5详解】
丙酮易挥发,为保证18O2气氛,通18O2前,需先使用“循环冷冻脱气法”排出装置中(空气中和溶剂中)的16O2,即反应液中有16O2,冷冻可排走一部分溶解的16O2,然后打开阀门抽气,一段时间后,再关闭阀门,待反应液恢复室温后,再冷冻反应液,即“循环冷冻脱气法”,所以操作顺序为:①→②→③→①→④(填标号),重复后四步操作数次;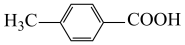 的相对原子质量为136,太阳光,空气,室温,CH3C18OCH3,5h得到的物质相对原子质量为136,为
的相对原子质量为136,太阳光,空气,室温,CH3C18OCH3,5h得到的物质相对原子质量为136,为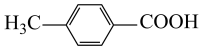 ,而太阳光,18O2,室温,CH3COCH3,5h得到的物质相对原子质量为138,说明目标产物中羧基O来源于醛基和空气中的氧气。
,而太阳光,18O2,室温,CH3COCH3,5h得到的物质相对原子质量为138,说明目标产物中羧基O来源于醛基和空气中的氧气。
【2025黑吉辽蒙等级考】18. 乙二醇是一种重要化工原料,以合成气(CO、H2)为原料合成乙二醇具有重要意义。
Ⅰ.直接合成法:2co(g)+3h2(g) HOCH2CH2OH(g),不同温度下平衡常数如下表所示。
HOCH2CH2OH(g),不同温度下平衡常数如下表所示。
温度 | 298K | 355K | 400K |
平衡常数 | 6.5×104 | 1.0 | 1.3×10-3 |
(1)该反应的ΔH_______0(填“>”或“<”)。
(2)已知CO(g)、H2(g)、HOCH2CH2OH(g)的燃烧热(ΔH)分别为-akJ/mol、-bkJ/mol、-ckJ/mol,则上述合成反应的ΔH=_______kJ/mol(用a、b和c表示)。
(3)实验表明,在500K时,即使压强(34MPa)很高乙二醇产率(7%)也很低,可能的原因是_______(答出1条即可)。
Ⅱ.间接合成法:用合成气和O2制备的DMO合成乙二醇,发生如下3个均放热的连续反应,其中MG生成乙二醇的反应为可逆反应。

(4)在2MPa、Cu/SiO2催化、固定流速条件下,发生上述反应,初始氢酯比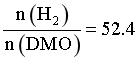 ,出口处检测到DMO的实际转化率及MG、乙二醇、乙醇的选择性随温度的变化曲线如图所示[某物质的选择性
,出口处检测到DMO的实际转化率及MG、乙二醇、乙醇的选择性随温度的变化曲线如图所示[某物质的选择性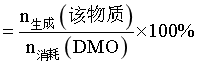 ]。
]。
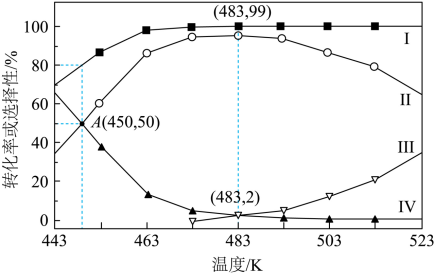
①已知曲线Ⅱ表示乙二醇的选择性,则曲线_______(填图中标号,下同)表示DMO的转化率,曲线_______表示MG的选择性。
②有利于提高A点DMO转化率的措施有_______(填标号)。
A.降低温度 B.增大压强
C.减小初始氢酯比 D.延长原料与催化剂的接触时间
③483K时,出口处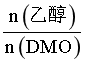 的值为_______(精确至0.01)。
的值为_______(精确至0.01)。
④A点反应MG(g)+2H2(g) HOCH2CH2OH(g)+CH3OH(g)的浓度商Qx=_______(用物质的量分数代替浓度计算,精确至0.001)。
HOCH2CH2OH(g)+CH3OH(g)的浓度商Qx=_______(用物质的量分数代替浓度计算,精确至0.001)。
【答案】(1)< (2)-2a-3b+c(或c-2a-3b)
(3)温度过高,反应平衡常数较小导致产率过低(或温度过高,催化剂的催化活性下降导致产率过低)
(4) ①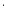 I ②. IV ③. BD ④. 1.98 ⑤. 0.025
I ②. IV ③. BD ④. 1.98 ⑤. 0.025
【解析】
【小问1详解】
根据表格中的数据,反应温度升高反应的平衡常数减小,说明反应向逆反应方向移动,又因升高温度向吸热反应方向移动,故逆反应为吸热反应,正反应为放热反应,该反应的ΔH<0。
【小问2详解】
根据已知条件可以写出如下热化学方程式:
①CO(g)+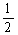 O2(g)=CO2(g) ΔH1=-a kJ・mol-1
O2(g)=CO2(g) ΔH1=-a kJ・mol-1
②H2(g)+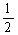 O2(g)=H2O(g) ΔH2=-b kJ・mol-1
O2(g)=H2O(g) ΔH2=-b kJ・mol-1
③HOCH2CH2OH(g)+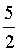 O2(g)=2CO2(g)+3H2O(g) ΔH3=-c kJ・mol-1
O2(g)=2CO2(g)+3H2O(g) ΔH3=-c kJ・mol-1
根据盖斯定律,用反应③减去2倍的反应①和3倍的反应②即可得到目标方程式,故目标方程式的ΔH=(c-2a-3b) kJ・mol-1。
【小问3详解】
根据表格中的平衡常数,反应温度在500K时,平衡常数K<1.3×10-3,此时平衡常数过小,导致乙二醇产率过低;或温度过高,催化剂的催化活性下降,导致乙二醇打标产率过低。
【小问4详解】
根据图示的曲线,随着反应的温度升高I曲线的变化趋势为上升后逐渐平衡,此时说明DMO的转化率区域恒定,故I曲线为DMO的实际转化率曲线;又已知II为乙二醇的选择性曲线,观察曲线II和曲线IV可知,随着反应的进行MG逐渐转化为乙二醇,故曲线IV为MG的选择性曲线,因此曲线III为乙醇的选择性曲线。
①根据上述分析,曲线I为DMO的实际转化率曲线;曲线IV为MG的选择性曲线;
②A.根据图示,降低温度,DMO的转化率降低,A不符合题意;
B.增大压强,反应体系中的活化分子数增加,化学反应速率加快,DMO的转化率增大,B符合题意;
C.减小初始的氢酯比导致体系中氢含量下降,DMO的转化率降低,C不符合题意;
D.A点时DMO的转化率为80%,升高温度后转化率持续上升说明A点时反应未平衡,延长原料和催化剂的反应时间可以促进反应的继续进行,增大DMO的转化率,D符合题意;
故答案选BD;
③483K时,DMO的实际转化率为99%,设起始投入反应的DMO为100mol,则出口出流出的乙醇的物质的量为100mol×99%×2%=1.98mol,此时还有1mol DMO未反应从出口流出,因此出口处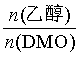 =
=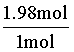 =1.98;
=1.98;
④设初始时H2与DMO的投料分别为52.4mol和1mol,A点时DMO的实际转化率为80%,MG和乙二醇的选择性为50%,假设该反应分步进行,第一步发生DMO转化为MG,可写出如下关系:

第二步反应,MG转化为乙二醇,可写出如下关系:
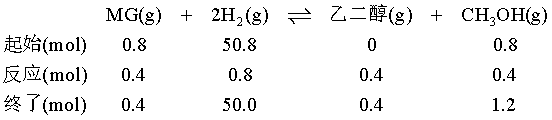
这时,体系中DMO的物质的量为0.2mol、MG的物质的量为0.4mol、H2的物质的量为50.0mol、CH3OH的物质的量为1.2mol、乙二醇的物质的量为0.4mol,体系中总物质的量为0.2+0.4+50.0+1.2+0.4=52.2mol。用物质的量分数代替浓度计算反应的浓度熵Qx=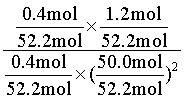 =0.025。
=0.025。
【2025黑吉辽蒙等级考】19. 含呋喃骨架的芳香化合物在环境化学和材料化学领域具有重要价值。一种含呋喃骨架的芳香化合物合成路线如下:
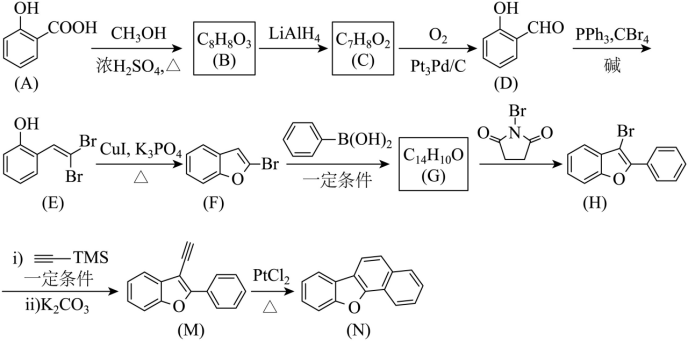
回答下列问题:
(1)A→B的化学方程式为_______。
(2)C→D实现了由_______到_______的转化(填官能团名称)。
(3)G→H的反应类型为_______。
(4)E的同分异构体中,含苯环(不含其他环)且不同化学环境氢原子个数比为3:2:1的同分异构体的数目有_______种。
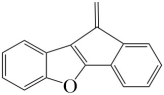
(5)M→N的三键加成反应中,若参与成键的苯环及苯环的反应位置不变,则生成的与N互为同分异构体的副产物结构简式为_______。
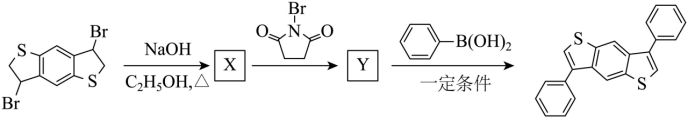
(6)参考上述路线,设计如下转化。X和Y的结构简式分别为_______和_______。
【答案】(1)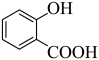 +CH3OH
+CH3OH
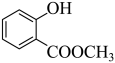 +H2O
+H2O
(2) ①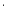 羟基 ②. 醛基
羟基 ②. 醛基
(3)取代反应 (4)4
(5) (6) ①.
(6) ①. 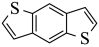 ②.
②. 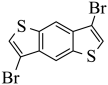
【解析】
【分析】A为邻羟基苯甲酸,与甲醇发生酯化反应生成B(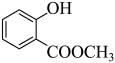 ),
),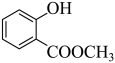 在LiAlH4的作用下,发生还原反应生成C(
在LiAlH4的作用下,发生还原反应生成C(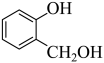 ),C被氧气氧化为D(
),C被氧气氧化为D(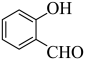 ),D和CBr4反应生成E(
),D和CBr4反应生成E(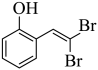 ),E在CuI作用下,生成F(
),E在CuI作用下,生成F(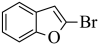 ),F与
),F与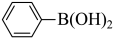 反应生成G,结合H的结构可推出G为
反应生成G,结合H的结构可推出G为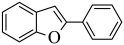 ,G与
,G与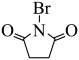 反应生成H,H在一定条件下转化为M(
反应生成H,H在一定条件下转化为M(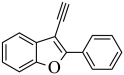 ),M与PtCl2反应生成N(
),M与PtCl2反应生成N(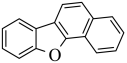 ),据此解答。
),据此解答。
【小问1详解】
由分析可知,A为邻羟基苯甲酸,与甲醇发生酯化反应生成B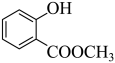 ,化学方程式为
,化学方程式为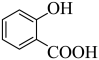 +CH3OH
+CH3OH
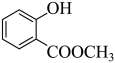 +H2O;
+H2O;
【小问2详解】
由分析可知,C为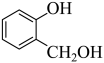 ,C被氧气氧化为D(
,C被氧气氧化为D(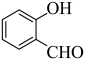 ),羟基转化为醛基,故答案为:羟基;醛基;
),羟基转化为醛基,故答案为:羟基;醛基;
【小问3详解】
G为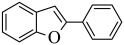 ,与
,与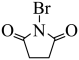 反应生成
反应生成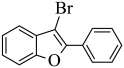 ,属于取代反应的特征,故答案为:取代反应;
,属于取代反应的特征,故答案为:取代反应;
【小问4详解】
E为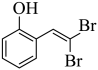 ,含苯环(不含其他环)且不同化学环境氢原子个数比为3:2:1的同分异构体,如果为醛基,溴原子,甲基的组合时,可形成
,含苯环(不含其他环)且不同化学环境氢原子个数比为3:2:1的同分异构体,如果为醛基,溴原子,甲基的组合时,可形成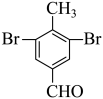
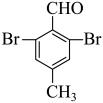 两种,如果为酮碳基,溴原子组合时可形成
两种,如果为酮碳基,溴原子组合时可形成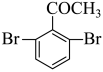
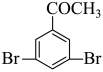 ,一共有4种,故答案为:4;
,一共有4种,故答案为:4;
【小问5详解】
M→N的三键加成反应中,若参与成键的苯环及苯环的反应位置不变,N为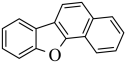 ,可以推断出M中的三键与右侧苯环连接时可以形成N中的六元环或五元环,因此可能的副产物为
,可以推断出M中的三键与右侧苯环连接时可以形成N中的六元环或五元环,因此可能的副产物为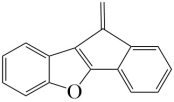 ,故答案为:
,故答案为: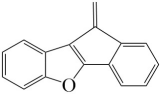 ;
;
【小问6详解】
参考上述路线,可先将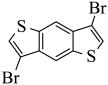 消去生成
消去生成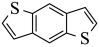 ,
,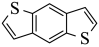 再与
再与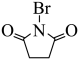 反应生成
反应生成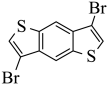 ,
,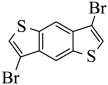 与
与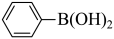 在一定条件下得到目标产物
在一定条件下得到目标产物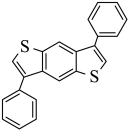 ,故答案为:
,故答案为: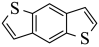 ;
;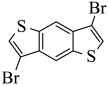 。
。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。一、选择题:本大题共 16 小题,共 44 分。第 1- 题,每小题 2 分;第 11-16 小题,每...
一、选择题:本题共 7 小题,每小题 6 分,共 42 分。在每小题给出的 4 个选项中,只...
一、选择题 ( 本大题共 16 小题,每小题 3 分,共 48 分。每小题列出的四个备选项中只...
1. 定窑是宋代五大名窑之一,其生产的白瓷闻名于世。下列说法正确的是 A. 传统陶瓷是...
可能用到的相对原子质量: H-1 C-12 N-14O-16 Mg-24 S-32 第一部分 本部分共 14 小题...
一位资深的班主任曾说:“家长与学校配合得越好,教育越会成功。我可以非常负责任的说...