
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
原子半径和离子半径(包括阳离子、阴离子)是元素的重要性质,跟元素原子的得失电子能力、元素原子间成键的类型等密切相关。
那么,如何比较原子半径、离子半径的大小呢?
首先我们要明确,原子和离子不像日常生活中所见的篮球、乒乓球那样有一个明确的边界(球皮)。
不论原子半径还是离子半径,都只是人为定义的概念。
从根本上来说,原子和离子是没有边界的,都是若干电子以极高的速度在核外运动时所占据的空间,离核近处电子出现的机会多些,而离核远处电子出现的机会少些,据此人们一般用电子云描述原子的模样。
原子可看作由原子核与核外电子运动所形成的电子云构成,因电子云只是“内密外疏”的“模模糊糊一团”,没有边界,所以严格地说,单独一个原子的半径是无法测定的。
那么原子半径数据是如何取得的呢?
通常所说的“原子半径”是指原子处于某种特定的环境中,如在晶体或与其它原子结合成分子时所表现出的大小。
经常用到的原子半径有三种:共价半径、金属半径和范德华半径。
这些不同类型的原子半径分别是在不同条件下,通过X射线探测到临近原子核间的最小距离后,除以2所得的数据。如下图所示:
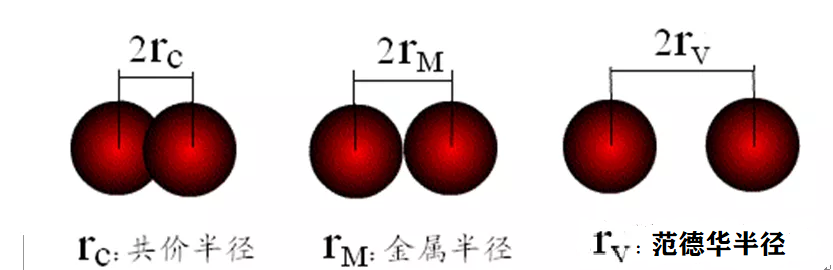
同种元素的两个原子以共价单键连接时,它们核间距离的一半叫做原子的“共价半径”。
如氢分子中两个氢原子核间的距离是74 pm,所以氢原子的共价半径是37pm。
同种元素的共价半径在不同条件下基本不变,如金刚石晶体中C―C键长为154 pm,饱和烃中C-C键长为152~155 pm,故C的共价半径是77 pm。
大多数教科书里提供的非金属元素原子半径的数据都是共价半径。
在金属晶体中,把相邻两个原子核间距离的一半叫做这种元素的金属半径。
在液态和固态的共价分子形成的晶体中,分子和分子之间有一定的吸引力,叫做范德华力。
例如稀有气体的原子,由于它们很难与别的原子结合,故通常通过测定其晶体表面最邻近的2个原子核间距离以确定其原子的大小,最邻近的两个原子核间距离是一半叫范德华半径。
由于稀有气体原子间没有键合作用,结构松散,故范德华半径比一般的共价半径大得多,跟共价半径不具有可比性。
这也是为什么中学教科书里一般不给出稀有气体元素原子半径的原因。
氯元素有共价半径,是99 pm;它也有范德华半径:在C12分子的晶体中,把不属同一分子的两个最接近的原子核间距离的一半称为范德华半径,氯元素原子的范德华半径是180 pm。
显然,同一元素的范德华半径比共价半径要大很多。
离子半径跟原子半径的测定方法相似,也是根据在不同离子化合物中阴阳离子间的距离测算得出的数据。
从理论上讲,决定原子半径或离子半径大小的因素有二:
一是核电荷数,核电荷数越大,则核对核外电子的束缚力越强,核外电子的运动范围越小,于是原子或离子半径越小;
另一因素是核外电子数,核外电子数越多,则其相互之间的排斥力越大,运动时所形成电子云大,则原子或离子半径越大。
有趣的是,对于原子或离子来说,往往是核电荷数越多,则核外电子数也随之增多,这就令我们很难根据原子结构简单地比较不同元素原子半径或离子半径大小。
能不能根据核外电子层数的多少比较元素原子半径或离子半径呢?
答案是否定的。请看实例:
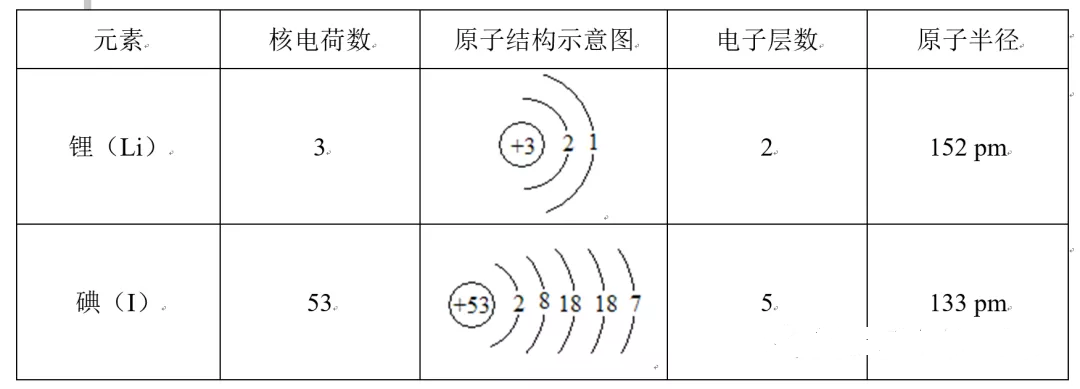
说明:此处Li的半径是金属半径,严格讲不可跟I的共价半径做比较。查Li的共价半径为134 pm,依然大于I的共价半径。
我们看到,核外有5个电子层的碘原子半径竟然比只有2个电子层的锂原子还要小。显然不能依据电子层数多少比较元素的原子半径大小。
幸好我们有元素周期律。元素周期律告诉我们:
① 同一周期元素,从左到右原子半径逐渐减小。
如r(Na)>r(Mg)>r(Al)>……r(Cl)。
② 同一主族元素,原子半径从上到下依次增大。
如r(Na)>r(Li)>r(H);r(I)>r(Br)>r(Cl)。
这样,我们还可以比较周期表内左下方和右上方元素的原子半径。如下图所示的A、B、C、D四种元素:
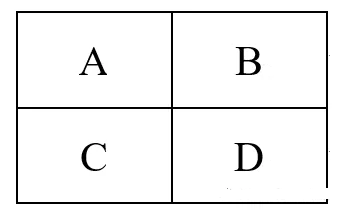
根据元素周期律可判断出:r(C)>r(A)>r(B);r(C)>r(D)>r(B)。
但我们无法比较A与D的原子半径大小。可以说,比较元素原子半径大小的理论依据只有上述①、②两条及由此推演出的“左下>右上”关系,再无别的规律。
同理,比较离子半径大小的一般规律有如下三条:
① 同一元素的阴离子半径 > 原子半径 > 阳离子半径。
如r(H-)>r(H)>r(H+)[价态越高半径越小,如r(Fe3+)<r(Fe2+)];
② 同主族元素的同价态离子,从上到下逐渐增大。
如r(K+)>r(Na+)>r(Li+);r(I-)>r(Br-)>r(Cl-)>r(F-);
③ 电子层结构相同的离子(不管阴离子还是阳离子),随着核电荷数增大,半径减小。例如:
r(N3-)> r(O2-)> r(F-)> r(Na+)>r(Mg2+)> r(Al3+);r(S2-)> r(Cl-)> r(K+)> r(Ca2+)。
对上述第③条我们可做如下理解:
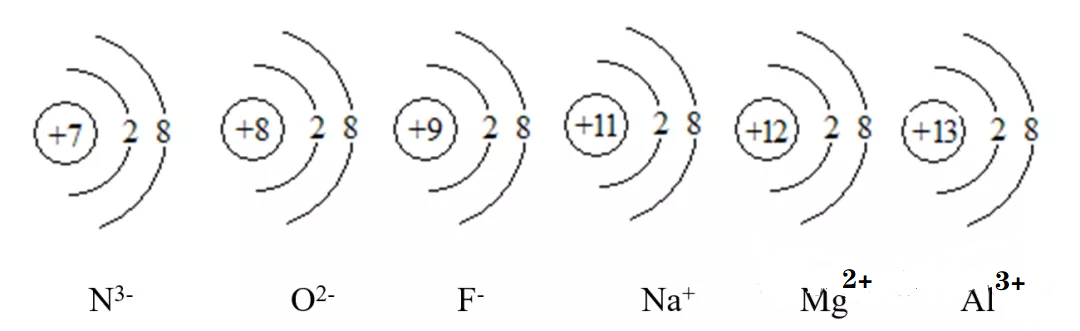
上述6种离子的大小均取决于其核外10个电子的运动范围。
显然,核电荷数越大,则对核外电子的束缚作用越大,电子的运动范围就会越小。故N3- 最大,而Al3+最小。
应该说,在没有数据的情况下比较离子半径大小,除以上规律及由此推演出的规律外,再无别的方法或依据。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
在共价化合物中形成弱极性键或强极性键是由哪些因素来决定的...
1.对角线规则 对比周期系中元素性质,发现: 左上~右下,对角线元...
电子、中子、质子的质量测量是贯穿经典物理到近代物理的重要...
【定义】又称离子有效半径,是通过实验测定的。一般认为的离...
关于117号元素是金属元素还是非金属元素的讨论以下几种意见:...
氢是元素周期表中的第一号元素,元素名来源于希腊文,原意是...