
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、知识梳理
1.当可逆反应达到一种平衡后,若某一时刻外界条件发生改变,都可能使速率—时间图像的曲线出现不连续的情况,根据出现“断点”前后的速率大小,即可对外界条件的变化情况作出判断。如图:
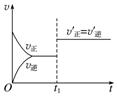
t1时刻改变的条件可能是使用了催化剂或增大压强(仅适用于反应前后气体物质的量不变的反应)。
2.常见含“断点”的速率变化图像分析
图像 |
|
|
|
| |
t1时刻所改变的条件 | 温 度 | 升高 | 降低 | 升高 | 降低 |
正反应为放热的反应 | 正反应为吸热的反应 | ||||
压 强 | 增大 | 减小 | 增大 | 减小 | |
正反应为气体物质的量增大的反应 | 正反应为气体物质的量减小的反应 | ||||
二、例题精讲
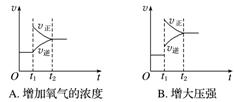
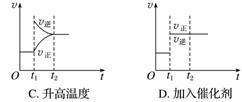
1.(2018·马鞍山二中质检)对于反应2SO2(g)+O2(g) 2SO3(g) ΔH<0已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图像不相符的是(O~t1:v正=v逆;t1时改变条件,t2时重新建立平衡)( )
2SO3(g) ΔH<0已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图像不相符的是(O~t1:v正=v逆;t1时改变条件,t2时重新建立平衡)( )
答案 C
解析 分析时要注意改变条件瞬间v正、v逆的变化。增加O2的浓度,v正增大,v逆瞬间不变,A正确;增大压强,v正、v逆都增大,v正增大的倍数大于v逆,B正确;升高温度,v正、v逆都瞬间增大,C错误;加入催化剂,v正、v逆同时同倍数增大,D正确。
2.(2018·长沙模拟)对于反应:X(g)+Y(g) 2Z(g) ΔH<0的反应,某一时刻改变外界条件,其速率随时间的变化图像如图所示。则下列说法符合该图像的是( )
2Z(g) ΔH<0的反应,某一时刻改变外界条件,其速率随时间的变化图像如图所示。则下列说法符合该图像的是( )
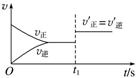
A.t1时刻,增大了X的浓度 B.t1时刻,升高了体系温度
C.t1时刻,降低了体系温度 D.t1时刻,使用了催化剂
答案 D
解析 由图像可知,外界条件同等程度地增大了该反应的正、逆反应速率。增大X的浓度、升高(或降低)体系温度均不会同等程度地改变正、逆反应速率,A、B、C错误;使用催化剂可同等程度地改变正、逆反应速率,D正确。
3.在一密闭容器中发生反应N2+3H2 2NH3 ΔH<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示。
2NH3 ΔH<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示。
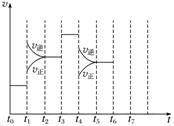
回答下列问题:
(1)处于平衡状态的时间段是________(填字母,下同)。
A.t0~t1 B.t1~t2 C.t2~t3
D.t3~t4 E.t4~t5 F.t5~t6
(2)判断t1、t3、t4时刻分别改变的一个条件。
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
t1时刻________;t3时刻________;t4时刻________。
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是__________。
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
(4)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化曲线。
答案 (1)ACDF (2)C E B (3)A
(4)
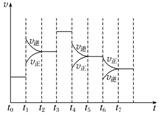
解析 (1)根据图示可知,t0~t1、t2~t3、t3~t4、t5~t6时间段内,v正、v逆相等,反应处于平衡状态。
(2)t1时,v正、v逆同时增大,且v逆增大得更快,平衡向逆反应方向移动,所以t1时改变的条件是升温。t3时,v正、v逆同时增大且增大量相同,平衡不移动,所以t3时改变的条件是加催化剂。t4时,v正、v逆同时减小,但平衡向逆反应方向移动,所以t4时改变的条件是减小压强。
(3)根据图示知,t1~t2、t4~t5时间段内平衡均向逆反应方向移动,NH3的含量均比t0~t1时间段的低,所以t0~t1时间段内NH3的百分含量最高。
(4)t6时刻分离出部分NH3,v逆立刻减小,而v正逐渐减小,在t7时刻二者相等,反应重新达到平衡,据此可画出反应速率的变化曲线。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
...
一、公式提出的背景 19世纪末,化学家们逐渐意识到温度对化学...
假设对于反应 a A(g) + b B(g) g G(g) + h H(g) 中各物质均为理想气体,...
例:某温度、起始压强为100 kPa下,若将2mol SO 2 和1molO 2 ,通入恒...
...
什么是活化能、能垒? 1 、能垒 活化分子含有的能参加化学反应...