
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
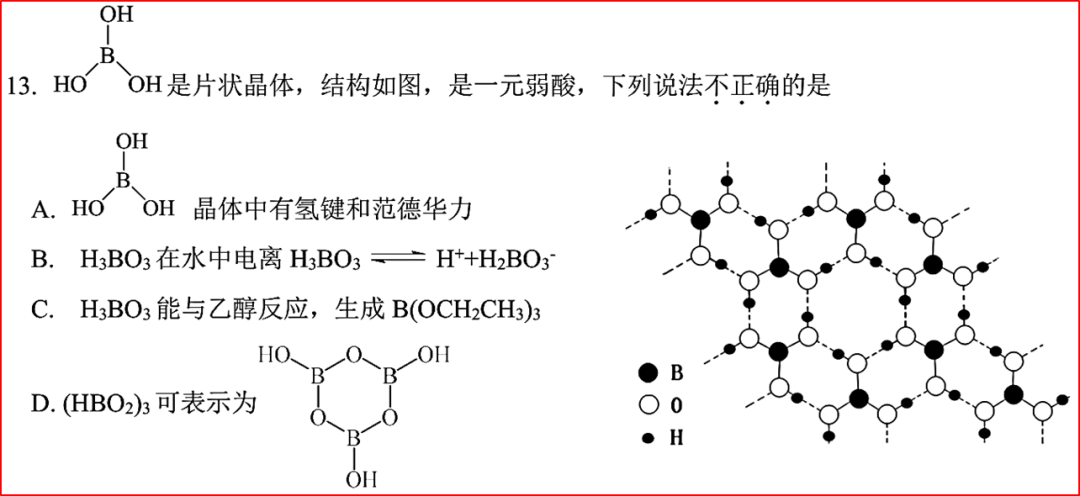
【导读】硼酸是一元酸,根本原因在于其独特的“缺电子”结构和典型路易斯酸性质,它不直接电离出H⁺,而是通过接受水分子中的OH⁻形成配离子[B(OH)₄]⁻,从而释放出一个H⁺,因此只能提供一个可解离的质子。
H₃BO₃+H₂O⇌[B(OH)₄]⁻+H⁺

一、H₃BO₃为什么是一元弱酸?
硼酸分子式B(OH)₃或H₃BO₃,化学式里3个氢原子,但并不是靠直接电离出H⁺来体现酸性的,而是因为其特殊的缺电子结构,遵循的是路易斯酸碱理论。
B(OH)₃结构特征:硼原子最外层只有3个电子,与O形成3个共价键后,中心b原子采用sp²杂化,其价层仍有一个未参与杂化的空P轨道,属于典型的缺电子原子,这个空轨道可以接受电子对,使其成为路易斯酸。
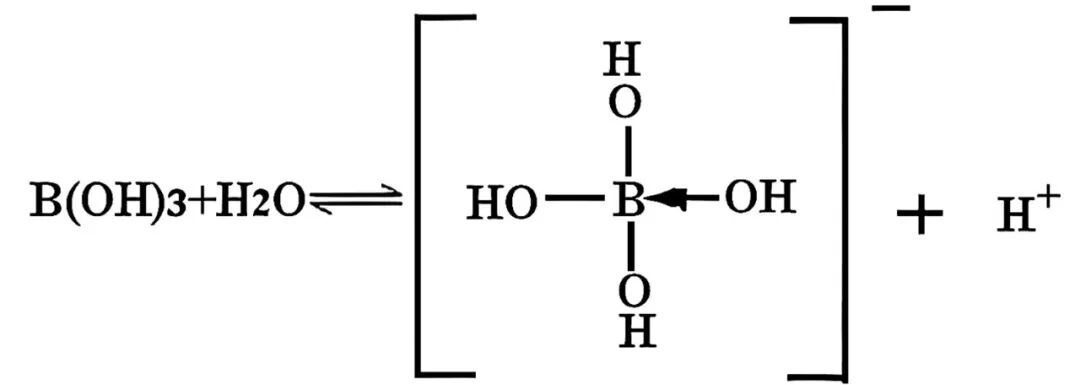
B(OH)₃电离机理:在水中B(OH)₃并不是直接断裂H-O键,而是利用其空轨道接受水分子中OH⁻的孤对电子,形成一个配位键,生成稳定的四面体结构的[B(OH)₄]⁻,同时使H₂O解离出H⁺。
B(OH)₃+H₂O⇌[B(OH)₄]⁻+H⁺
每个硼酸分子只能结合一个OH⁻(受硼原子配位能力限制),只能释放一个H⁺,符合一元酸的定义。其酸性极弱Ka≈5.8×10⁻¹⁰,正是因为这一过程依赖于水的微弱电离。
二、类似H₃BO₃的这类物质都有哪些特点?
这类物质的共同特点:酸的“元数”不由分子中氢原子总数决定,而取决于实际可解离的质子数或通过结合水的H⁺或OH⁻实现电离,导致“元数”与分子式直观氢数不符,打破了“几个H就是几元酸”的直观认知,体现了化学中结构决定性质的核心逻辑。
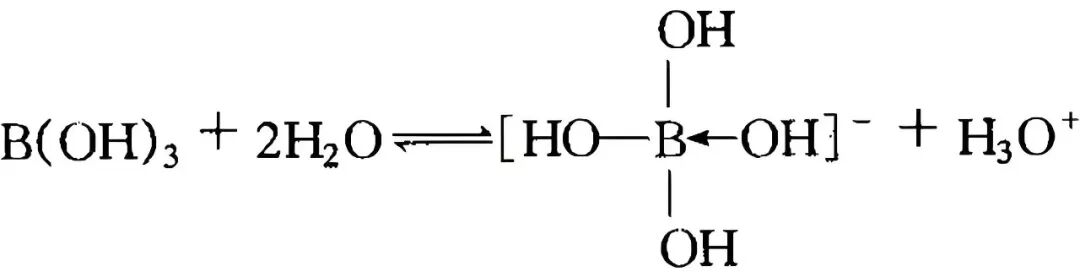
1.酸性类比:接受OH⁻,释放H⁺
Al(OH)₃:酸性时侧表现为路易斯酸,结合水电离的OH⁻,生成[Al(OH)₄]⁻,仅释放1个H⁺,Al和b是同一族,类似硼酸,为一元酸,表现出弱酸性,但通常归为两性氢氧化物而非典型酸。
Al(OH)₃+H₂O⇌[Al(OH)₄]⁻+H⁺
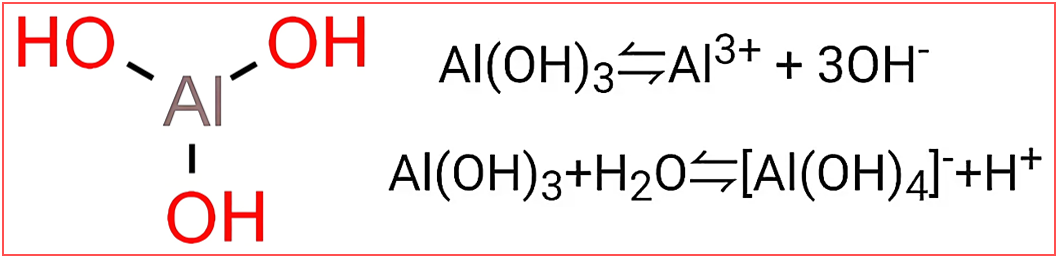
2.碱性类比:接受H⁺,释放OH⁻
NH₃:n(原子含孤电子对),是典型的路易斯碱,可以结合水电离的H⁺生成NH₄⁺,释放OH⁻,为一元弱碱。
NH₃+H₂O⇌NH₃⋅H₂O⇌NH₄⁺+OH⁻
N₂H₄:分步结合H⁺,本质为二元弱碱,但第一步电离主导,常表现为一元碱性质。
第一步:
N₂H₄+H₂O⇌N₂H₅⁺+OH⁻
第二步:
N₂H₅⁺+H₂O⇌N₂H₆²⁺+OH⁻
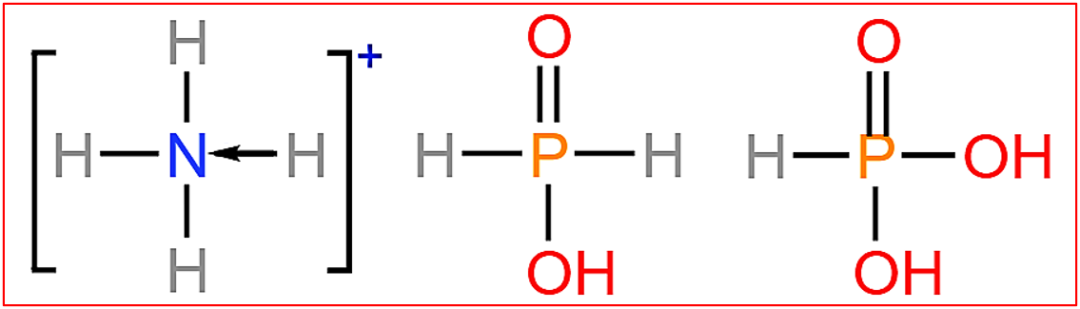
3.磷的含氧酸:结构决定元数,与分子式氢数不符
这类酸中,只有与P相连的-OH才能电离,直接与中心P原子相连的氢无法电离。
次磷酸分子式H₃PO₂,分子式含三个氢,但实为一元酸。结构中只有一个直接连在P上的可电离氢的-OH,其余两个氢直接与磷相连(P-H键),不能解离出H⁺。
H₃PO₂⇌H⁺+H₂PO₂⁻
亚磷酸分子式H₃PO₃,含三个氢,但为二元酸。结构中有一个P-H键和两个-OH基团,只有两个羟基氢能电离。
H₃PO₃⇌H⁺+H₂PO₃⁻
H₂PO₃⁻⇌H⁺+HPO₃²⁻

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
归纳 过二硫酸根 中的过氧键(—O—O—)与过氧化氢结构式(...
电子效应通过改变电子云分布(尤其是化学键的极性、电子离域程...
1、真题呈现: (2023山东--节选)ClO2中心原子为Cl,Cl2O中心原子...
一、螯合物的定义与特点 1. 定义 螯合物是由中心金属离子(或...
一、无机阴离子配体:铜配合物的基础“搭建模块” 无机阴离子...
...