
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
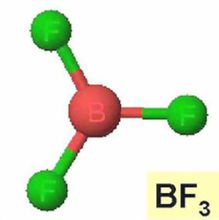
硼的最外电子层电子排布是2s22p1,在与氟形成的三氟化硼(BF3)分子中,B原子的1个2s电子激发到p轨道,以sp2杂化轨道与3个氟原子形成3个σ键。分子具有平面正三角形结构。位于中心的B原子未形成8电子结构,有一个垂直于分子平面p空轨道。3个氟原子中的任一个,都可能提供1个全充满的p轨道,与硼原子的p轨道形成π键。在BF3分子中存在离域π键(π46键)即存在由4p轨道提供的6个电子组成的大π键,它是4个原子共有的共价键。因此,分子中B—F键键长(130pm)短于成键原子的共价半径之和(152pm)。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
归纳 过二硫酸根 中的过氧键(—O—O—)与过氧化氢结构式(...
电子效应通过改变电子云分布(尤其是化学键的极性、电子离域程...
1、真题呈现: (2023山东--节选)ClO2中心原子为Cl,Cl2O中心原子...
一、螯合物的定义与特点 1. 定义 螯合物是由中心金属离子(或...
一、无机阴离子配体:铜配合物的基础“搭建模块” 无机阴离子...
...