
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
酒精和水能以任意比例混溶,这是众所周知的事实,但对此现象的解释,目前仍都是以分子的“相似相溶”原理进行说明。
在水分子中主要由于氧原子外层的六个电子呈sp3不等性杂化以及它的电负性比氢原子大,因而水分子是一个极性分子(a)或(b)。
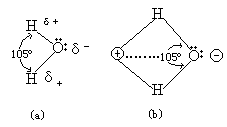
由于极性在水分子之间可由氢键的相互作用而发生缔合现象,成为缔合分子(c)。
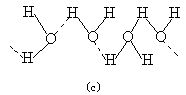
酒精(乙醇)的分子(d)和水分子极为相似,同样具H-O极性键,虽然氧原子的另一个键联结的是烃基,但整个分子也是极性分子。
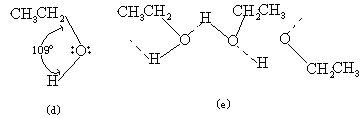
因此,在酒精分子之间同样也存在着缔合现象(e)。如果把酒精和水混在一起,不难理解,由于它们的分子结构相似,分子相互之间也都能发生缔合作用,因此,它们可以任意相互参差结合(f)。表示如下:
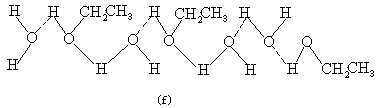
这就是表现出酒精和水不但可以相溶,而且可以任意比例相互混溶。
必须指出,若烃基R-所含碳链较长,则将使得醇分子与水分子的相似性逐渐减少,而不能相溶。根据实验结果,已知只有甲醇、乙醇、丙醇可以和水以任意比例相互混溶,从丁醇起除叔丁醇外,它的水溶性已明显地大为降低。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
把碘液滴加到淀粉当中,它们立刻就会形成墨水般的蓝黑色——...
苯的亲电取代反应定位规则是由许多实验事实中总结出来的经验...
分析:有机化学的学习中,经常用到高锰酸钾溶液。做试剂用时...
原子核外的电子排布,最外层不超过8个,次外层不超过18 个,这...
元素氧化物的水化物M(OH) x 在水溶液中有两种电离的可能性: 到底...
有机物普遍存在同分构现象, 大多数无机物的结构单一,所以无...