
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、注射器的优点:
注射器体积小、操作简便、节省试剂、可靠安全、污染少,广泛用在气体制备、收集,微型实验、家庭小实验等实验中,真正做到了一器多用
1、装置简单 实用性强
分液漏斗在化学实验中的应用比较广泛,用注射器代替分液漏斗,可控制药品的用量,又不会有气体从注射器内逸出;既能达到随时添加试剂的作用,还能起到防止挥发性的药剂因挥发而造成对空气的污染,注射器上标有的刻度能帮助实验者较准确地把握所加试剂的量,同时也解决了部分学校实验室分液漏斗配备不足而实际教学中分液漏斗应用较多的矛盾。用注射器代替分液漏斗,既能进行两种互不相溶的液体的分离,也能和其他仪器一起组装成可添加液体药品的简易装置。
医用注射器还可替代传统反应容器作为液体与液体、液体与固体间不需加热制取气体的发生装置。用注射器作制取气体的发生装置具有安全性高、污染少、操作方便的优点。
2、操作方便 灵活性好
注射器可以用来贮存气体,且可实现制气、贮气、用气一体化。
3、直观准确 有效性高
用医用注射器进行定量实验,操作方便、直观性强。注射器有从1ml到200ml不同的规格,上面标有刻度,带有活塞,能方便吸取和排出液体或气体,且极易控制液体或气体的量。最常见的定量实验应用就是将注射器作为滴管使用,由于其针头细,可控性强,可通过推拉活塞的方法来控制药品的用量,而且用量正确不仅能增强实验的效果,还能起到节约药品的作用。在滴定板上作微量实验时如果将注射器作为滴管使用将更为方便,其效果远远优于普通滴管,同时也避免了使用胶头滴管胶头易老化而需经常更换的问题。医用注射器定量吸取液体或气体的特点,更是超越了滴管只能吸取液体药品的思维定势。
医用注射器能作为气体压缩和抽气装置,应用于气体反应平衡、气体的取样、简易吸滤装置、气态和液态物质微粒间间隔大小的比较等方面,创造性地开展化学实验教学,离不开创造性的实践和探索,让你我共同探索,进一步开发和利用医用注射器简(装置简单)、便(操作方便)、明(现象明显)的独特功能。
二、注射器应用探究
(一)用于抽送气体:
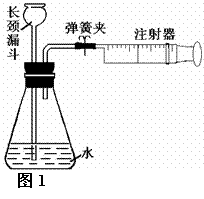
1、检查装置的气密性(如图1)
连接好装置(注射器内留有一半体积的空气),打开弹簧夹,向长颈漏斗中注入水,使其下管口必须液封,慢慢推注射器的活塞,长颈漏斗内形成一段水柱,过一会后水柱的液面不下降。再慢慢往外拉活塞,液柱下降,下管口有气泡冒出。说明装置不漏气。
2、排送气体(如图2)
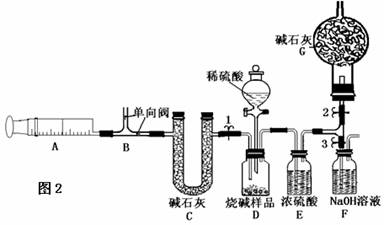
某同学为了测定变质的烧碱样品中Na2CO3的质量分数,设计了图2所示的装置。反应的开始、结束都要用注射器反复的排送气体。实验步骤为:
①检查装置的气密性。
②称取一定质量的干燥的烧碱样品放入广口瓶中,分液漏斗中加入适量的稀硫酸,准确称量装置F的质量,连好装置。
③关闭弹簧夹3,打开弹簧夹1和弹簧夹2。反复推拉注射器。
④关闭弹簧夹1和弹簧夹2,打开弹簧夹3,然后打开分液漏斗的活塞开关,让稀硫酸逐滴滴入样品中,直到不再产生气泡为止。
⑤打开弹簧夹1,立即不断反复推拉注射器。
⑥再称装置F质量,根据CO2的质量来计算样品中Na2CO3的质量分数。
可见:步骤③反复推拉注射器的目的是排尽装置中的CO2,以保证实验结果的准确性。而步骤⑤反复推拉注射器的目的是使生成的CO2充分被F中的试剂吸收。
(二)改变装置内的气体压强(如图3、图4)
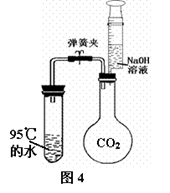
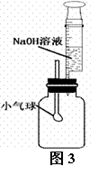
图3中将NaOH溶液注入集气瓶中,振荡,小气球很快膨胀起来。
图4 中打开弹簧夹,将NaOH溶液注入烧瓶中,试管内95℃的水会立即沸腾。(气压减小,沸点降低。)
(三)用于测量气体体积(如图5)
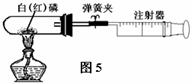
用45
mL试管作反应容器,磷的燃烧均在密闭容器里进行,可防止白烟污染空气。用20 mL注射器(活塞事先处在10
mL刻度处)测量磷燃烧消耗的氧气体积。
操作:①检查装置的气密性。②装药品,连好仪器。③夹紧弹簧夹,加热白磷,观察现象。④燃烧结束,试管冷却后松开弹簧夹,可以看到活塞慢慢左移到1 mL刻度处。说明空气中氧气的体积分数为1/5。[(10 mL~1 mL)/45 mL]。
(四)用于反应容器:(如图6、图7)
图6中用注射器吸收水和CO2(体积比为1:1),然后夹紧弹簧夹,用力振荡,活塞会自动向前推进。说明CO2溶于水后气压减小。
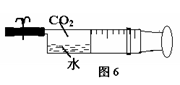
图7将块状固体放入干燥管中,用注射器取一定质量的酸,干燥管上接一个带活塞的导管,就制成了气体发生装置,该装置随时控制反应的进行。可用来制取H2和CO2。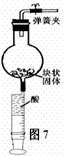
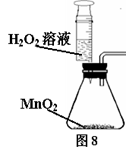
(五)用于分液漏斗、滴管的代用品(如图8)
图8中的注射器代替了分液漏斗,可随时添加药品,不断产生O2。还可控制氧气的生成速率。用注射器,取液、滴加都很方便,也可控制试剂用量和滴速,节省试剂。
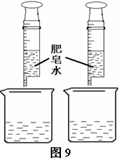
(六)用于量筒(如图9)
由于注射器上有计量单位,可用作一些对比实验的仪器。图9是用肥皂水区分硬水和软水的实验。用注射器取等体积的肥皂水加入盛有等体积硬水和软水的烧杯中,搅拌。操作简便,现象明显。
三、典型例题
【例1】注射器--钠与水反应实验的改进
仪器和药品
废弃的塑料饮料瓶,一次性针筒,100mL量筒,导管、止水夹、大头针等;钠,蒸馏水,酚酞。
实验装置
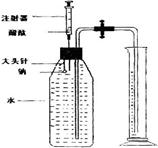
实验步骤
1.如图组装仪器。
2.在塑料瓶中注入蒸馏水至水面与橡胶塞下端相切。取一小块钠,将其插在大头针上,在注射器中吸入1-2mL酚酞。
3.实验时,把止水夹打开,把插有钠和注射器的橡皮塞迅速插入瓶口,并塞紧。钠与水剧烈反应,塑料瓶中的水沿导管流入量筒。
4.反应完毕,将注射器中的酚酞推入塑料瓶,溶液变红。
5.更换50mL注射器,抽取瓶内的气体。抽气后将注射器移进火焰,匀速推出气体,针头处立即燃起细长的火焰。
本实验的特点
本实验改进演示仪器操作简单,安全性强,现象鲜明,且可使学生理解气体压强可将液体从一个容器转移到另一个容器。
【例2】铜与氯气反应实验改进
1、制取氯气
按图1所示安装装置。在试管中加入约0.5克KMnO4固体和3mL浓盐酸,立即塞紧橡皮塞,取100mL注射器,将注射针刺入橡皮塞,缓慢拉动针栓,收集约100mL氯气,将注射针从橡皮塞中拔出,在针尖插上一个小橡皮塞密封。
2、氯气与铜反应操作
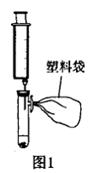
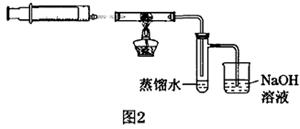
取一支约15×150mm石英玻璃管; 另取约10cm铜导线一根,去掉绝缘皮,将其中的一束细铜丝团成一团,置于石英玻璃管中部。按图2所示安装装置。点燃酒精灯,加热铜丝部位,约1~2分钟后移开酒精灯,迅速拔掉注射器上的橡皮塞,将针尖刺入石英玻璃管的橡皮塞中,将氯气缓缓推入玻璃管中,可观察到:铜丝变成红热状态,玻璃管内产生大量棕黄色的烟。氯气全部推入后,拔出针头,然后用同样的方法,用注射器向玻璃管中快速推入空气,将棕黄色烟赶入盛有少量蒸馏水的具支试管中,轻轻摇动试管使之溶解,溶液呈蓝绿色;缓缓拉动针栓,使少量NaOH溶液吸入具支试管中,有蓝色絮状沉淀产生。
3、说明
1.为防止因塑料袋口扎不严而漏气,可在具支试管的支管上先套上一小段橡胶管,然后把塑料袋口紧扎在上面。
2.具支试管中的导管口不要浸入水中,防止在拉动针栓时倒吸。
3. 不能用铜粉来代替铜丝,防止反应物过热炸裂玻璃管。
4. 利用本装置还可以完成铁与氯气反应等实验。
【例3】全封闭式制取氯气微型实验
实验装置(如图1)
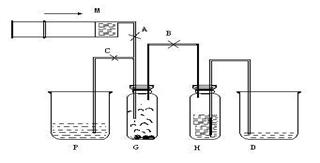
图1
①a、b、c为自由夹;②P为盛有约20ml4mol/LNaOH溶液的50ml烧杯;③G为装有约1gKMnO4固体的青霉素药剂瓶;④H为盛满饱和NaCl溶液的青霉素药剂瓶;⑤D为50ml烧杯;⑥M为盛有约4.5ml12mol/L浓盐酸的10ml注射器;⑦导气管用输液管和12号注射器针头代替。
实验步骤与现象
①如图1所示,打开自由夹a和c,关闭自由夹b,缓缓推动注射器M的活塞,按约1滴/秒的滴加速率逐滴滴入青霉素瓶G中;
②当观察到反应生成的黄绿色氯气充满青霉素药剂瓶G时,打开自由夹b,同时关闭自由夹c;
③此时便观察到氯气将青霉素药剂瓶H中的饱和NaCl溶液压入50ml烧杯D中;
④当观察到青霉素药剂瓶H中的饱和NaCl全部被氯气压出时,关闭自由夹b,同时缓缓回抽注射器M活塞(旨在平衡反应容器青霉素药剂瓶G中的氯气压力)。
⑤制取氯气实验结束时,关闭自由夹a,将注射器M从装有自由夹a的输液管中拔出,换吸约6ml4mol/LNaOH溶液,再按如图1所示使注射器M与装有自由夹a的输液管相连接,关闭自由夹b,打开自由夹a、c,将注射器M中的NaOH溶液一次性注入青霉素药剂瓶G中。
【例4】如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。试回答下列问题:
![]()
实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
1 | 10mL FeSO4溶液 | 10mL NH3 | 生成白色沉淀,后变色 |
2 | 20mL H2S | 10mL SO2 |
|
3 | 30mL NO2(主要) | 10mL H2O( | 剩有无色气体,活塞自动向内压缩 |
4 | 15mL Cl2 | 40mL NH3 |
|
(1)实验1中,沉淀最终变为________色,写出沉淀变色的化学方程式_______________________________。
(2)实验2甲针筒内的现象是:有___________生成,活塞________移动(填向外、向内、不)。反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入___________溶液中。
(3)实验3中,甲中的3mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是_______,写出NO2与H2O反应的化学方程式为_______________________________。
(4)实验4中,已知:3Cl2+2NH3![]() N2+6HCl。甲针筒出活塞有移动,针筒内有白烟产生外,气体的颜色变为____________。最后针筒内剩余气体的体积约为________mL。
N2+6HCl。甲针筒出活塞有移动,针筒内有白烟产生外,气体的颜色变为____________。最后针筒内剩余气体的体积约为________mL。
【解析】:(1)NH3+H2O![]() NH3·H2O,FeSO4+2NH3·H2O===Fe(OH)2↓+(NH4)2SO4,
NH3·H2O,FeSO4+2NH3·H2O===Fe(OH)2↓+(NH4)2SO4,
4Fe(OH)2+O2+2H2O===4Fe(OH)3,Fe(OH)3为红褐色。
(2)H2S+SO2===3S+2H2O,S为黄色固体,反应后针筒内的压强降低,所以针筒内的活塞向内压缩,反应后甲针筒内剩余的少量气体不管是SO2还是H2S或其混合物均可用NaOH溶液吸收。
(3)3NO2+H2O===2NHO3+NO,N2O4![]() 2NO2,所以最后剩余的气体为NO。
2NO2,所以最后剩余的气体为NO。
(4)由方程式可知,随着反应的进行,Cl2的量逐渐减少,最终完全反应。
3Cl2+2NH3===N2+6HCl
15mL 10mL 5mL 30mL
剩余的NH3为30mL,由NH3+HCl===NH4Cl可知,生成的HCl与剩余的NH3恰好完全反应生成NH4Cl,所以最后剩余的气体为5mL。
【答案】(1)红褐色;4Fe(OH)2+O2+2H2O = 4Fe(OH)3↓。
(2)黄色固体;向内;NaOH。
(3)NO;3NO2+H2O=2HNO3+NO。
(4)黄绿色变为无色;5。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
在高中化学实验与物质制备题型中,干燥剂的选择是高频考点,...
高中化学教材实验中多次出现的饱和食盐水 一、氯气的净化除杂...
一、干燥 干燥是除去固体液体或气体中含有的水分或有机溶剂的...
一、乙醇的结构 首先,和水(H-OH)相比,乙醇(CHCH-OH)分子中的...
...
中学化学 实验 中,有许多处都用到饱和溶液,现举例如下。 一...