
|
学习小专题 |

|
学习小专题 |
 [方法与规律j] 盐类水解在解题中的运用 作者:陈博殷 来源:未知 日期:2012-10-24 17:25:23 点击:16623 所属专题:盐类水解应用
[方法与规律j] 盐类水解在解题中的运用 作者:陈博殷 来源:未知 日期:2012-10-24 17:25:23 点击:16623 所属专题:盐类水解应用
一、下列情况要考虑盐类的水解 1. 配制某些盐溶液 [ 例 1] 如何配制澄清透明的 SnCl 2 、 FeCl 3 、 CuSO 4 、 AgNO 3 、 FeSO 4 等溶液? [ 分析 ] 上述盐都能水解,有少量难溶的物质生成,溶液往往浑浊。配制时,应将这些固体溶解在对应的酸里,以抑制水解。如配制 FeSO 4...
 [方法与规律j] 质子平衡式的三种推导方法 作者:刘心宇 来源:未知 日期:2014-03-20 10:43:20 点击:29351 所属专题:质子守恒
[方法与规律j] 质子平衡式的三种推导方法 作者:刘心宇 来源:未知 日期:2014-03-20 10:43:20 点击:29351 所属专题:质子守恒
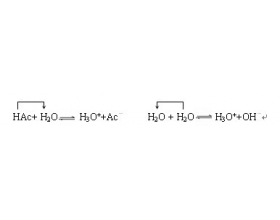
质子平衡式是用物质的量浓度表示得失质子(指氢离子)数相等的方程式。其书写方法有很多,现 有 以下几种比较简便的方法 : 1. 关系式法 关系式法的使用关键是找出溶液中各物质之间的平衡关系,并依据平衡条件,即 碱得到的质子总数 == 酸放出的质子总数 如:醋酸溶液中...
 [方法与规律j] 剖析电解质溶液中微粒关系 作者:陈桂芳 来源:未知 日期:2016-02-02 20:01:27 点击:20706 所属专题:离子浓度大小比较
[方法与规律j] 剖析电解质溶液中微粒关系 作者:陈桂芳 来源:未知 日期:2016-02-02 20:01:27 点击:20706 所属专题:离子浓度大小比较
电解质溶液属于混合体系。因电解质溶液能够发生电离、水解等反应,使得溶液中存在着多种形式的微粒,微粒的浓度也因此而变化。下面是笔者的一些探讨,供参考。 一、守恒关系 (1)电荷守恒:电解质溶液中阳离子所带的正电荷总数等于阴离子所带的负电荷总数。值得注意的...
 [方法与规律j] 一元强酸与一元弱酸比较的几种方法 作者:邵磊 来源:未知 日期:2012-09-22 20:10:10 点击:17732 所属专题:强酸与弱酸比较
[方法与规律j] 一元强酸与一元弱酸比较的几种方法 作者:邵磊 来源:未知 日期:2012-09-22 20:10:10 点击:17732 所属专题:强酸与弱酸比较
在中学化学电解质溶液一章的学习中,常常需要根据一元强酸与一元弱酸的一些性质进行有关的判断和推断。一元强酸与一元弱酸(或一元强碱与一元弱碱)的比较,属于高考的热点,掌握一强一弱的比较方法和技巧,在解题中能达到事半功倍的效果。下面结合自己的教学,谈谈几种比较方...
 [方法与规律j] 快速书写质子守恒的方法 作者:李开振 来源:未知 日期:2016-02-02 20:14:16 点击:28687 所属专题:质子守恒
[方法与规律j] 快速书写质子守恒的方法 作者:李开振 来源:未知 日期:2016-02-02 20:14:16 点击:28687 所属专题:质子守恒
质子守恒就是酸失去的质子和碱得到的质子数目相同,质子守恒和物料守恒,电荷守恒一样同为溶液中的三大守恒关系 电荷守恒 化合物电荷: ⒈ 化合物中元素正负化合价代数和为零 溶液电荷 ⒉ 溶液中所有阳离子所带的正电荷总数等于所有阴离子所带的负电荷总数 例:NaHCO 3 ...
 [方法与规律j] 盐和盐的反应规律 作者:马文礼 来源:未知 日期:2016-02-02 20:18:35 点击:12268 所属专题:双水解反应 酸碱盐
[方法与规律j] 盐和盐的反应规律 作者:马文礼 来源:未知 日期:2016-02-02 20:18:35 点击:12268 所属专题:双水解反应 酸碱盐
由于盐的水解及某些盐具有氧化性,还原性,当盐和盐反应时,有下列四种情况: (1)氧化还原反应 当盐和盐反应时,如果有一种盐是氧化剂,另一种盐是还原剂,则发生的是氧化还原反应,例如: 2FeCl 3 +Na 2 S=2FeCl 2 +2NaCl+S↓ 2FeCl 3 +2KI=2FeCl 2 +2KCl+I 2 (2)...
 [方法与规律j] 一种配平水解反应方程式的简便方法 作者:童建军 来源:未知 日期:2012-05-16 09:38:58 点击:10586 所属专题:盐类水解方程式
[方法与规律j] 一种配平水解反应方程式的简便方法 作者:童建军 来源:未知 日期:2012-05-16 09:38:58 点击:10586 所属专题:盐类水解方程式
对于水解盐间反应式的配平,不少中学生感到困难.这是由于一部分同学对水解原理理解不清,不知写什么,怎么写;另一部分同学虽然理解了水解原理,但方法欠妥,结果反应式没有写对;还有不少同学是模仿分步化学反应方程式的写法,即先写出各种盐的离子水解的反应式,然后将各...
 [方法与规律j] 怎样利用溶度积来判断沉淀的生成和溶解? 作者:李浩 来源:未知 日期:2019-06-11 16:33:00 点击:16058 所属专题:溶度积 沉淀转化
[方法与规律j] 怎样利用溶度积来判断沉淀的生成和溶解? 作者:李浩 来源:未知 日期:2019-06-11 16:33:00 点击:16058 所属专题:溶度积 沉淀转化
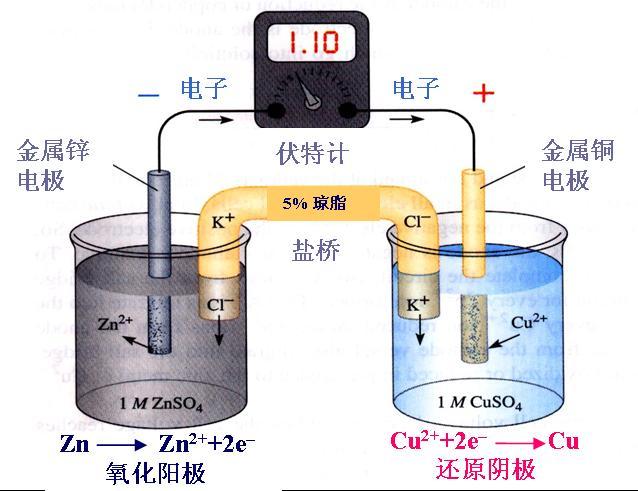
难溶电解质的沉淀和溶解是化学实验和化工生产中经常遇到的过程。例如氯化物在水溶液中同硝酸银反应,生成氯化银沉淀。 NaCl+AgNO 3 ===AgCl↓+NaNO 3 虽然AgCl的溶解度很小,但微溶在水中的AgCl全部电离成Ag + 和Cl - 。在一定温度下,Ag + 和Cl - 与AgCl固体之间,处于...
 [方法与规律j] 常见pH计算的关键 作者:刘玉林 来源:未知 日期:2016-02-02 19:49:28 点击:7207 所属专题:ph计算
[方法与规律j] 常见pH计算的关键 作者:刘玉林 来源:未知 日期:2016-02-02 19:49:28 点击:7207 所属专题:ph计算
一、强酸稀释 关键:必须抓H + ;当酸电离出的H + 很少时,H 2 O的电离不可忽略。 例 1. 将pH=3的盐酸溶液稀释100倍、10 5 倍后其pH各变为多少? 解析: 原溶液中[H+]=1×10 -3 mol/L。 稀释:100倍后,抓H+可知[H + ]=1×10 -3 ÷100=1×10 -5 mol/L,能得出正确结果p...
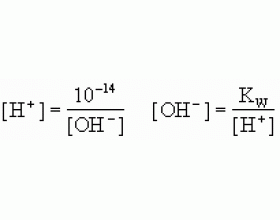 [方法与规律j] 有关pH的计算公式有哪些 作者:单莹 来源:未知 日期:2020-02-28 15:09:32 点击:27004 所属专题:ph计算 计算公式
[方法与规律j] 有关pH的计算公式有哪些 作者:单莹 来源:未知 日期:2020-02-28 15:09:32 点击:27004 所属专题:ph计算 计算公式
(1)pH= -lg[H + ];[H + ]=10 -pH (2)pOH= -lg[OH - ];[OH - ]=10 -pOH (3)K W =[H + ]·[OH - ]=1×10 -14 (4)pH+pOH=14 (5)pH=-lg[H + ]= -lg(m×10 -n )=n-lgm (注意:不指明温度时,温度为常温25℃) 下表是常用到的几个lg值:...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
【导读】化学界的“万能公式”亨德森-哈塞尔巴尔赫方程,就像...
一、先搞懂:Ksp到底是个啥? 很多同学一听到“溶度积常数”就...
在高中化学定量实验与高考考点中,碘量法是氧化还原滴定法里...
一、酸溶液的pH 强酸和弱酸的电离略有不同,下面我们分开阐述...
双指示剂法是一种利用两种具有不同变色范围的酸碱指示剂,在...
弱酸也可以制备强酸!!! 比如向 CuSO 4 溶液中加入 H 2 S 溶液生...
氧化还原滴定法: 1.特点: 氧化还原滴定法在药物分析中应用广...
问题1: 在酸溶液中,H + 和OH - 的来源分别是什么?举例说明...