
|
学习小专题 |

|
学习小专题 |
 [方法与规律j] 溶度积常数的要点及应用 作者:黄元 来源:未知 日期:2014-03-20 20:35:51 点击:2122 所属专题:溶度积
[方法与规律j] 溶度积常数的要点及应用 作者:黄元 来源:未知 日期:2014-03-20 20:35:51 点击:2122 所属专题:溶度积
一、沉淀溶解平衡中的常数( K sp )——溶度积 1. 定义:在一定温度下,难溶电解质的饱和溶液中,存在沉淀溶解平衡,其平衡常数叫做溶度积常数(或溶度积) 2. 表示方法:以M m A n (s) mM n+ (aq) + nA m - (aq)为例(固体物质不列入平衡常数), K sp =[c(M n+ )] m ·...
 [方法与规律j] 溶液中离子浓度大小的比较及其规律与应用 作者:汪谦 来源:未知 日期:2020-03-08 14:17:31 点击:3379 所属专题:离子浓度大小比较
[方法与规律j] 溶液中离子浓度大小的比较及其规律与应用 作者:汪谦 来源:未知 日期:2020-03-08 14:17:31 点击:3379 所属专题:离子浓度大小比较
在判断能水解的盐溶液中的离子浓度大小时,首先要明确盐的电离是强烈的,水解是微弱的,其次还要明确多元弱酸盐的水解是分步进行的,而且第一步是主要的,最后不要忘记水的电离。 电离和水解两个过程产生离子或使离子浓度发生变化,所以离子浓度的比较一般从这两方面着...
 [方法与规律j] 沉淀溶解平衡的应用 作者:陈艳丽 来源:山东省平度市第六中学 日期:2019-04-02 09:22:13 点击:8833 所属专题:溶解平衡 溶度积
[方法与规律j] 沉淀溶解平衡的应用 作者:陈艳丽 来源:山东省平度市第六中学 日期:2019-04-02 09:22:13 点击:8833 所属专题:溶解平衡 溶度积
一、判断离子沉淀的 pH 值 例 1. 一溶液中含有 Fe 3+ 和 Fe 2+ , 它们的浓度都是 0.050mol.L -1 . 如果要求 Fe 3+ 沉淀完全而 Fe 2+ 不生成沉淀 Fe(OH) 2 , 需控制 pH 为何范围已知 : Ksp [Fe(OH) 3 ]=1.1×10 -36 (mol.L -1 ) 4 Ksp[Fe(OH) 2 ]= 1.64×10 -14 (mol.L -...
 [方法与规律j] 弱酸、弱碱的证明方法 作者:吴旭东 来源:未知 日期:2022-02-22 14:52:43 点击:9102 所属专题:弱酸实验判断
[方法与规律j] 弱酸、弱碱的证明方法 作者:吴旭东 来源:未知 日期:2022-02-22 14:52:43 点击:9102 所属专题:弱酸实验判断
一、弱电解质的证明理论依据 弱电解质的证明,是基于与强电解质对比进行的。弱电解质与强电解质最大的区别就是弱电解质存在电离平衡,而强电解质不存在电离平衡。因此,只要证明有电离平衡存在,就证明了弱电解质。 二、弱酸CH 3 COOH的证明方法 1、测定一定浓度的CH 3 ...
 [方法与规律j] 如何计算稀溶液中由水电离出的氢离子浓度或氢氧根离子浓度 作者:张玮 来源:未知 日期:2023-06-27 16:50:02 点击:8048 所属专题:水电离氢离子浓度
[方法与规律j] 如何计算稀溶液中由水电离出的氢离子浓度或氢氧根离子浓度 作者:张玮 来源:未知 日期:2023-06-27 16:50:02 点击:8048 所属专题:水电离氢离子浓度
问题1: 在酸溶液中,H + 和OH - 的来源分别是什么?举例说明怎样计算由水电离产生的 c (OH-)的大小 答 : 在酸溶液中,H + 可看作是全由酸电离的,水电离的氢离子可忽略不计;而OH - 全来源于水电离,即酸溶液中的氢氧根离子全部是由水电离产生的。则: c (OH - )...
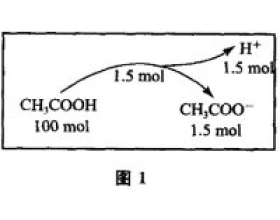 [方法与规律j] 基于模型思想的离子浓度大小比较 作者:邬兆宇 来源:未知 日期:2014-11-24 11:06:28 点击:13552 所属专题:离子浓度大小比较
[方法与规律j] 基于模型思想的离子浓度大小比较 作者:邬兆宇 来源:未知 日期:2014-11-24 11:06:28 点击:13552 所属专题:离子浓度大小比较
人的认识是从感性的直观开始到理性的抽象才能反映客观事物本质的规律性。要反映事物本质的规律性,认识必须超出感性的直观世界,形成相对独立的主观精神世界。这种超越要依靠一种抽象化的能够分开主体与客体的中介物,这个中介物就是模型。在通常情况下,模型分为物质模...
 [方法与规律j] 盐类水解的应用规律 作者:邬兆宇 来源:未知 日期:2013-03-11 10:36:19 点击:5394 所属专题:盐类水解应用
[方法与规律j] 盐类水解的应用规律 作者:邬兆宇 来源:未知 日期:2013-03-11 10:36:19 点击:5394 所属专题:盐类水解应用
盐的离子跟水电离出来的氢离子或氢氧根离子生成弱电解质的反应,称为盐类的水解。 其一般规律是:谁弱谁水解,谁强显谁性;两强不水解,两弱更水解,越弱越水解。 哪么在哪些情况下考虑盐的水解呢? 1.分析判断盐溶液酸碱性时要考虑水解。 2.确定盐溶液中的离子种类和浓度时要考虑...
 [方法与规律j] 由水电离出的氢离子浓度大小与溶液的pH关系的讨论 作者:袁建标 来源:未知 日期:2018-07-19 16:53:56 点击:53197 所属专题:水电离氢离子浓度
[方法与规律j] 由水电离出的氢离子浓度大小与溶液的pH关系的讨论 作者:袁建标 来源:未知 日期:2018-07-19 16:53:56 点击:53197 所属专题:水电离氢离子浓度
怎样理解“由水电离出的氢离子浓度=10 -a mol/L”,这句话能够推出什么,是令许多同学困惑的问题。我认为,主要原因是这是一个逆向思维的问题。由于思维所需要的知识不清楚,所以导致了思维混乱。为了解决这一难题,本文拟做以下尝试。 为了能够解决本文题目提出的问题,...
 [方法与规律j] 酸碱溶液等体积混合后溶液pH的定性分析专题 作者:胡嘉谋 来源:未知 日期:2018-11-28 10:19:38 点击:15102 所属专题:酸碱中和 酸碱性判断
[方法与规律j] 酸碱溶液等体积混合后溶液pH的定性分析专题 作者:胡嘉谋 来源:未知 日期:2018-11-28 10:19:38 点击:15102 所属专题:酸碱中和 酸碱性判断
【问题】 室温时,下列溶液等体积混合后,溶液pH是大于7、小于7、等于7、还是无法判断? ①0.1 mol·L - 1 的盐酸溶液和pH=13的氢氧化钡溶液 ②0.1 mol·L - 1 的硫酸溶液和pH=13的氢氧化钠溶液 ③pH=1的盐酸溶液和0.1 mol·L - 1 的氨水溶液 ④pH=1的硫酸和0.1mol·L -...
 [方法与规律j] 溶液混合与pH判断分析 作者:方丽妹 来源:未知 日期:2016-02-02 19:52:30 点击:9490 所属专题:酸碱中和 酸碱性判断
[方法与规律j] 溶液混合与pH判断分析 作者:方丽妹 来源:未知 日期:2016-02-02 19:52:30 点击:9490 所属专题:酸碱中和 酸碱性判断
溶液混合后,溶液整体的PH如何计算?如何快速判断混合溶液的酸碱性? 教学过程中经常听说:等浓度等体积混合,谁强显谁性;等体积PH之和为14,谁弱显谁性。当然这样的判断方法绝大多数情况下没有大问题,但是细究起来,这种简单的技巧很容易造成判断的失误。 先分析一下...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
【导读】化学界的“万能公式”亨德森-哈塞尔巴尔赫方程,就像...
一、先搞懂:Ksp到底是个啥? 很多同学一听到“溶度积常数”就...
在高中化学定量实验与高考考点中,碘量法是氧化还原滴定法里...
一、酸溶液的pH 强酸和弱酸的电离略有不同,下面我们分开阐述...
双指示剂法是一种利用两种具有不同变色范围的酸碱指示剂,在...
弱酸也可以制备强酸!!! 比如向 CuSO 4 溶液中加入 H 2 S 溶液生...
氧化还原滴定法: 1.特点: 氧化还原滴定法在药物分析中应用广...
问题1: 在酸溶液中,H + 和OH - 的来源分别是什么?举例说明...