
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑i] 范特霍夫方程与阿伦尼乌斯公式在高中化学的作用 作者:化学自习室 来源:未知 日期:2025-08-07 08:19:54 点击:316 所属专题:范特霍夫方程 阿伦尼乌斯公式
[注解与辨疑i] 范特霍夫方程与阿伦尼乌斯公式在高中化学的作用 作者:化学自习室 来源:未知 日期:2025-08-07 08:19:54 点击:316 所属专题:范特霍夫方程 阿伦尼乌斯公式
一、范特霍夫方程:化学反应的“平衡指挥家” 在可逆反应里,化学平衡常数(K)能衡量反应进行的程度。K越大,意味着反应正向进行得越彻底。范特霍夫方程就揭示了K和温度(T)之间的关系,它的核心就是:平衡常数随温度的变化,取决于反应是吸热还是放热。 二、阿伦尼乌...
 [注解与辨疑i] 化学反应平衡常数K值与温度是什么关系? 作者:化学自习室 来源:未知 日期:2025-08-07 07:47:26 点击:358 所属专题:范特霍夫方程
[注解与辨疑i] 化学反应平衡常数K值与温度是什么关系? 作者:化学自习室 来源:未知 日期:2025-08-07 07:47:26 点击:358 所属专题:范特霍夫方程
【导读】范特霍夫方程很好的描述了可逆反应的化学平衡常数(K)与温度(T)的关系,其核心规律:平衡常数随温度的变化取决于反应的热效应(Δ H )。 ①吸热反应(Δ H >0): K随温度升高而增大; ②放热反应(Δ H <0): K随温度升高而减...
 [注解与辨疑i] 能垒与活化能区别 作者:化学自习室 来源:未知 日期:2024-12-24 07:56:27 点击:1109 所属专题:能垒 活化能
[注解与辨疑i] 能垒与活化能区别 作者:化学自习室 来源:未知 日期:2024-12-24 07:56:27 点击:1109 所属专题:能垒 活化能
什么是能垒、活化能?二者有什么区别? 1、能垒 活化分子含有的能参加化学反应的最低限度的能量,称为化学反应的能垒,或称能阈或能障 。对于一个化学反应,要想从反应物变成产物必须要“翻山越岭”。 能垒,则是反应物变成产物所必须克服的能量障碍。能垒的高度表示了...
 [注解与辨疑i] 有关化学反应速率和化学平衡易错点 作者:化学自习室 来源:未知 日期:2024-04-23 08:24:28 点击:574 所属专题:速率与平衡
[注解与辨疑i] 有关化学反应速率和化学平衡易错点 作者:化学自习室 来源:未知 日期:2024-04-23 08:24:28 点击:574 所属专题:速率与平衡
1.无论是用某一反应物表示还是用某一生成物表示,由于Δ C 是取浓度变化的绝对值,因此,其化学反应速率都取正值,且是某一段时间内的平均速率。 2.化学反应速率可用反应体系中一种反应物或生成物浓度的变化来表示,一般是以最容易测定的一种物质表示,书写时应标明是什么物...
 [注解与辨疑i] 碰撞理论、过渡态理论简介 作者:徐全勇 来源:未知 日期:2023-09-19 15:41:54 点击:538 所属专题:有效碰撞 过渡态理论
[注解与辨疑i] 碰撞理论、过渡态理论简介 作者:徐全勇 来源:未知 日期:2023-09-19 15:41:54 点击:538 所属专题:有效碰撞 过渡态理论
...
 [注解与辨疑i] 阿伦尼乌斯公式与活化能、速率方程 作者:化学自习室 来源:未知 日期:2023-09-14 10:03:32 点击:1303 所属专题:阿伦尼乌斯公式 活化能 速率方程
[注解与辨疑i] 阿伦尼乌斯公式与活化能、速率方程 作者:化学自习室 来源:未知 日期:2023-09-14 10:03:32 点击:1303 所属专题:阿伦尼乌斯公式 活化能 速率方程
本题考查了阿伦尼乌斯公式中温度和速率常数的关系,即温度升高,速率常数变大。 本题考查了阿伦尼乌斯公式中活化能大小决定了温度对速率影响程度的关系,即活化能越大,温度对反应速率的影响程度越大。 本题依据平行反应活化能的不同,通过调控温度来不同程度改变平行反...
 [注解与辨疑i] 高考化学阿伦尼乌斯公式及应用 作者:化学自习室 来源:未知 日期:2023-09-14 10:17:18 点击:1222 所属专题:阿伦尼乌斯公式
[注解与辨疑i] 高考化学阿伦尼乌斯公式及应用 作者:化学自习室 来源:未知 日期:2023-09-14 10:17:18 点击:1222 所属专题:阿伦尼乌斯公式
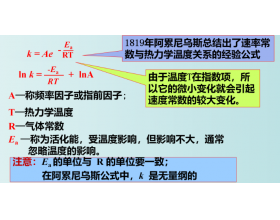
一、人物简介: 阿伦尼乌斯·斯万特·奥古斯特(1859年2月19日~1927年10月2日)瑞典物理化学家,他奠定了物理化学的基础,主要贡献为:提出电离理论学说和阿伦尼乌斯方程,1903年获得诺贝化学奖。 二、阿伦尼乌斯方程 1889年,在大量实验结果的基础上,阿伦尼乌斯提出了...
 [注解与辨疑i] 工业生产中适宜生产条件的选择原则 作者:化学自习室 来源:未知 日期:2023-05-16 11:15:02 点击:547 所属专题:工业条件选择
[注解与辨疑i] 工业生产中适宜生产条件的选择原则 作者:化学自习室 来源:未知 日期:2023-05-16 11:15:02 点击:547 所属专题:工业条件选择
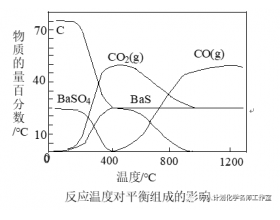
工业生产中适宜生产条件的选择原则 : (1)从化学反应速率分析:既不能过快,也不能太慢 (2)从化学平衡移动分析:既要注意外界条件对速率和平衡影响的一致性,又要注意两者影响的矛盾性。 (3)从原料的利用率分析:增加易得廉价原料,提高高价原料的利用率。 (4)...
 [注解与辨疑i] 工业合成氨的两个问题答疑 作者:化学自习室 来源:未知 日期:2023-04-28 11:02:14 点击:1695 所属专题:合成氨
[注解与辨疑i] 工业合成氨的两个问题答疑 作者:化学自习室 来源:未知 日期:2023-04-28 11:02:14 点击:1695 所属专题:合成氨
问题一:根据合成氨的反应方程式, N 2 和 H 2 物质的量之比为 1 ﹕ 3 ,但实际生产中, N 2 和 H 2 物质的量之比为 1 ﹕ 2. 8 ,即 N 2 过量,原因是什么? 分析:工业合成氨时,使用的是铁催化剂,反应历程如下图所示: 从图中可知,工业合成氨是多步进行的反应,其中...
 [注解与辨疑i] 对化学反应自发性理解的思考 作者:王鹏飞 来源:化学读思教 日期:2022-12-12 10:28:05 点击:970 所属专题:自发反应
[注解与辨疑i] 对化学反应自发性理解的思考 作者:王鹏飞 来源:化学读思教 日期:2022-12-12 10:28:05 点击:970 所属专题:自发反应
作者:汉中市陕飞二中 723213 王鹏飞 摘要:本文对“自发”主要从社会学、化学教材和自然科学谈了对化学反应自发性理解的思考,得出“化学反应自发性的自由能判据必须是在恒温恒压条件下且不做非体积功时进行的化学反应”的重要结论。 关键词:化学自发性焓判据熵判据自由能...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。一、范特霍夫方程:化学反应的“平衡指挥家” 在可逆反应里,化学平衡常数(K)能衡量...
什么是能垒、活化能?二者有什么区别? 1、能垒 活化分子含有的能参加化学反应的最低...
1.无论是用某一反应物表示还是用某一生成物表示,由于Δ C 是取浓度变化的绝对值,因...
在一个恒温恒容的密闭容器里,充入2mol SO 2 和1mol O 2 ,发生如下反应并建立化学平...
...
一、人物简介: 阿伦尼乌斯·斯万特·奥古斯特(1859年2月19日~1927年10月2日)瑞典物...
本题考查了阿伦尼乌斯公式中温度和速率常数的关系,即温度升高,速率常数变大。 本题...
工业生产中适宜生产条件的选择原则 : (1)从化学反应速率分析:既不能过快,也不能...