
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
技巧点拨
一、常见气体的检验原则
1.实验现象明显;
2.可操作性强、操作简单;
3.环保、成本低。
【答题模板】
操作和试剂[将气体通入×××溶液或把×××试纸靠近集气瓶口(或伸入集气瓶内)等]→现象(可观察到×××现象)→ 结论(说明该气体为×××或含有×××气体)
【关键警示】
(1)答题关键词:将气体通入,加入试剂、现象、结论。
(2)答题步骤:①将气体通入某种溶液;②根据性质选择合适的试剂;③准确完整地描述反应现象;④根据现象得出结论或判断。
二、常见气体的检验方法
1.酸性气体的检验

2.碱性气体的检验(NH3)

3.还原性气体的检验

4.强氧化性气体的检验
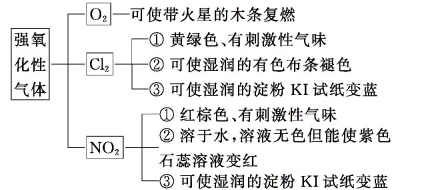
5.混合气体检测规范表述举例
①检验碳与浓硫酸反应的产物的方法
【规范表达】气流通过试剂的先后顺序以及作用分别是:
无水硫酸铜→品红溶液→酸性KMnO4溶液或溴水→品红溶液→澄清石灰水
检验H2O 检验SO2 除去SO2 检验SO2已经除尽 检验CO2
②实验室证明一氧化碳能还原氧化铜并检验产物二氧化碳的实验设计
【规范表达】CO气体依次通过的实验装置以及各装置的作用如下:
硬质玻璃管(盛CuO、加热)→澄清石灰水→NaOH溶液→燃着的酒精灯
主反应装置 检验CO2 除去CO2 消除CO的污染
注意:(1)点燃酒精灯之前一定要检验CO的纯度。
(2)先通一氧化碳驱除装置中的空气后再点燃主反应装置的酒精灯。
(3)停止加热硬质玻璃管后要继续通入CO直至玻璃管冷却。
(4)NaOH溶液的作用是除去气体中的二氧化碳便于尾气燃烧。
(5)实验现象:硬质玻璃管中的黑色粉末变为红色固体,澄清石灰水变浑浊。
典题精析
【典例】(2019·重庆模拟改编)某兴趣小组的同学在学习浓硫酸性质时,发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体。他们对气体的成分很感兴趣,有的同学认为气体只含有SO2,也有的同学认为还应该含有H2;请你帮他们设计实验验证所产生的气体的成分__________。
【标准答案】
将气体先通入含有少量酸性KMnO4的溶液,若观察到溶液褪色,说明有SO2。
再通入含有过量KMnO4的溶液,最后用试管收集气体,若KMnO4溶液的颜色不变,试管中收集到气体,则气体为SO2、H2的混合物。
强化训练
1.(2019·石家庄模拟)实验室用草酸与浓硫酸反应制备CO,其原理如下:H2C2O4![]() CO↑+CO2↑+H2O。某课题组同学设计实验探究CO还原氧化铅(黄色粉末)并检验氧化产物(已知CO能使银氨溶液产生黑色沉淀),装置如图所示。
CO↑+CO2↑+H2O。某课题组同学设计实验探究CO还原氧化铅(黄色粉末)并检验氧化产物(已知CO能使银氨溶液产生黑色沉淀),装置如图所示。
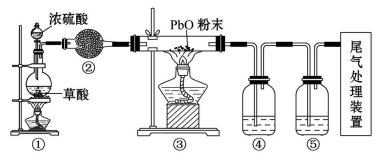
下列说法正确的是 ( )
A.②、④、⑤中试剂依次为碱石灰、银氨溶液、澄清石灰水
B.实验时,先点燃①处酒精灯,⑤中连续产生气泡且有明显现象后点燃③处酒精灯
C.实验结束时,先熄灭①处酒精灯,再熄灭③处酒精灯
D.实验过程中观察到③玻璃管中黄色粉末逐渐变成白色粉末
【解析】选B。先检验CO2,后检验未完全反应的CO,试剂顺序为碱石灰、澄清石灰水、银氨溶液,A项错误;⑤中连续产生气泡,银氨溶液中产生黑色沉淀,表明装置内空气排尽,B项正确;类似一氧化碳还原氧化铜,先停止加热,继续通入气体,应先熄灭③处酒精灯,再熄灭①处酒精灯,C项错误;铅粉末是黑色粉末,不是白色粉末,D项错误。
2.(2019·成都模拟)下列关于硫化氢的说法错误的是 ( )
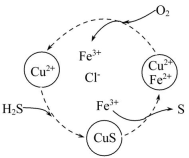
A.H2S是一种弱电解质
B.可用石灰乳吸收H2S气体
C.根据如图可知FeCl3、CuCl2均能氧化H2S
D.H2S在空气中燃烧可以生成SO2
【解析】选C。H2S溶于水形成氢硫酸,为弱酸,能用石灰乳(碱性)吸收,A、b项正确;C项,Cu2+与H2S生成CuS沉淀,是非氧化还原反应,不能氧化H2S,错误;D项,H2S在空气中充分燃烧可生成SO2:2H2S+3O2![]() 2SO2+2H2O(若不充分燃烧可生成S:2H2S+O2
2SO2+2H2O(若不充分燃烧可生成S:2H2S+O2![]() 2H2O+2S↓),正确。
2H2O+2S↓),正确。
3.为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,某化学小组开展如下探究:
【查阅资料】2KNO3![]() 2KNO2+O2↑
2KNO2+O2↑
Fe(NO3)2![]() FexOy+NO2↑+O2↑
FexOy+NO2↑+O2↑
实验一:探究Fe(NO3)2热分解固体产物中铁元素的价态。
实验二:探究Fe(NO3)2热分解气体产物的性质。
该组同学进行了如下实验,请完成实验空缺部分内容。限选试剂和用品:浓硫酸、4mol·L-1NaOH溶液、0.1mol·L-1BaCl2溶液、带火星的木条、0.1mol·L-1酸性KMnO4溶液、蒸馏水。
实验步骤 | 预期现象和结论 |
步骤1:取少量Fe(NO3)2固体于试管中,加热分解 | ________,说明分解产生的气体中含有NO2 |
步骤2:将产生的气体依次通过盛有足量_______、浓硫酸的洗气瓶,______在最后一个出口检验 | ____________,说明分解产生的气体中含O2 |
【解析】Fe(NO3)2受热分解产生的气体产物中,NO2是红棕色气体,O2是无色气体,有红棕色气体产生,就能说明分解产物中含有NO2,由于NO2有毒,且易与水反应生成能与O2反应的NO,因此步骤2中应该先将多余的NO2用NaOH溶液吸收,再用浓硫酸干燥,在最后一个出气口用带火星的木条检验,若带火星木条复燃,说明分解产生的气体中含有O2。
答案:有红棕色气体产生(其他合理表述也可)
4 mol·L-1NaOH溶液 用带火星的木条 带火星的木条复燃
【加固训练】
某无色混合气体中可能含有乙烯、二氧化碳、二氧化硫和氧气,为确定其中一定含有二氧化碳、二氧化硫,甲、乙两位同学分别设计了下述实验方案,并都认为:如果观察到的现象与自己设计的方案一样,就可确认无色气体中一定含有二氧化碳和二氧化硫。
(1)方案甲:
混合气体→溴水褪色→澄清石灰水变浑浊
(2)方案乙:
混合气体→足量品红溶液
颜色变浅→澄清石灰水变浑浊
试用简要语言评价上述各实验方案是否严密?并说明原因。
(1)方案甲:______________;
(2)方案乙:______________。
【解析】因混合气体中可能含C2H4、CO2、SO2、O2,当混合气体通过酸性高锰酸钾溶液和溴水而分别使之褪色时,可能是C2H4,也可能是SO2反应引起的,不能确定一定含SO2,因此甲方案设计不严密。而上述混合气体中能使品红溶液褪色的只有SO2,且品红溶液颜色变浅而不是褪色,说明SO2完全被吸收,再使澄清的石灰水变浑浊,说明一定含有CO2。
答案:(1)不严密,有乙烯的干扰
(2)严密,上述气体中只有SO2能使品红溶液褪色,通过足量品红溶液后,除去二氧化硫,剩余气体能使澄清石灰水变浑浊,则一定有CO2存在。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
...
1.测溶液pH的操作 用玻璃棒(干燥洁净)取少量待测液点在干燥的...
在近几年的高考化学试题中,开放性、探究性的实验试题逐渐成...
1.亚氯酸钠(NaClO 2 )是一种高效含氯消毒剂和漂白剂,主要用于...
一、解题要点: 1、防氧化:排尽装置中的空气,避免易还原性...
化学的实验基本操作一直以来都是高考的重点,看似简单,但回...