
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
在有机化学实验中,“试剂添加顺序”从来不是随便规定的“仪式感”,而是兼顾安全、产率和实验效果的核心细节。其中,制备硝基苯时“先加浓硝酸→再加浓硫酸→最后加苯”的顺序,更是高中化学和基础有机实验的高频考点,也是很多人容易记混、踩坑的地方。
看似简单的三步添加,背后藏着明确的化学原理和安全逻辑——错一步可能引发危险,还会导致实验失败、产物不纯。今天就用通俗的语言,把这个“顺序密码”彻底讲明白,不管是备考还是做实验,都能轻松掌握。
先搞懂核心:制备硝基苯的反应本质
首先我们要明确,制备硝基苯的核心反应是 苯的硝化反应:苯(C₆H₆)与浓硝酸(HNO₃)在浓硫酸(H₂SO₄)的催化下,在50~60℃水浴加热条件下,发生取代反应,生成硝基苯(C₆H₅NO₂)和水。反应方程式如下:
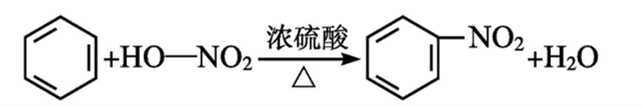
这里要注意两个关键:一是浓硫酸的作用不只是“脱水剂”,更重要的是与浓硝酸反应生成 硝酰正离子(NO₂⁺)——这才是真正能进攻苯环、引发反应的“关键试剂”;二是整个反应放热,且试剂本身具有强腐蚀性、挥发性,因此添加顺序必须围绕“控温、防危险、提产率”展开。
第一步:先加浓硝酸——为后续反应打基础
为什么要先加浓硝酸?其实很简单:浓硝酸是本次硝化反应的“硝基来源”,先将它加入容器,相当于为后续反应“铺好底色”。
从实验逻辑来看,后续要加入的浓硫酸密度比浓硝酸大,若先加浓硫酸,再倒密度更小的浓硝酸,硝酸会浮在浓硫酸表面;而浓硫酸溶于水(浓硝酸中含有一定水分)会释放大量热量,热量无法及时扩散,会导致硝酸剧烈挥发甚至分解,不仅浪费试剂,还可能产生有毒气体,带来安全隐患。
简单说:先加浓硝酸,是为了给后续加入的浓硫酸“留足扩散空间”,避免一开始就出现局部过热、试剂飞溅的危险。
第二步:再加浓硫酸——控温+生成“反应关键物”
这一步是整个顺序的“核心关键”,也是最容易出错的地方——很多人会疑惑,为什么不能先加苯,或者把浓硫酸和浓硝酸一起倒进去?
答案很明确:这一步的核心目的,是 安全配制“混酸”,并生成硝酰正离子(NO₂⁺),同时严格控制温度。
1. 安全角度:浓硫酸密度(1.84g/cm³)远大于浓硝酸(1.50g/cm³),将浓硫酸缓慢加入浓硝酸中,并用玻璃棒不断搅拌,浓硫酸会因密度大而缓慢下沉,过程中释放的热量能均匀扩散,避免局部过热导致液体飞溅。这和我们稀释浓硫酸时“先加水、后加浓硫酸”的原理完全一致——都是为了防止密度小的液体浮在表面,被浓硫酸溶解时的热量灼伤。
2. 反应角度:浓硫酸不仅是催化剂,还能与浓硝酸发生反应,促使硝酸离解,生成硝酰正离子(NO₂⁺),反应可简单表示为:HNO₃ + H₂SO₄ → NO₂⁺ + HSO₄⁻ + H₂O。这个硝酰正离子是进攻苯环的“核心试剂”,只有先配好混酸、生成足够的硝酰正离子,后续加入苯才能顺利发生反应。
特别提醒:加入浓硫酸时,一定要缓慢滴加、不断搅拌,最好将容器放在冷水浴中冷却,防止温度过高(超过60℃)引发副反应——比如生成二硝基苯等杂质,降低硝基苯的产率。
第三步:最后加苯——防挥发+控反应速率
混酸配制完成、冷却至室温后,再缓慢滴加苯,这一步的目的的是 减少苯的挥发,控制反应速率,避免副反应发生。
1. 减少挥发:苯的沸点较低(80.1℃),且具有挥发性,若先加苯,后续加入浓硫酸时释放的大量热量,会导致苯快速挥发,不仅浪费试剂,还会因苯的浓度不足,影响反应进行。
2. 控制反应:苯的硝化反应是放热反应,若将苯加入到已经冷却的混酸中,能避免反应放热过于剧烈——如果苯和混酸同时混合,大量热量瞬间释放,会导致反应失控,生成过多副产物(如二硝基苯),甚至引发危险。
另外,苯的密度(0.88g/cm³)比混酸小,加入后会浮在混酸表面,通过不断搅拌,能让苯与混酸充分接触,保证反应均匀进行,提高硝基苯的产率。
易错点提醒:这3个错误千万别犯!
很多人记混顺序,本质是没理解背后的逻辑,这里总结3个高频错误,帮你避开坑:
错误1:先加浓硫酸,再加浓硝酸——浓硫酸密度大,硝酸浮在表面,放热导致硝酸挥发、分解,易飞溅伤人;
错误2:先加苯,再加混酸——苯挥发严重,且混酸加入时放热,会导致反应失控,副产物增多;
错误3:三者同时加入——试剂混合瞬间释放大量热量,不仅有安全隐患,还会导致反应混乱,几乎得不到纯净的硝基苯。
总结:记住“顺序”,更要记住“逻辑”
其实制备硝基苯的试剂添加顺序,核心逻辑就3点:
1.控温防危险:利用密度差异,让浓硫酸缓慢下沉,避免局部过热、液体飞溅;
2.提产率:先配混酸生成关键试剂(硝酰正离子),再加苯避免挥发和副反应;
3.易记忆:可以简化为“先硝后硫再加苯,控温搅拌记在心”。
最后补充一个小细节:硝基苯有毒,实验时一定要在通风橱中进行,若不慎溅到皮肤上,先用酒精擦拭,再用肥皂水清洗;反应完成后,需将混合物倒入水中,通过分液分离出硝基苯(下层油状液体),再经过洗涤、干燥、蒸馏,得到纯净的硝基苯。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
在有机化学实验中,“试剂添加顺序”从来不是随便规定的“仪...
正确示意图: 审题 注意1:醇发生消去反应的条件——浓硫酸、...
审题注意1:卤代烃消去反应的条件——“氢氧化钠醇溶液、加热...
一、实验装置图及原理 主反应: 副反应: CaS+2H 2 O==Ca(OH) 2 +...
1.加热浓硫酸与乙醇的混合物制乙烯时,混合液为什么会变黑且...
1.用电石制取乙炔的实验中,为什么要用饱和食盐水替代纯水?...