
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑j] 弱电解质电离度α与电离平衡常数K的关系 作者:陈丽娟 来源:未知 日期:2016-02-02 20:00:27 点击:17991 所属专题:电离度 电离平衡常数
[注解与辨疑j] 弱电解质电离度α与电离平衡常数K的关系 作者:陈丽娟 来源:未知 日期:2016-02-02 20:00:27 点击:17991 所属专题:电离度 电离平衡常数
问题:醋酸在水中电离后的电离平衡常数为K,加入盐酸,氢离子浓度增加了,醋酸电离平衡逆向移动,使得醋酸电离程度改变,但是为什么加入盐酸前后醋酸的电离平衡常数不变?电离平衡常数不是表示电离程度吗? 分析: 1、逆向移动使得醋酸电离程度改变 这句话是对的 因为电...
 [注解与辨疑j] 水的电离方程式所蕴含的几组关系 作者:陈博殷 来源:未知 日期:2016-02-02 20:07:49 点击:6238 所属专题:水的电离
[注解与辨疑j] 水的电离方程式所蕴含的几组关系 作者:陈博殷 来源:未知 日期:2016-02-02 20:07:49 点击:6238 所属专题:水的电离
水是一种极弱的电解质,能够发生微弱的电离,存在着电离平衡。在一定温度下,[H + ]与[OH - ]的乘积是一个常数,即[H + ][OH - ]=KW,KW叫做水的离子积常数,简称水的离子积。 通过水的电离方程式,可以发现它蕴含了如下几组关系,在我们教学和学习中,都至关重要。现...
 [注解与辨疑j] 稀释有利于水解,亦有利于电离 作者:邱东兰 来源:未知 日期:2016-02-02 20:11:42 点击:11504 所属专题:溶液稀释 盐类水解规律 电离平衡
[注解与辨疑j] 稀释有利于水解,亦有利于电离 作者:邱东兰 来源:未知 日期:2016-02-02 20:11:42 点击:11504 所属专题:溶液稀释 盐类水解规律 电离平衡
为什么 弱电解质溶液加水冲稀 电离平衡右移? 1.在其他条件不变的情况下,向一定浓度的弱电解质溶液中加水,由于水分子数增多,使得弱电解质电离的离子之间的距离增大,离子间相互碰撞结合成分子的机会减小,单位时间内离子间的有效碰撞次数减少。另外,弱电解质分子由于...
 [注解与辨疑j] 如何理解电解质、非电解质、强电解质、弱电解质的概念及其导电性 作者:李小明 来源:未知 日期:2018-07-19 16:02:37 点击:26404 所属专题:电解质 弱电解质 导电性
[注解与辨疑j] 如何理解电解质、非电解质、强电解质、弱电解质的概念及其导电性 作者:李小明 来源:未知 日期:2018-07-19 16:02:37 点击:26404 所属专题:电解质 弱电解质 导电性
一、相关概念: 1.电解质和非电解质:溶于水或熔化状态下能导电的化合物叫电解质。溶于水或熔化状态下不能导电的化合物叫做非电解质。 2.强电解质和弱电解质:在水溶液里能够完全电离的电解质叫强电解质。如强酸、强碱、大多数盐类、金属氧化物等。在水溶液里不能完全电...
 [注解与辨疑j] 谈谈盐类水解离子方程式的书写与应用 作者:栾春武 来源:未知 日期:2019-06-28 18:38:53 点击:19894 所属专题:盐类水解方程式 盐类水解应用
[注解与辨疑j] 谈谈盐类水解离子方程式的书写与应用 作者:栾春武 来源:未知 日期:2019-06-28 18:38:53 点击:19894 所属专题:盐类水解方程式 盐类水解应用
一、盐类水解方程式的书写一般要注意一下几点: (1)一般来说盐类水解的程度不大,是中和反应的逆反应,由于中和反应趋于完成,所以盐类的水解反应是微弱的,盐类水解的离子方程式一般不写“ === ”,而是写“ ”。由于盐类的水解程度一般都很小,通常不生成沉淀和气体...
 [注解与辨疑j] 弱碱阳离子与弱酸根不能大量共存? 作者:邱东兰 来源:未知 日期:2012-05-28 18:40:22 点击:4019 所属专题:离子共存 双水解反应
[注解与辨疑j] 弱碱阳离子与弱酸根不能大量共存? 作者:邱东兰 来源:未知 日期:2012-05-28 18:40:22 点击:4019 所属专题:离子共存 双水解反应
弱碱阳离子与弱酸很能不能大量共存,不能一概而论。而在中学不少资料上的离子能否共存习题中都认为:弱碱阳离子与弱酸根不能大量共存,这是错误的。如醋酸铵、碳酸氢铵等就是弱碱阳离子与弱酸根可以大量共存的例子。而有些弱碱阳离子与弱酸根互促水解程度大,甚至生成沉淀或...
 [注解与辨疑j] 盐类水解反应的离子方程式书写 作者:刘玉林 来源:未知 日期:2012-05-16 15:11:42 点击:15329 所属专题:盐类水解方程式
[注解与辨疑j] 盐类水解反应的离子方程式书写 作者:刘玉林 来源:未知 日期:2012-05-16 15:11:42 点击:15329 所属专题:盐类水解方程式
正确书写盐类水解反应的离子方程式之一 书写盐类水解的反应的离子方程式的关键是写出弱酸根阴离子或不活泼金属阳离子(包括铵离子)与水反应生成相应弱酸或弱碱的反应式.书写盐类水解反应的离子方程式应注意以下几点: (1)写盐类水解的离子方程式时,应遵循书写离子方程...
 [注解与辨疑j] 盐类的水解反应进行的程度 作者:刘明 来源:未知 日期:2016-02-02 20:16:49 点击:8314 所属专题:盐类水解规律
[注解与辨疑j] 盐类的水解反应进行的程度 作者:刘明 来源:未知 日期:2016-02-02 20:16:49 点击:8314 所属专题:盐类水解规律
酸碱中和和盐类水解在一定条件下互为可逆,构成矛盾的两个方面,这对矛盾有时这方面成为主要方面,有时候另一方面成为矛盾的主要方面.如何正确理解中和反应和盐类的水解反应的进行程度问题?现分以下几类情况来谈. (1)盐类的水解进行的程度很小:由于中和反应有极弱...
 [注解与辨疑j] 由于双水解在溶液中不能大量共存的离子组总结 作者:张澳 来源:未知 日期:2016-02-02 20:17:51 点击:7647 所属专题:双水解反应 离子共存
[注解与辨疑j] 由于双水解在溶液中不能大量共存的离子组总结 作者:张澳 来源:未知 日期:2016-02-02 20:17:51 点击:7647 所属专题:双水解反应 离子共存
弱酸根离子与弱碱阳离子在水溶液中 不能 大量 共存 的情况常见的有:...
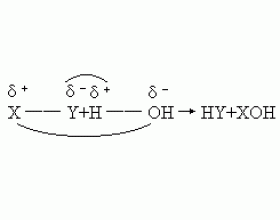 [有机化学] 水解反应面面观 作者:周广 来源:未知 日期:2016-01-08 22:24:24 点击:11586 所属专题:水解反应 有机反应
[有机化学] 水解反应面面观 作者:周广 来源:未知 日期:2016-01-08 22:24:24 点击:11586 所属专题:水解反应 有机反应
所谓水解反应,即物质跟水发生的相互变换成分的反应.用通式可表示为: 反应的机理可简单地认为是:共价键(X―Y键、H―O键)断裂(一般地,一个水分于中只有一个H―O键断裂),再按异电相吸原则,重新组合成新键即得产物.至于离子键则视为共价键的极限情形.各类水解...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。【学生疑问】 教材上有两个实验,一个是 AgI 转化为 Ag 2 S,一个是 Mg(OH) 2 转化为 ...
25 ℃ 时, K a1 (H 2 S)=1.1 × 10 -7 ; K a2 (H 2 S)=1.3 × 10 -13 . (高等教育...
沉淀转化是沉淀溶解平衡的应用之一。 对于溶度积较大的沉淀转为溶度积较小的沉淀这类...
1.实例 常温下,用0.100 0 mol・L -1 NaOH溶液滴定20.00 mL 0.100 0 mol・L -1 CH 3...
问题呈现:pH=5的稀盐酸加水冲稀1000倍,稀释后溶液的pH=?请通过计算说明。 错解:由...
多元弱酸是分步电离的,且以第一步电离为主,各级电离常数逐级减少,且相差很大。 对...
过渡金属具有多变的氧化数,因为次外层d电子可以部分或者全部参与成键,因此它们能形...
问:为什么强酸在冰醋酸中可以比较出其酸性强弱? 想要回答这个问题,还是得回到酸电...