
|
ѧϰСר�� |

|
ѧϰСר�� |
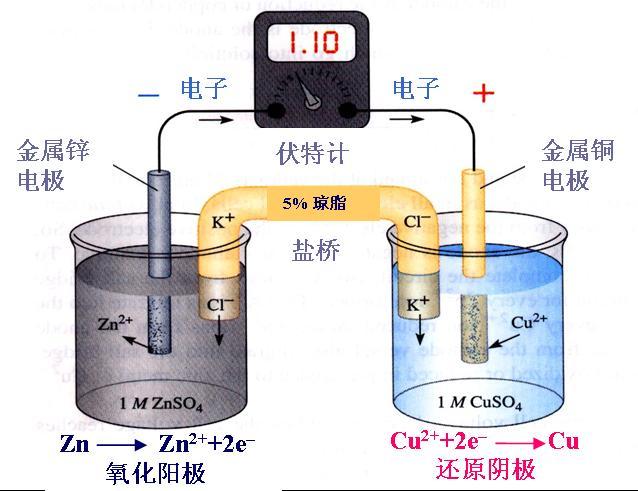 [ע�������j] ���ε�ˮ�ⷴӦ---���ҡ����ȡ���ȫ ����:������ ��Դ:δ֪ ���ڣ�2016-03-22 14:58:46 �����1192 ����ר�⣺����ˮ�ⷴӦ
[ע�������j] ���ε�ˮ�ⷴӦ---���ҡ����ȡ���ȫ ����:������ ��Դ:δ֪ ���ڣ�2016-03-22 14:58:46 �����1192 ����ר�⣺����ˮ�ⷴӦ
�˽�������ˮ�⣬����Ҫ�����������ˮ�⣡ ���䣺�����ˮ�⣭����ˮ��Һ��ε��������������ˮ������������γ�������ʵķ�Ӧ���ص����������桢���ȡ�ǰ������������ˮ�У�������������ӡ� �������ˮ�����ܷ������ҡ���ȫ�����ȵ�һ������������...
 [ע�������j] �������ӳ���PHֵ ����:��Ƽ ��Դ:δ֪ ���ڣ�2019-05-23 10:36:24 �����15117 ����ר�⣺���������� �������ӳ���phֵ ������������
[ע�������j] �������ӳ���PHֵ ����:��Ƽ ��Դ:δ֪ ���ڣ�2019-05-23 10:36:24 �����15117 ����ר�⣺���������� �������ӳ���phֵ ������������
�������ӳ���PHֵ����(20��) ��������Ũ�� 10^-1 10^-2 10^-3 10^-4 10^-5 pKsp In 3.27 3.6 3.93 4.26 4.59 33.2 Sn(��������) 0.57 1.07 1.57 2.07 2.57 27.8 Sn(�ļ�����) 0.25 0.5 0.75 1 1.25 56 Cd 7.7 8.2 8.7 9.2 9.7 13.6 Pb(��������) 7.04 7.54 8.04 8.54 9....
 [ע�������j] ˮ��Һ�еĸ�������ƽ�ⳣ���뻯ѧƽ�ⳣ���Ĺ�ϵ ����:���� ��Դ:δ֪ ���ڣ�2021-01-20 09:11:17 �����6693 ����ר�⣺��ѧƽ�ⳣ�� ƽ�ⳣ��
[ע�������j] ˮ��Һ�еĸ�������ƽ�ⳣ���뻯ѧƽ�ⳣ���Ĺ�ϵ ����:���� ��Դ:δ֪ ���ڣ�2021-01-20 09:11:17 �����6693 ����ר�⣺��ѧƽ�ⳣ�� ƽ�ⳣ��
��ˮ��Һ�г�������ƽ�ⳣ������ K w �� K a �� K b �� K sp �� K h �ȣ����Ƿֱ����ʲô��˼������֮����ʲô��ϵ���������ڽ����Щ��ѧ���⣿�뿴���·����� ��䲻�����ڣ�ˮ��Һ�еĸ�������ƽ�ⶼ��ѭ��ѧƽ����ص㣬���ϸ���ƽ�ⳣ���뻯ѧƽ�ⳣ���������Ե�...
 [ע�������j] ˮ��Һ�е�����ƽ���е��״��ж� ����:���� ��Դ:δ֪ ���ڣ�2016-02-02 18:10:26 �����1110 ����ר�⣺�������Һ �Ƿ��ж�
[ע�������j] ˮ��Һ�е�����ƽ���е��״��ж� ����:���� ��Դ:δ֪ ���ڣ�2016-02-02 18:10:26 �����1110 ����ר�⣺�������Һ �Ƿ��ж�
�� ��1.ij��Һ��ֻ���� NH 4 �� ��Cl �� ��H �� ��OH �� ���� c ( NH 4 �� )= c (Cl �� )������Һ��pH=7 �� ��2. �����£�ij���ʵ���Һ��pH7���������һ��������Һ��ǿ����������Һ �� ��3. �����£���ˮ�м����ƻ��������ƶ���ʹˮ�ĵ���ƽ�������ƶ���ˮ�����ӻ���...
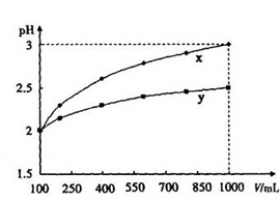 [ע�������j] ����ʹ���Ŀ������ ����:���� ��Դ:δ֪ ���ڣ�2016-02-02 18:13:37 �����4179 ����ר�⣺ǿ��������Ƚ�
[ע�������j] ����ʹ���Ŀ������ ����:���� ��Դ:δ֪ ���ڣ�2016-02-02 18:13:37 �����4179 ����ר�⣺ǿ��������Ƚ�
ǿ�� ��� �ʵĵ����� ���� ��ѧ ���ص���ѵ㣬Ҳ�� �߿� �� �ȵ� ������ʹ�����ΪһԪǿ���һԪ����Ĵ������� ���ʵ��� Ũ�ȵĴ�...
 [ע�������j] ����к͵ζ���ϸ���� ����:��Ө ��Դ:δ֪ ���ڣ�2014-04-23 10:10:31 �����27973 ����ר�⣺�к͵ζ�
[ע�������j] ����к͵ζ���ϸ���� ����:��Ө ��Դ:δ֪ ���ڣ�2014-04-23 10:10:31 �����27973 ����ר�⣺�к͵ζ�
һ������к͵ζ�����Ҫ�����ǵζ�ǰ�����͵ζ��������裺 (1)�ζ�ǰ������©��ϴ�ӡ���ϴ��עҺ����Һ������ �ٲ�©�����ζ����Ƿ�©Һ����ϴ�ӣ���ˮ������ˮ�ֱ�ϴ�ӵζ��ܡ���Һ�ܡ���ƿ������ϴ����ʢװ�ζ��ܺ���Һ�ܣ���ƿ������ʢװҺ��ϴ����עҺ��...
 [ע�������j] ̼����ˮ������������ܽ� ����:������ ��Դ:δ֪ ���ڣ�2016-02-02 18:16:23 �����20187 ����ר�⣺̼���� ����ˮ��Ӧ��
[ע�������j] ̼����ˮ������������ܽ� ����:������ ��Դ:δ֪ ���ڣ�2016-02-02 18:16:23 �����20187 ����ר�⣺̼���� ����ˮ��Ӧ��
һ��̼����ˮ�ⷽ��ʽ ̼����ˮ��Һ�лᷢ��ˮ�ⷴӦ�����ӷ�Ӧ����ʽ���£� C O 3 2 �� ��H 2 O �PHC O 3 �� ��OH - HC O 3 �� �� H 2 O�P H 2 CO 3 ��OH - ����̼����ˮ����� (1)�ζ�Ӧ����(���)Խ����ˮ��̶�Խ����Һ����(������)Խǿ�� �磺��ͬ�����£���Ũ��...
 [ע�������j] �����ܽ�ƽ���ѵ�ͻ�� ����:��ζ� ��Դ:δ֪ ���ڣ�2014-04-03 15:23:17 �����2927 ����ר�⣺�ܽ�ƽ��
[ע�������j] �����ܽ�ƽ���ѵ�ͻ�� ����:��ζ� ��Դ:δ֪ ���ڣ�2014-04-03 15:23:17 �����2927 ����ר�⣺�ܽ�ƽ��
�ܽ�ƽ�⼰�ܽ�ƽ�ⳣ�� ��һ���¶������ܵ���ʾ������ܽ�����Һ�е�����֮������ܽ�ͽᾧ��ƽ�⣬������������ƽ�⣬Ҳ��Ϊ�����ܽ�ƽ�⡣ ��AgClΪ��������AgCl��ˮ���ܽ�Ⱥ�С������������ȫ���ܽ⡣ �ӹ����ܽ�ƽ��Ƕ���ʶ��AgCl����Һ�д��������������̣� ����ˮ...
 [ע�������3] �ܽ�̶ȵ��ж� ����:���� ��Դ:δ֪ ���ڣ�2014-03-31 15:40:20 �����1933 ����ר�⣺�ܽ���
[ע�������3] �ܽ�̶ȵ��ж� ����:���� ��Դ:δ֪ ���ڣ�2014-03-31 15:40:20 �����1933 ����ר�⣺�ܽ���
�ܽ��� �ܽ�� ���ܣ��������ܻ��ܣ� 0.01 �� �� 0.01g= �� 1 �� ���� 1g= ���� 10 �� ���� = 10 �� ������������� �ܽ�������...
 [ע�������j] �������Һϡ��ʱ����Ũ�ȵı仯 ����:���ڷ� ��Դ:δ֪ ���ڣ�2016-02-02 18:19:06 �����4940 ����ר�⣺��Һϡ�� ����Ũ�ȴ�С�Ƚ�
[ע�������j] �������Һϡ��ʱ����Ũ�ȵı仯 ����:���ڷ� ��Դ:δ֪ ���ڣ�2016-02-02 18:19:06 �����4940 ����ר�⣺��Һϡ�� ����Ũ�ȴ�С�Ƚ�
�������Һ������Ũ�ȴ�С��仯�Ķ��ԺͰ붨���������Ǹ߿����ȵ㣬Ҳ��ѧϰ���ѵ�֮һ��ѧ���ձ�е������գ�����ټ���������ϣ���ܶ�ͬѧ������������ һ��������Һϡ��ʱ����Ũ�ȵı仯 [ �� 1] ��ˮϡ�� 0.1mol/L �İ�ˮʱ����Һ������ˮ�������Ӷ����ٵ��ǣ�...
 ��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ�
��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ� ��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�
��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء���ѧ�����ʡ� �̲���������ʵ�飬һ���� AgI ת��Ϊ Ag 2 S��һ���� Mg(OH) 2 ת��Ϊ ...
25 �� ʱ�� K a1 (H 2 S)=1.1 �� 10 -7 �� K a2 (H 2 S)=1.3 �� 10 -13 . ���ߵȽ���...
����ת���dz����ܽ�ƽ���Ӧ��֮һ�� �����ܶȻ��ϴ�ij���תΪ�ܶȻ���С�ij�������...
1.ʵ�� �����£���0.100 0 mol��L ��1 NaOH��Һ�ζ�20.00 mL 0.100 0 mol��L ��1 CH 3...
������֣�pH=5��ϡ�����ˮ��ϡ1000����ϡ�ͺ���Һ��pH=����ͨ������˵���� ���⣺��...
��Ԫ�����Ƿֲ�����ģ����Ե�һ������Ϊ�����������볣�����٣������ܴ� ��...
���ɽ������ж�������������Ϊ�����d���ӿ��Բ��ֻ���ȫ������ɼ��������������...
�ʣ�Ϊʲôǿ���ڱ������п��ԱȽϳ�������ǿ���� ��Ҫ�ش�������⣬���ǵûص����...