
|
ѧϰСר�� |

|
ѧϰСר�� |
 [ע�������j] Ksp��s��p�ĺ��� ����:�Ű� ��Դ:δ֪ ���ڣ�2013-03-28 09:10:28 �����4589 ����ר�⣺�ܶȻ�
[ע�������j] Ksp��s��p�ĺ��� ����:�Ű� ��Դ:δ֪ ���ڣ�2013-03-28 09:10:28 �����4589 ����ר�⣺�ܶȻ�
Ksp��sp��solubility product��solubility���������product���˻�����solubility product���ܶȻ��������Ƶ�Kw�е�w��water��ˮ)��...
 [ע�������j] Ӧ������ˮ��֪ʶ���͵ļ������� ����:���� ��Դ:δ֪ ���ڣ�2020-01-30 14:08:15 �����8000 ����ר�⣺����ˮ��Ӧ��
[ע�������j] Ӧ������ˮ��֪ʶ���͵ļ������� ����:���� ��Դ:δ֪ ���ڣ�2020-01-30 14:08:15 �����8000 ����ר�⣺����ˮ��Ӧ��
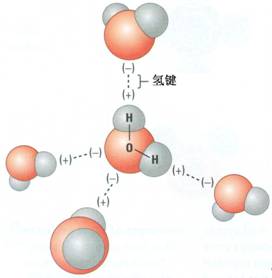
1 . ��ѧʵ���е�����ˮ������ �� Ϊʲôʵ���������� FeCl 3 ��ҺʱҪ�����м�������Ũ��� Ŀ����Ϊ�˷�ֹ FeCl3 ��Һ��ˮ�⣬��Ϊ�� FeCl3 ��Һ�д�������ˮ�ⷽ��ʽ�� FeCl 3 �� 3H 2 O Fe(OH) 3 ���� 3HCl��������Һ�м���Ũ����ʱ����ˮ�ⷽ��ʽ������У��Ӷ�...
 [ע�������j] �����볣�·ֱ��Ƕ���? ����:��ͤ ��Դ:δ֪ ���ڣ�2020-02-26 10:32:59 �����17450 ����ר�⣺�����볣��
[ע�������j] �����볣�·ֱ��Ƕ���? ����:��ͤ ��Դ:δ֪ ���ڣ�2020-02-26 10:32:59 �����17450 ����ר�⣺�����볣��
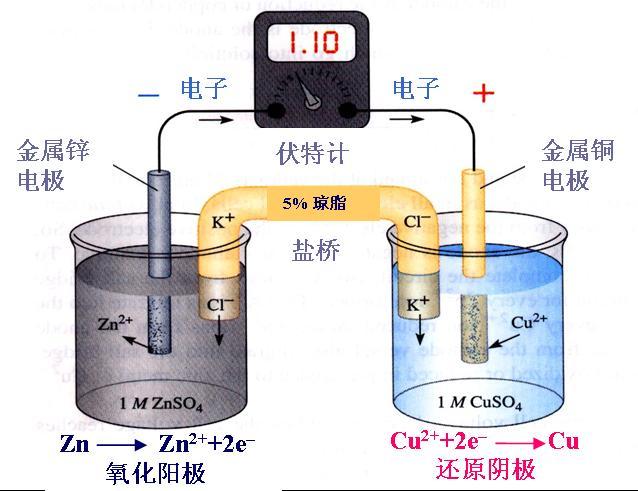
�ҹ���������Ϊ25�棬����Ϊ20�档 ������һ���϶����ºͳ��¶�Ϊ20�� �����¡����ֵij��Ϸ�Ϊ��ͬ�����ճ�֮�У�������Ʒ��������ȡ��ڼ�������ͬγ�ȹ��һ���������ƹ��ұ��ij��¹涨���������£� ��ŷ��15��......��䡢������Ų�������� ŷ�ޣ�20��.........
 [ע�������j] NaHCO3�ļ��Ա�NaAcǿ�� ����:���� ��Դ:δ֪ ���ڣ�2013-03-12 15:34:25 �����3021 ����ר�⣺̼������01 ������ж�
[ע�������j] NaHCO3�ļ��Ա�NaAcǿ�� ����:���� ��Դ:δ֪ ���ڣ�2013-03-12 15:34:25 �����3021 ����ר�⣺̼������01 ������ж�
����������ʦ��ѧ�����⣺ H 2 CO 3 �����Ա� HAc �������Զ�Ӧ NaHCO 3 �ļ��Ա� NaAc ǿ���Ȼ�Ǵ���ģ���ʵ�� NaHCO 3 ��Һ�� pH ԼΪ 8.3 ���� 0.1mol/L NaAc ��Һ�� pH Ϊ 8.9 �� 0.01mol/L NaAc ��Һ�� pH ԼΪ 8.4 �� �������� NaHCO 3 ����ʽ�Σ���ˮ��ȿ��ܸ�...
 [̽������չ3] �����������������һ�����ܴ��������� ����:��ʤ ��Դ:δ֪ ���ڣ�2013-03-07 10:43:29 �����4584 ����ר�⣺���ӹ��� ˫ˮ�ⷴӦ
[̽������չ3] �����������������һ�����ܴ��������� ����:��ʤ ��Դ:δ֪ ���ڣ�2013-03-07 10:43:29 �����4584 ����ר�⣺���ӹ��� ˫ˮ�ⷴӦ
������������������������ܲ��ܴ������棬����һ�Ŷ��ۡ�������ѧ���������ϵ������ܷ�ϰ���ж���Ϊ����������������������ܴ������棬���Ǵ���ġ������李�̼����淋Ⱦ�����������������������Դ�����������ӡ�����Щ���������������������ˮ��̶ȴ�����...
 [̽������չ3] ���ֽⷴӦ����֮һ���������������� ����:����̩ ��Դ:δ֪ ���ڣ�2013-03-07 10:30:25 �����2901 ����ר�⣺���ֽⷴӦ
[̽������չ3] ���ֽⷴӦ����֮һ���������������� ����:����̩ ��Դ:δ֪ ���ڣ�2013-03-07 10:30:25 �����2901 ����ר�⣺���ֽⷴӦ
������ �¡��ɽ̲��ڲ������ֽⷴӦ������ʱ�������������ģ���ʵ����ѧ����������Ӱ�죬����ѧ��������Ϊֻ�������������ʲŻ��г�������ʵֻҪ���ʵ��������ܽ��������ֵ�������������ʻ����������ʶ��ܳ�������ӦҲ����˶������ˣ�ѧ�����������ɳ����������������...
 [ע�������j] �й������������±�淶���� ����:���� ��Դ:δ֪ ���ڣ�2013-02-28 16:22:46 �����3502 ����ר�⣺�淶
[ע�������j] �й������������±�淶���� ����:���� ��Դ:δ֪ ���ڣ�2013-02-28 16:22:46 �����3502 ����ר�⣺�淶
K c ����K p �� �� c �� p �ֱ� ��ʾŨ�Ⱥ�ѹǿ��Ҫб�壻�� K a �� K b �� K w �� K sp �� a �� b �� w �� sp ������б�壻 �� G m �� ( T ) �� G �� T Ϊб�壬�� m �� �� ����б�� �� �� H m �� ( T ) �� H �� T Ϊб�壬�� m �� �� ����б�� ��...
 [ע�������j] ij����Һ�����ԣ�����һ��δˮ���� ����:���� ��Դ:δ֪ ���ڣ�2012-11-07 09:41:39 �����4019 ����ר�⣺����ˮ�����
[ע�������j] ij����Һ�����ԣ�����һ��δˮ���� ����:���� ��Դ:δ֪ ���ڣ�2012-11-07 09:41:39 �����4019 ����ר�⣺����ˮ�����
ij����Һ�����ԣ����β�һ��δˮ�⣬���磺NaCl��Һ�����ԣ�����ΪNaCl��ǿ��ǿ���Σ���ˮ�⡣�����磺CH 3 COONH 4 ��Һ�����ԣ�ȴ��ˮ��Ľ���� CH 3 COONH 4 �����ܡ���������������Σ���������ˮ���ԭ����ʵ��������CH 3 COONH 4 ȷʵ��ˮ�⣬CH 3 COO - ˮ������C...
 [ע�������j] Ϊʲô���ӻ����ﶼ��ǿ����ʣ� ����:�º� ��Դ:δ֪ ���ڣ�2012-11-07 09:39:12 �����5955 ����ר�⣺���ӻ����� ǿ�����
[ע�������j] Ϊʲô���ӻ����ﶼ��ǿ����ʣ� ����:�º� ��Դ:δ֪ ���ڣ�2012-11-07 09:39:12 �����5955 ����ר�⣺���ӻ����� ǿ�����
���ӻ����ﱾ��������������ɵģ������ӻ������в����ڷ��ӡ����ӻ���������������ˮ�����ۻ�״̬�����������ӵ���ʽ���ڣ��������ڷ��ӡ������ӻ���������ˮ�������ۻ��Ժ���ȫ����Ϊ�����ƶ������ӣ������ӻ����ﶼ��ǿ����ʡ�...
 [ע�������j] ����������ʼ��������������⼯ ����:������ ��Դ:δ֪ ���ڣ�2018-07-19 15:51:32 �����11985 ����ר�⣺�������
[ע�������j] ����������ʼ��������������⼯ ����:������ ��Դ:δ֪ ���ڣ�2018-07-19 15:51:32 �����11985 ����ר�⣺�������
һ��������ʵ���ƽ������ 1 ����ʵ����ۡ��� ��ǿ�ᡢ�����ˮϡ��ʱ����Һ�� pH ������ c(H �� ) ����С����Һ�е� c(OH �D ) �������ǿ������ˮϡ��ʱ����Һ�� pH ����С�� c(OH �D ) ����С����Һ�е� c(H �� ) ������� ��ǿ�ᡢǿ���ˮϡ��ʱ����Һ...
 ��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ�
��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ� ��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�
��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء���ѧ�����ʡ� �̲���������ʵ�飬һ���� AgI ת��Ϊ Ag 2 S��һ���� Mg(OH) 2 ת��Ϊ ...
25 �� ʱ�� K a1 (H 2 S)=1.1 �� 10 -7 �� K a2 (H 2 S)=1.3 �� 10 -13 . ���ߵȽ���...
����ת���dz����ܽ�ƽ���Ӧ��֮һ�� �����ܶȻ��ϴ�ij���תΪ�ܶȻ���С�ij�������...
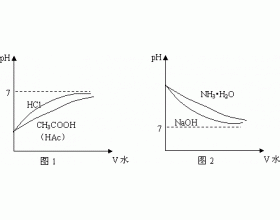
1.ʵ�� �����£���0.100 0 mol��L ��1 NaOH��Һ�ζ�20.00 mL 0.100 0 mol��L ��1 CH 3...
������֣�pH=5��ϡ�����ˮ��ϡ1000����ϡ�ͺ���Һ��pH=����ͨ������˵���� ���⣺��...
��Ԫ�����Ƿֲ�����ģ����Ե�һ������Ϊ�����������볣�����٣������ܴ� ��...
���ɽ������ж�������������Ϊ�����d���ӿ��Բ��ֻ���ȫ������ɼ��������������...
�ʣ�Ϊʲôǿ���ڱ������п��ԱȽϳ�������ǿ���� ��Ҫ�ش�������⣬���ǵûص����...