
|
学习小专题 |

|
学习小专题 |
 [方法与规律e] 计算法分析离域π键 作者:化学自习室 来源:未知 日期:2024-01-26 08:09:11 点击:2211 所属专题:大π键
[方法与规律e] 计算法分析离域π键 作者:化学自习室 来源:未知 日期:2024-01-26 08:09:11 点击:2211 所属专题:大π键
1 、 离域 π 键 的概念 : 把分子轨道理论的一些结果,引入价键理论,来解释分子的结构和一些性质,产生了离域 π 键的概念。 离域 π 键不同于两原子间的 π 键,是由三个或三个以上原子形成的 π 键。不像普通 π 键,它的成键电子不再局限在两个原子之间的区域,而...
 [方法与规律e] 如何比较NH3和NF3的键角大小? 作者:化学自习室 来源:未知 日期:2024-01-17 08:05:34 点击:3086 所属专题:键角
[方法与规律e] 如何比较NH3和NF3的键角大小? 作者:化学自习室 来源:未知 日期:2024-01-17 08:05:34 点击:3086 所属专题:键角
键角是共价键的键参数之一,在多原子分子中,2个相邻共价键之间的夹角称为键角。键角是描述分子空间结构的重要参数,分子的许多性质都与键角有关。 那么,如何判断分子键角的大小呢? (1)确定中心原子的杂化类型。 根据VSEPR理论,中心原子分别为sp 3 、sp 2 和sp杂化时,它们...
 [方法与规律e] 分子中键角大小影响因素 作者:化学自习室 来源:未知 日期:2024-01-16 16:23:04 点击:1233 所属专题:键角
[方法与规律e] 分子中键角大小影响因素 作者:化学自习室 来源:未知 日期:2024-01-16 16:23:04 点击:1233 所属专题:键角
共价键的键角是中心原子与另两个原子所成共价键间的夹角,是共价键的基本参数之一。 影响分子中共价键键角大小的主要因素有: (1)中心原子的杂化类型: (2)中心原子的孤对电子数目: (3)配位原子的电负性: (4)中心原子的电负性: (5) 单键与重键: (6)单电子: (7)配体的体积 ...
 [方法与规律e] 高中化学中大π键的题型中π电子数快速分析 作者:化学自习室 来源:未知 日期:2023-12-29 08:40:38 点击:688 所属专题:大π键
[方法与规律e] 高中化学中大π键的题型中π电子数快速分析 作者:化学自习室 来源:未知 日期:2023-12-29 08:40:38 点击:688 所属专题:大π键
我来给个简单的计算π电子数的办法吧,高中生很容易听得懂 首先,判断中心原子杂化情况,中心原子sp2杂化就只有一组大π键,如果中心原子是sp3杂化,那就会有两组相互垂直的。 先说第一类情况。 首先,高考题目的大π键体系,端位原子(H除外)一般会有四个轨道,即一个...
 [方法与规律e] 2023年7月人教版《化学必修一》再印改变之处总结 作者:化学自习室 来源:未知 日期:2023-11-29 08:16:14 点击:870 所属专题:教材对比
[方法与规律e] 2023年7月人教版《化学必修一》再印改变之处总结 作者:化学自习室 来源:未知 日期:2023-11-29 08:16:14 点击:870 所属专题:教材对比
2019年6月第1版(即新教材),版次为2019年,从第1次印刷(2019年6月,以下简称“原”)至第6次印刷(2023年7月,以下简称“现”),全书多处改动,分列如下: 1.P 7 :原“CaO、Fe 2 O 3 等能与酸反应生成盐和水,这类氧化物称为碱性氧化物”,现变更为“CaO、MgO等能与酸反应生...
 [方法与规律e] 如何计算氢键数目? 作者:化学自习室 来源:未知 日期:2024-03-13 08:28:58 点击:1965 所属专题:氢键数目
[方法与规律e] 如何计算氢键数目? 作者:化学自习室 来源:未知 日期:2024-03-13 08:28:58 点击:1965 所属专题:氢键数目
均摊法常用在晶体有关分析及计算中:如果一个微粒被n个晶胞共享,那么它属于每一个晶胞的只有1/n,这种方法称为均摊法。 根据冰的结构,每个水分子与周围的4个水分子形成氢键。但是每两个水分子共用1个氢键,所以氢键数目= 4×1/2 = 2,即因此1mol水分子(冰))分子间实...
 [方法与规律e] 键角大小的比较小专题 作者:化学自习室 来源:未知 日期:2023-05-18 16:01:17 点击:2724 所属专题:键角
[方法与规律e] 键角大小的比较小专题 作者:化学自习室 来源:未知 日期:2023-05-18 16:01:17 点击:2724 所属专题:键角
【知识归纳】 一.中心原子杂化方式不同 (比较杂化方式) 分子 CO 2 、C 2 H 2 BF 3 、SO 3 CH 4 、S O 4 2 - 杂化方式 sp sp 2 sp 3 分子构型 直线型 平面三角形 正四面体 键角 180 ° 120 ° 109 ° 28' 二.中心原子杂化方式相同( 比较孤电子对数,斥力:孤对孤>孤对键...
 [方法与规律e] 杂化轨道的判断 作者:化学自习室 来源:未知 日期:2023-01-10 10:01:48 点击:6562 所属专题:杂化类型判断
[方法与规律e] 杂化轨道的判断 作者:化学自习室 来源:未知 日期:2023-01-10 10:01:48 点击:6562 所属专题:杂化类型判断
一、基本方法 最基本的常规方法,是根据 VSEPR 判断。由于 Vp (价层电子对数) =Lp (孤电子对数) + Bp ( σ 键电子对数),而杂化轨道要么用来容纳孤电子对( Lp ),要么填充 1 个电子用来形成 σ 键( Bp )。因此 杂化轨道数就等于 Vp 数 。 (中学教材只涉及了 ...
 [方法与规律e] 电子式法快速判断大π键类型 作者:叶昌平 来源:启迪化学 日期:2022-08-13 09:14:16 点击:3923 所属专题:大π键
[方法与规律e] 电子式法快速判断大π键类型 作者:叶昌平 来源:启迪化学 日期:2022-08-13 09:14:16 点击:3923 所属专题:大π键
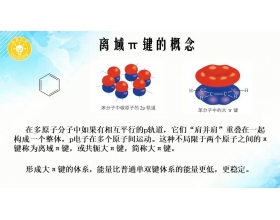
作者说解:离域π键的类型可依据概念进行判断、或依据等电子原理判断、或用电子式快速分析判断。在高中不宜讲解过深、过于复杂,更不应该作为一个知识点做系统补充,2017年全国卷二考察N5-离子的大 π 键类型是基于信息和能力的考察,主要考察学生对于原子轨道和轨道间...
 [方法与规律e] 氮及其化合物的分子空间结构分析 作者:张仿刚 来源:化学教育期刊 日期:2022-07-29 10:23:13 点击:26692 所属专题:氮及其化合物 分子空间结构判断
[方法与规律e] 氮及其化合物的分子空间结构分析 作者:张仿刚 来源:化学教育期刊 日期:2022-07-29 10:23:13 点击:26692 所属专题:氮及其化合物 分子空间结构判断
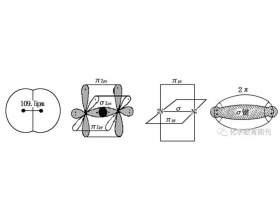
氮原子的价电子结构为2s22p3,电负性仅次于氟与氧,能与其他元素形成较强的化学键,存在多种价态,高中生很难正确把握氮及其化合物的结构,笔者对此进行理论分析和结构总结,以期有助于师生的正确理解。 根据中心原子成键时杂化方式的不同,本文将氮及其化合物分成四大...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。顺反异构中,分子的对称性、极性以及熔点和沸点存在以下差异: 1.对称性比较 反式异构...
01 ― 概念 在多原子分子(就是三个或三个以上的原子构成的分子)中,如有相互平行的p...
含有共价键的物质中相邻两键之间的夹角称为键角。键角是决定物质分子空间构型的主要因...
1.非环状小分子和离子中的大π键:大多数满足AB n 型,可以计算杂化类型。 首先:参与...
1.σ键与π键 σ键:原子轨道沿着轨道对称轴的方向“头碰头”重叠形成的共价键。 π键...
配位化合物的空间构型: 二配位:直线型;四配位:正四面体型或平面正方形;六配位(无...
1、当中心离子(或原子)与多基配体配合时,配位数可以等同于配位原子的数目,但不是配...
一、 知识储备 1、 手性 手性 ( chirality ) 一词指一个物体不能与其镜像相重合 。 ...