
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑a] 常用36元素的一些性质和用途 作者:周四 来源:未知 日期:2021-12-29 09:18:09 点击:7416 所属专题:短周期元素
[注解与辨疑a] 常用36元素的一些性质和用途 作者:周四 来源:未知 日期:2021-12-29 09:18:09 点击:7416 所属专题:短周期元素
氢( H ) 主要性质和用 熔点为 -259.1 ℃ ,沸点为 -252.9 ℃ ,密度为 0.08988g/L(10 ℃ ) 。无色无臭气体,不溶于水,能在空气中燃烧,与空气形成爆炸混合物。工业上用于制造氨、环已烷、甲醇等。 氦 (He) 主要性质和用途 熔点为 -272.2 ℃ (加压),沸点为- 268.9...
 [注解与辨疑a] 元素金属性及非金属性的比较方法 作者:章金莲 来源:未知 日期:2013-11-13 17:18:36 点击:10601 所属专题:金属性 非金属性
[注解与辨疑a] 元素金属性及非金属性的比较方法 作者:章金莲 来源:未知 日期:2013-11-13 17:18:36 点击:10601 所属专题:金属性 非金属性
一、元素金属性的比较方法 1 、用失去电子的难易比较:金属原子失去电子越容易,金属元素的金属性就越强;金属原子失去电子越不容易,金属元素的金属性就越弱。 例如:钠比镁更容易失去电子,钠金属性比镁强。 2 、用与水反应产生氢气的能力比较:金属越容易和水反应产生氢...
 [注解与辨疑a] 原子序数与化学式关系归纳 作者:陈爱玉 来源:未知 日期:2016-01-24 17:06:23 点击:2892 所属专题:原子序数 化学式
[注解与辨疑a] 原子序数与化学式关系归纳 作者:陈爱玉 来源:未知 日期:2016-01-24 17:06:23 点击:2892 所属专题:原子序数 化学式
原子序数与化学式的联系依靠化合价关联在一起,而化合价又主要取决于最外层电子数。原子序数决定了原子的核外电子排布,决定了最外层电子数,决定了在周期表的周期和族,也就决定了元素的化合价。原子序数就就主要通过主族序数和化学式关联在一起。 例如:AB 2 型的化合...
 [注解与辨疑a] 常见的含氧酸及其含氧酸盐的化学式 作者:李萱 来源:未知 日期:2014-01-11 17:34:16 点击:5878 所属专题:含氧酸 分子式
[注解与辨疑a] 常见的含氧酸及其含氧酸盐的化学式 作者:李萱 来源:未知 日期:2014-01-11 17:34:16 点击:5878 所属专题:含氧酸 分子式
1 、突破含氧酸及其含氧酸盐的化学式关键还是把握元素的化合价,一般来说,元素有什么样的化合价,就有什么样的含氧酸,也就有什么样的含氧酸盐。 Be H 2 BeO 2 、 Na 2 BeO 2 B HBO 2 、 H 3 BO 3 、 H 2 B 4 O 7 、 NaBO 2 、 Na 3 BO 3 、 Na 2 B 4 O 7 、 Al H 3 Al...
 [注解与辨疑a] 有关元素性质的几个问题集 作者:舒龙昌 来源:山西省壶关县第一中学 日期:2016-01-24 17:02:07 点击:5800 所属专题:元素性质
[注解与辨疑a] 有关元素性质的几个问题集 作者:舒龙昌 来源:山西省壶关县第一中学 日期:2016-01-24 17:02:07 点击:5800 所属专题:元素性质
1、元素的金属性和金属活动性有什么区别? 元素的金属性是元素固有的性质。它反映了元素的原子失去电子成为阳离子能力的大...
 [注解与辨疑a] 元素周期表的特点以及分类 作者:张玮 来源:未知 日期:2013-05-03 20:01:54 点击:8858 所属专题:元素周期表结构
[注解与辨疑a] 元素周期表的特点以及分类 作者:张玮 来源:未知 日期:2013-05-03 20:01:54 点击:8858 所属专题:元素周期表结构
组 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 周 期 ⅠA ⅧA 1 1 H 非金属 稀有气体 2 He 氢g ⅡA 碱金属 准金属 ⅢA ⅣA ⅤA ⅥA ⅦA 氦g 2 3 Li 4 Be 碱土金属 卤素 5 B 6 C 7 N 8 O 9 F 10 Ne 锂 铍 过渡金属 主族元素 硼 碳 氮g 氧g 氟g 氖g 3 11 Na 12 Mg 稀...
在所有的原子中,氢原子是最小的,其直径大约为lA,即10 -8 (亿分之一)cm。把一亿个氢原子一个紧挨着一个地排成一个长队,这个长队也仅有1cm长。 把氢原子与乒乓球直径约为4cm放大相同的倍数会怎样?当把氢原子放大到乓球那么大时,乒乓球的直径将变为:4×4×10 8 cm...
 [注解与辨疑a] 分子间作用力的特点 作者:关平 来源:未知 日期:2013-04-09 16:50:54 点击:6335 所属专题:分子间作用力
[注解与辨疑a] 分子间作用力的特点 作者:关平 来源:未知 日期:2013-04-09 16:50:54 点击:6335 所属专题:分子间作用力
1. 不同情况下分子间作用力的组成不同 极性分子与极性分子间的作用力是由取向力,诱导力和色散力三部分组成;极性分子与非极性分子间只有诱导力和色散力,非极性分子间仅存在色散力.色散力是普遍存在.不仅如此,在多数情况下,色散力占据分子间作用力的绝大部分。 2. 分子间作用...
 [注解与辨疑a] 水的同位素组成 作者:向小平 来源:未知 日期:2013-04-09 16:13:41 点击:6637 所属专题:同位素
[注解与辨疑a] 水的同位素组成 作者:向小平 来源:未知 日期:2013-04-09 16:13:41 点击:6637 所属专题:同位素
1、水分子的结构式是H 2 O,实际上H有三种同位素 1 H(氕H)、 2 H(氘D)、 3 H(氚T)、氧有三种同位素 16 O、 17 O、 18 O,所以水实际上是18种水分子的混合物C 3 2 C 3 1 =18。 2、当然H 2 O是最普通的水分子(包括H 2 16 O(99.73%)、H 2 17 O(0.18%)、H 2 18 O(0....
 [注解与辨疑a] 原子结构易混概念辨析 作者:何永成 来源:未知 日期:2016-01-24 18:12:23 点击:4984 所属专题:原子结构03 概念辨析
[注解与辨疑a] 原子结构易混概念辨析 作者:何永成 来源:未知 日期:2016-01-24 18:12:23 点击:4984 所属专题:原子结构03 概念辨析
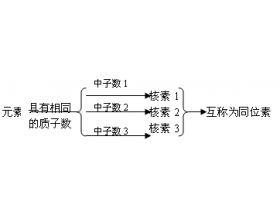
一、区分元素、核素、同位素的相互关系 1、元素 具有相同质子数的同一类原子的总称,元素是宏观概念,只表示种类,没有数量含义。如:氕( 1 1 H)、氘( 2 1 H或D)、氚(31H或T)三种原子的总称为氢元素。 2、核素 具有一定数目的质子和一定数目的中子的一种原子称为核...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。人教版高中化学必修第一册2019年6月第1版2024年7月第8次印刷P 10 3 讲解卤素单质与氢...
冰在0℃开始融化。这是本家都熟悉的事儿。 然而,世界上竟有热冰它在3.8℃方才融化! ...
1. 为什么 HF 分子间氢键比 H 2 O 分子间氢键强,而 HF 的沸点却比 H 2 O 的低? 由于...
1、为什么氧、氟没有最高正价?(朱朝宇) 氟是非金属性最强的元素,理论上没有哪种物...
1.如何理解分子间作用力的本质也是静电作用? 首先,在极性分子与极性分子之间,存在...
【关于化学键(Chemical bond)】: 化学键(Chemical bond)实质上是电性的微观作用...
...
准金属(metalloid),又称为半金属(semimetal),介于金属和非金属之间的物质。准金...