
|
ѧϰСר�� |

|
ѧϰСר�� |
 [ע�������a] �����������۲쵽С��ԭ������ģ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-02-08 19:21:35 �����554 ����ר�⣺����
[ע�������a] �����������۲쵽С��ԭ������ģ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-02-08 19:21:35 �����554 ����ר�⣺����
�ڽ���̫�����ε�ͬʱ������Ҳ��̽���ŷ��ӡ�ԭ��������ԭ�ӻ�С�������档�ڼ��������İ����£��˵���Ұ������С���������������� �š� 17���ͣ����������ĺ������������� ��ѧ���� �۲һ��ˮ�ᄍ����270���С�����ЩС������ٵ��ܶ��š�Ť���š���...
 [ע�������a] ��ˮ����ͨˮ����Щ���� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-02-08 18:35:18 �����1662 ����ר�⣺��ˮ ͬλ��
[ע�������a] ��ˮ����ͨˮ����Щ���� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-02-08 18:35:18 �����1662 ����ר�⣺��ˮ ͬλ��
���������϶ȾͻῪʼ�ڻ������Ǵ�Ҷ���Ϥ��֪ʶ��Ȼ���������Ͼ��С��ȱ���������3.8��ſ�ʼ�ڻ����Dz��ǽ�����ֱ���ˮ������?�����ǡ��γ����֡��ȱ�����Ҳ�ǵصص�����ˮ������������ͨˮ��Щ��һ����������ˮ������Է���������18����20�� ��ˮ����Է�������Ϊ...
 [ע�������a] ��ԭ�Ӻ��йصĻ�ѧ֪ʶ ����:������ ��Դ:δ֪ ���ڣ�2021-12-17 10:59:55 �����520 ����ר�⣺ԭ�ӹ���
[ע�������a] ��ԭ�Ӻ��йصĻ�ѧ֪ʶ ����:������ ��Դ:δ֪ ���ڣ�2021-12-17 10:59:55 �����520 ����ר�⣺ԭ�ӹ���
1.���Ӷ���������ɣ�ͬ�Ե������֮����ų⣬Ϊʲô���ǿ��Ծۼ���һ���γ��ȶ���ԭ�Ӻ��أ� ˵����֮�����ų⣬������Ϊ����֮����ڵ���������� ���ǣ���Ȼ�粻ֻ���ڵ��������һ��������������������⣬����ǿ����á�������á��Լ����������� ԭ�Ӻ���...
 [ע�������a] ���ں��������������������ǿ������ ����:������ ��Դ:δ֪ ���ڣ�2021-11-08 09:56:13 �����1169 ����ר�⣺������
[ע�������a] ���ں��������������������ǿ������ ����:������ ��Դ:δ֪ ���ڣ�2021-11-08 09:56:13 �����1169 ����ר�⣺������
�����������е����ǣ������ĺ��������и�ij�ᡢ��ij�ᡢ��ij�ᡢ��ij�ᡢƫij��ȣ���Щ���ƾ����������涨�ģ���ͬԪ�صĺ����ᣬͬ��Ԫ�ز�ͬ��̬�ĺ����ᣬ������ǿ���кι��ɣ�Ϊʲô����������Ҏ�ɣ������������ǿ������ȡ����ʲô�����أ� 1���Ժ��������Ա��ʵķ���...
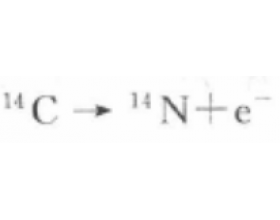 [ע�������a] ����ͬλ��֪ʶ������� ����:������ ��Դ:δ֪ ���ڣ�2021-11-08 08:53:53 �����1628 ����ר�⣺ͬλ��
[ע�������a] ����ͬλ��֪ʶ������� ����:������ ��Դ:δ֪ ���ڣ�2021-11-08 08:53:53 �����1628 ����ר�⣺ͬλ��
1��ͬλ�ص������к���ͬ�� ͬ��Ԫ�صIJ�ͬ���ػ���ͬλ�أ�����Ԫ���Ļ�ѧ����ȡ���ں˵�����ͺ�������Ų�����ͬλ��ǡǡ������ȫ��ͬ�ĺ˵�������������Ų�����ͬλ�ؾ�����ͬ�Ļ�ѧ���ʡ���Ҳ��Ϊʲô�Ѿ�����ͬ�������IJ�ͬ����ͳ��Ϊһ��Ԫ�ء��������ڱ���ͬ...
 [ע�������a] ���ڻ�ѧ����������� ����:������ ��Դ:δ֪ ���ڣ�2021-11-02 09:49:40 �����1441 ����ר�⣺��ѧ��
[ע�������a] ���ڻ�ѧ����������� ����:������ ��Դ:δ֪ ���ڣ�2021-11-02 09:49:40 �����1441 ����ר�⣺��ѧ��
1����ѧ�����ڡ�ǿ����á����ǡ�������ã� ��Ȼ�繲����4����������ǿ�����(��Ҫ��ָԭ�Ӻ������ӡ����ӵȻ�������֮��Ľ������)�� �������(��Ҫ��ָ����˥�䡢��������Ӻ����ӽ�Ϲ����б��ֳ�������)���������(������֪�ĵ��֮��ͬ����⡢��������...
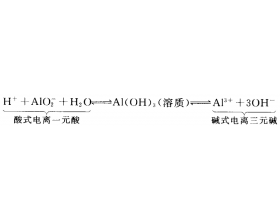 [ע�������a] ��������������������ԣ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-08-24 10:31:43 �����2430 ����ר�⣺��������
[ע�������a] ��������������������ԣ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-08-24 10:31:43 �����2430 ����ר�⣺��������
���ǰѼ������ᷴӦ�����κ�ˮ��������Ӧ�����κ�ˮ�Ļ� �����Ϊ�������ʡ������ȿ�һ��һЩ������������Ϊ�������ʵ� ���͡� 1.����Ԫ����Ԫ�����ڱ��е�λ�ÿ� Al�ǵ�3���ڡ���A��Ԫ�أ����ڽ�����ǽ����Ľ��紦������� ����Ԫ����ǽ���Ԫ�ع��ɵġ��߽�Ԫ�ء���...
 [ע�������a] ���Լ��ͷǼ��Լ���ô�ж� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2020-06-18 07:50:43 �����3569 ����ר�⣺���ļ���
[ע�������a] ���Լ��ͷǼ��Լ���ô�ж� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2020-06-18 07:50:43 �����3569 ����ר�⣺���ļ���
���Լ��ͷǼ��Լ������� (1) �Ǽ��Լ���ͬ��ԭ���γɹ��ۼ�������ԭ���������ӵ�������ͬ����ͬ���ӶԲ�ƫ���κ�һ��ԭ�ӣ����������ԭ�Ӻ˸����ԳƵطֲ�����˳ɼ���ԭ�Ӷ����Ե��ԡ������Ĺ��ۼ���Ϊ�Ǽ��Լ��� �жϷ���������ͬԪ�ص�ԭ���γɵĹ��ۼ��ǷǼ��Լ����絥...
 [ע�������a] Ԫ�������ɡ�Ԫ�����ڱ���ʶ���� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2020-06-13 11:15:28 �����878 ����ר�⣺Ԫ��������
[ע�������a] Ԫ�������ɡ�Ԫ�����ڱ���ʶ���� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2020-06-13 11:15:28 �����878 ����ר�⣺Ԫ��������
1������Ϊ����Ԫ�ص��������һ������������������F�����ۡ� 2������ΪԪ�صķǽ�����Խǿ�����������Ӧˮ��������Ծ�Խǿ������HClO��H 2 SO 3 �����ᣬ�����˹ؼ��ʡ���ۡ��� 3������Ϊͬ��������������Ԫ��ԭ������֮�����1�����������11��25�� 4������Ϊʧ������...
 [ע�������a] ���°�ע��Ԫ�����ڱ���˫��ͼƬ�Ŵ�鿴�� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-12-29 14:11:03 �����4476 ����ר�⣺Ԫ�����ڱ��ṹ Ԫ�ض���
[ע�������a] ���°�ע��Ԫ�����ڱ���˫��ͼƬ�Ŵ�鿴�� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-12-29 14:11:03 �����4476 ����ר�⣺Ԫ�����ڱ��ṹ Ԫ�ض���
...
 ��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ�
��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ� ��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�
��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء��˽̰���л�ѧ����һ��2019��6�µ�1��2024��7�µ�8��ӡˢP 10 3 ����±�ص�������...
����0�濪ʼ�ڻ������DZ��Ҷ���Ϥ���¶��� Ȼ���������Ͼ����ȱ�����3.8�淽���ڻ�! ...
1. Ϊʲô HF ���Ӽ������ H 2 O ���Ӽ����ǿ���� HF �ķе�ȴ�� H 2 O �ĵͣ� ����...
1��Ϊʲô������û��������ۣ����쳯� ���Ƿǽ�������ǿ��Ԫ�أ�������û��������...
1.���������Ӽ��������ı���Ҳ�Ǿ������ã� ���ȣ��ڼ��Է����뼫�Է���֮�䣬����...
�����ڻ�ѧ����Chemical bond������ ��ѧ����Chemical bond��ʵ�����ǵ��Ե�������...
...
������metalloid�����ֳ�Ϊ�������semimetal�������ڽ����ͷǽ���֮������ʡ���...