
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
在讨论"惰性气体"对"化学反应平衡"的影响之前,首先需要明确:这里所讨论的“惰性气体”究竟指的是什么?
这里的“惰性气体”不仅指“元素周期表”中第0族中的惰性气体元素(如He、Ne和 Ar等),还泛指一切不参与目标化学反应的气体。
惰性气体本身虽不直接参与化学反应。但其引入会改变系统的宏观状态(如,体积、压强或者浓度等),进而导致反应体系中各组分的分压(如果是气体)、浓度或者摩尔分数的改变。这种改变可能会打破原有的平衡状态,使反应发生移动,直至到新的条件下达到新的平衡(即平衡点)。可以想象一下天平中“物”和“码”之间的平衡关系。
易错点: 误把“平衡点(平衡组成)”和“平衡常数”混为一谈。
本质性差异:实际上,“平衡点”和“平衡常数”是有本质差别的。为便于说明与理解,引入“天平”这个例子。
左物(反应物或者生成物) 右码(生成物或者反应物)
平衡常数是“判据”,是“标尺”。是由“反应本性”和“温度”决定的热力学常数。在温度不变的情况下,是恒定不变的。
类比于天平。天平一经校准(温度确定),其“零点”(对应于“平衡常数”)的物理属性就被固定下来,不会改变了。
平衡点(平衡组成)刻画的则是:在特定温度、压强和初始浓度等条件下,化学反应达到平衡时,系统内各物质所需要满足的条件(如,浓度或者分压)。
类比于天平。为了保证天平的指针仍然能够回到零点(即,化学反应能够再次达到平衡),“左物”和“右码”必须重新匹配,形成一组新的组合。在化学平衡的语境下,可以将“左物”视为“反应物”,“右码”视为“生成物”(或反之)。当外界条件发生改变(如,加入惰性气体)时,相当于改变了天平所处的环境。原有“砝码”(各物质的平衡分压或者浓度)平衡组合一旦被打破,导致天平指针偏离“零点”。此时,需要重新调整“物”和“砝码”(通过化学反应调整),直至形成一组新的砝码组合(“平衡点”各组分的组成),使指针重新指向零点(达到化学平衡)。这一过程正是化学平衡的移动,最终系统在新的平衡下达到新的平衡点,而天平的零点(即平衡常数)始终保持不变。
接下来,将对此展开详细的“定量”分析。
惰性气体对化学反应平衡的影响机制,根本上取决于系统所处的宏观约束条件。在理想化的热力学中,“恒容”与“恒压”代表了两种最典型、物理图像相反的理想约束条件,为我们提供了最清晰的分析框架和视角。尽管实际工业过程或者实验装置可能更为复杂,但是其内在的基本原理仍可追溯并基于这两种理想模型进行理解和逻辑推演。理解这两种极端情况,是掌握惰性气体如何影响化学平衡的钥匙。
以这两种极端情况作为切入点,系统揭示其内在机理。
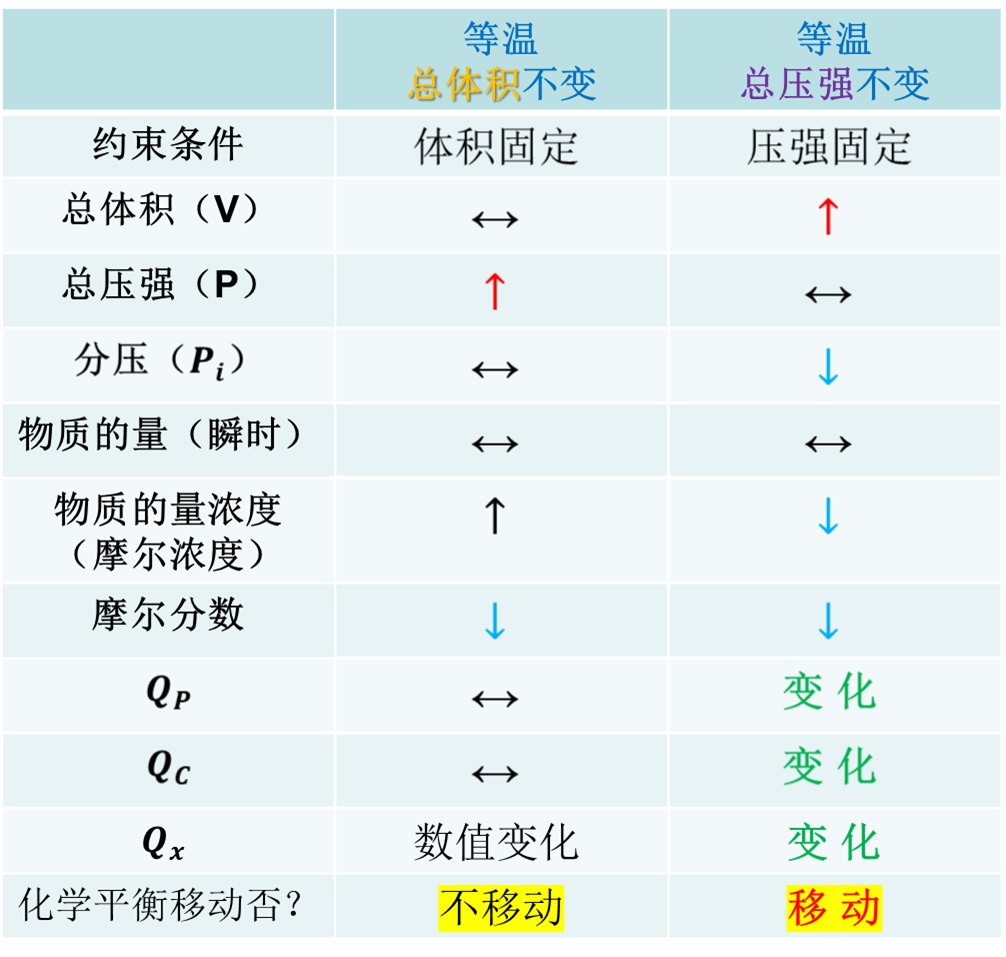
1)等温、总体积不变的情况下(如,容器的体积是固定的,或者容器是刚性密闭容器,亦或体积变化小到可以忽略不计),加入惰性气体后,系统的总压强升高了。
约束条件为:恒容
例 子:在《燃烧热》实验中用到的不锈钢制燃烧弹;水热/溶剂热合成微/纳米材料时用到的高压反应釜;高压锅;密封罐;气瓶/气罐;喷雾的储存状态等。
实际效果:引入惰性气体后,
a)系统的总压强增大了;
b)系统内各组分的摩尔分数(![]() )减小了(惰性气体加入的瞬间,各组成的物质的量不变,但是总的物质的量增加了。分母增大导致各组分摩尔分数变小。)
)减小了(惰性气体加入的瞬间,各组成的物质的量不变,但是总的物质的量增加了。分母增大导致各组分摩尔分数变小。)
c)系统内各组分的物质的量浓度(或者摩尔浓度 ![]() )没有发生变化(系统内各组分的物质的量不变,系统的总体积亦未发生变化),其效果等同于被稀释;
)没有发生变化(系统内各组分的物质的量不变,系统的总体积亦未发生变化),其效果等同于被稀释;
d)系统内各组分的分压没有发生变化(可参照理想气体方程![]() )。
)。
综上所述,等温、恒容条件下,加入惰性气体以后,仅仅增加了容器内“背景粒子密度”,提高了总压,但是并未改变系统内各组分的物质的量、摩尔浓度和分压。(天平两端的“砝码”没有发生变化。)
因此,基于“摩尔浓度”的化学反应商(![]() )和基于“压强”的化学反应商(
)和基于“压强”的化学反应商(![]() )没有发生变化。
)没有发生变化。
表明:在等温、恒容的条件下,惰性气体的加入不会影响化学平衡的移动(![]() )
)
易错点:将“数值变化”的![]() 误认为是反应物或者产物的物质的量发生改变。
误认为是反应物或者产物的物质的量发生改变。
本 质:![]() 的“数值变化”是相对于
的“数值变化”是相对于![]() 和
和![]() 而言的。这种变化主要来自于摩尔分数定义中分母的改变,并不反映反应物或者产物的实际量发生了变化,是纯粹的“数值重标定”。
而言的。这种变化主要来自于摩尔分数定义中分母的改变,并不反映反应物或者产物的实际量发生了变化,是纯粹的“数值重标定”。
此外,以"摩尔分数"为基准,判断反应方向或者计算平衡常数时,需要额外知道平衡总压,并会引入压力修正项,使计算较为繁琐。故,在高中化学课程的学习中,同学们处理的都是基于“摩尔浓度”和基于“压强”的化学平衡常数/商。
2)等温、总压强不变的情况下(比如,采用带活塞的容器),加入惰性气体后,系统的总体积增大了。
约束条件为:恒压
例 子:吹气球;敞口的罐子(此时的压力为大气压);喷雾的喷出/使用瞬间等。
实际效果:引入惰性气体后,
a)系统的总体积增大了(鉴于![]() 的关系;为了保证系统的压强不变。);
的关系;为了保证系统的压强不变。);
b)系统内各组分的物质的量浓度减小了(因为总体积增大了),其效果等同于被稀释了;
c)系统内各组分的分压变小了(鉴于![]() );
);
d)各组分的摩尔分数(![]() )减小了(引入惰性气体后,总的物质的量增大了)
)减小了(引入惰性气体后,总的物质的量增大了)
综上所述,等温、恒压条件下,加入惰性气体后,系统内各组分的物质的量浓度、分压和摩尔分数均变小了。
因此,基于“压强”的化学反应商![]() 、基于“浓度”的化学反应商
、基于“浓度”的化学反应商![]() 和基于“摩尔分数”的化学反应商
和基于“摩尔分数”的化学反应商![]() 均瞬间减小。
均瞬间减小。
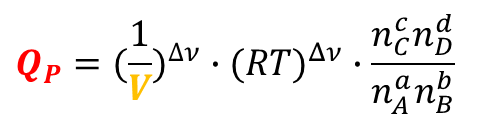
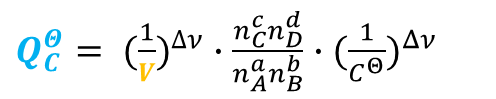
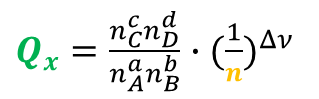
如上可知:等温等压下,惰性气体通过体积膨胀改变了反应商,化学反应进行的方向由![]() 唯一确定(惰性气体引入瞬间)。
唯一确定(惰性气体引入瞬间)。
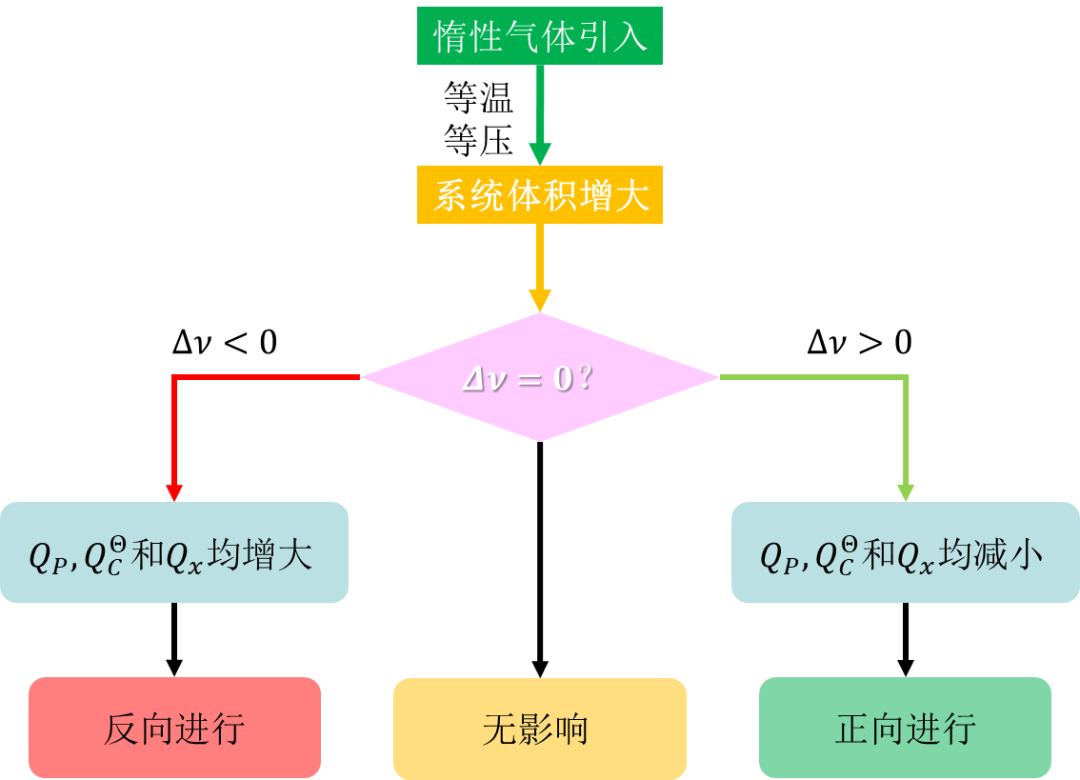
是不是和高中化学熟悉的“勒夏特列原理”不谋而合了。:)
勒夏特列原理:
如果改变一个处于平衡状态的系统的条件(如温度、压力和浓度),平衡会向减弱这种改变的方向移动。即,“抵抗”改变。
综上,可以得到如下小结:

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
在讨论惰性气体对化学反应平衡的影响之前,首先需要明确:这...
一、外界条件对反应速率的影响:别只看压强! 很多同学在判断...
在化学反应中,驱动力指的是推动反应进行的内在因素,它决定...
一.核心概念辨析 中间体:寿命长于分子振动的瞬态物种,多步...
活化分子百分数和活化分子数,理解它对掌握化学反应速率至关...
化学反应的焓变越大,代表这个反应受温度变化的影响越大吗?...