
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、一个“懒惰”的电子对如何改写元素命运?
在元素周期表的底部,第六周期的 p 区元素——铊(Tl)、铅(Pb)、铋(Bi)、钋(Po)和砹(At)——展现出一种奇特的化学行为:它们似乎“偏爱”较低的氧化态,而对本应更稳定的高氧化态表现出明显的“抗拒”。例如,铅最常见的化合物是 Pb²⁺(如 PbCl₂、PbO),而非按族序预期的 Pb⁴⁺;铋在自然界中以 Bi³⁺ 为主,而 Bi⁵⁺ 几乎只存在于强氧化剂如 NaBiO₃ 中。这种现象并非偶然,其背后隐藏着一个精妙的物理化学原理——惰性电子对效应(Inert Pair Effect)。
二、什么是惰性电子对效应?
惰性电子对效应是指:在第六周期(以及部分第五周期)p 区重元素中,最外层的 ns² 电子对(如 6s²)倾向于保持不参与成键或氧化,导致低价态(比族序低2)比高价态更稳定的现象。
元素 | 族 | 族序价态 | 实际稳定价态 | 高价态性质 |
|---|---|---|---|---|
Tl | 13 | +3 | +1 | Tl³⁺ 是强氧化剂 |
Pb | 14 | +4 | +2 | Pb⁴⁺(如 PbO₂)是强氧化剂 |
Bi | 15 | +5 | +3 | Bi⁵⁺(如 NaBiO₃)是极强氧化剂 |
Po | 16 | +6 | +4 / +2 | Po⁶⁺ 极不稳定 |
At | 17 | +7 | +1 / –1 | 高价砹化合物罕见 |
这一趋势从第五周期开始初现端倪(如 Sb³⁺ 比 Sb⁵⁺ 更稳定),到第六周期达到顶峰,成为理解这些元素化学性质的核心。
三、相对论效应如何“冻结”s 电子?
传统周期律认为,同族元素自上而下金属性增强,高价态应更稳定。但惰性电子对效应打破了这一预期。其根本原因在于——相对论量子力学效应。
1. s 轨道的相对论收缩
在原子序数Z >70的重元素中,内层电子运动速度接近光速,根据狭义相对论,其有效质量增加,导致轨道行为改变:
• s 轨道(尤其是 6s):因角动量为零(角量子数ℓ=0),电子有显著概率出现在原子核附近,受强核电荷吸引,轨道半径收缩,能量显著降低。
• p、d、f 轨道:因存在角动量(ℓ≥1),电子远离核区,受相对论效应影响较小,甚至因屏蔽增强而略微膨胀。
以铅(Pb, Z=82为例:
• 6s 轨道能量大幅下降,6s² 电子被“牢牢锁在”原子核附近;
• 6p 轨道能量相对升高;
• 6s 与 6p 能级差显著增大。
2. 激发能剧增:ns² → ns¹np¹ 变得极其困难
要形成比族序低2的高价态(如 Pb⁴⁺),需将 6s² 电子激发至 6p 轨道,形成 sp³ 杂化(如 PbCl₄ 中的 Pb⁴⁺)。但由于 6s–6p 能隙变大,激发能极高,远超成键所能释放的能量。
结果:原子“宁愿”只使用 6p 电子成键,保留 6s² 电子对——即呈现 +2 价(Pb²⁺),而非 +4 价。
3. 电离能异常:第二电离能 < 第三电离能(反常)
以 Tl 为例(电子构型 [Xe]4f¹⁴5d¹⁰6s²6p¹):
• 移去 6p¹ 电子(形成 Tl⁺)较容易;
• 再移去一个 6s 电子(形成 Tl²⁺)极难;
• 移去第二个 6s 电子(形成 Tl³⁺)更是难上加难。
因此,Tl⁺ 的稳定性远高于 Tl³⁺,后者极易获得电子还原为 Tl⁺,表现为强氧化性。
四、化学表现:从稳定低价到超强氧化性
惰性电子对效应在化学性质上体现为两个看似矛盾实则统一的方面:
1. 低价态异常稳定
• Tl⁺ 的化学行为类似碱金属离子(如 K⁺):TlCl、Tl₂SO₄ 可溶,TlOH 为强碱。
• Pb²⁺ 是铅化学的主角:PbO(黄丹)、PbCO₃(白铅矿)、PbSO₄(铅矾)均为常见矿物。
• Bi³⁺ 在水溶液中稳定存在,可形成 BiOCl(次氯酸铋,用于化妆品)等化合物。
这些低价化合物不仅热力学稳定,且动力学惰性高,不易被氧化。
2. 高价态成为强氧化剂
由于高价态违背了“6s² 惰性”的自然倾向,它们处于高能、不稳定状态,极易被还原:
• PbO₂(二氧化铅):用于铅酸电池正极:
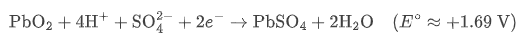
可氧化浓 HCl 生成 Cl₂。
• NaBiO₃(铋酸钠):实验室经典试剂,用于定性检测 Mn²⁺:
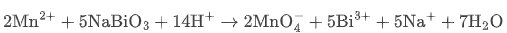
紫红色 MnO₄⁻ 的出现,正是 Bi⁵⁺ 强氧化性的直接证据。
• Tl³⁺ 盐:在水溶液中迅速水解并氧化水或有机物,需在强酸中稳定存在。
五、现实应用
1. 材料科学:Pb²⁺ 基钙钛矿(如 MAPbI₃)在光伏领域大放异彩,其稳定性部分源于 6s² 惰性对的立体化学活性(孤对电子效应)。
2. 分析化学:NaBiO₃ 成为 Mn²⁺ 的特效氧化剂,依赖 Bi⁵⁺ 的强氧化性。
3. 环境与健康:Tl⁺ 的类钾性质使其易被生物体误吸收,造成剧毒;理解其 +1 价稳定性有助于解毒机制研究。
4. 核化学:Po 和 At 的化学研究极度困难,但惰性电子对效应帮助预测其可能的价态与化合物形式。
惰性电子对效应看似是一个关于“电子懒惰”的简单描述,实则揭示了高速运动下的电子如何被原子核“捕获”,从而改写元素的化学命运。它告诉我们:在重元素的世界里,爱因斯坦的相对论不再是遥远的天体物理,而是试管中真实发生的化学驱动力。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
我国著名化学家徐光宪先生提出关于轨道能量的(n+0.7l)近似规律...
由于其他电子对某一电子的排斥作用而抵消了一部分核电荷,从...
元素周期律是化学的基石,而有效核电荷(Z eff 则是解开周期律...
一、为何硒酸能氧化盐酸,而硫酸不能? 在元素周期表中,同族...
一、一个“懒惰”的电子对如何改写元素命运? 在元素周期表的...
为什么元素周期表第8族不归到主族或副族中?是为了与7个主族...