
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、等电子体的定义
狭义等电子体:原子总数相同、价电子总数相同的分子或离子(高考主流考查范畴)。
广义等电子体:原子总数相同、电子总数相同的分子或离子(拓展内容,部分模拟题涉及)。
核心判断依据:原子总数相等;价电子总数(或电子总数)相等;
价电子:主族元素的价电子为最外层电子,过渡元素需考虑次外层 d 电子(高考一般不涉及过渡元素等电子体)。
二、等电子体的判断方法
1. 同族替换法
将分子中的某一原子替换为同主族元素的原子,原子总数和价电子总数不变。
示例:CO2→ CS2(O 和 S 同主族,价电子均为 6);CH4→ SiH4(C 和 Si 同主族,价电子均为 4)。
2. 电子转移法
在分子或离子间通过得失电子实现价电子总数相等,原子总数不变。
示例:CO(原子数 2,价电子数 4+6=10)→CN-
C、N 原子数 2,价电子数4+5+1=10,N 得 1 个电子);
N2(原子数 2,价电子数5+5=10)与CO、CN-互为等电子体。
3. 基团替换法
将分子中的原子团替换为价电子数相等的其他原子团。
示例:CH4(原子数 5,价电子数4+1×4=8)→NH4+(原子数 5,价电子数(5+1×4-1=8,失去 1 个电子)。
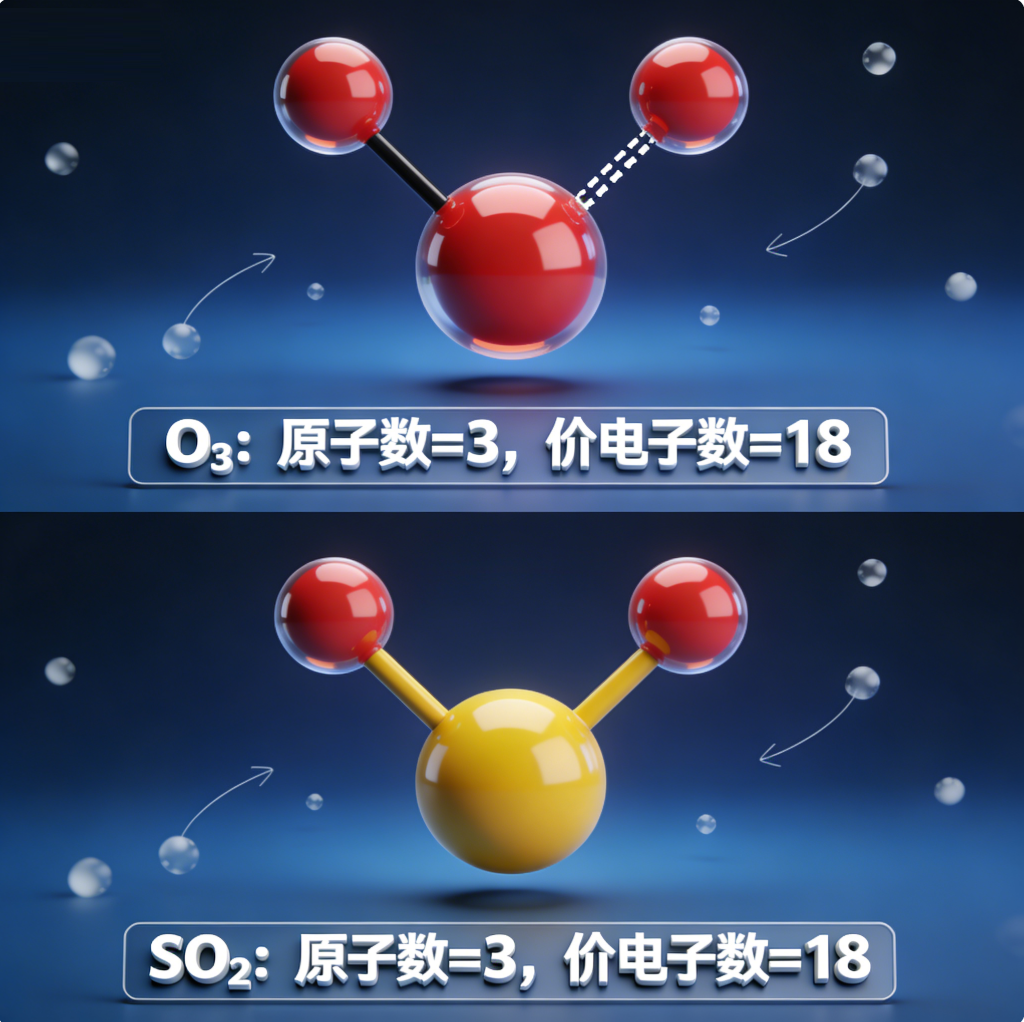
三、高考常考等电子体列表(原子总数 + 价电子总数)
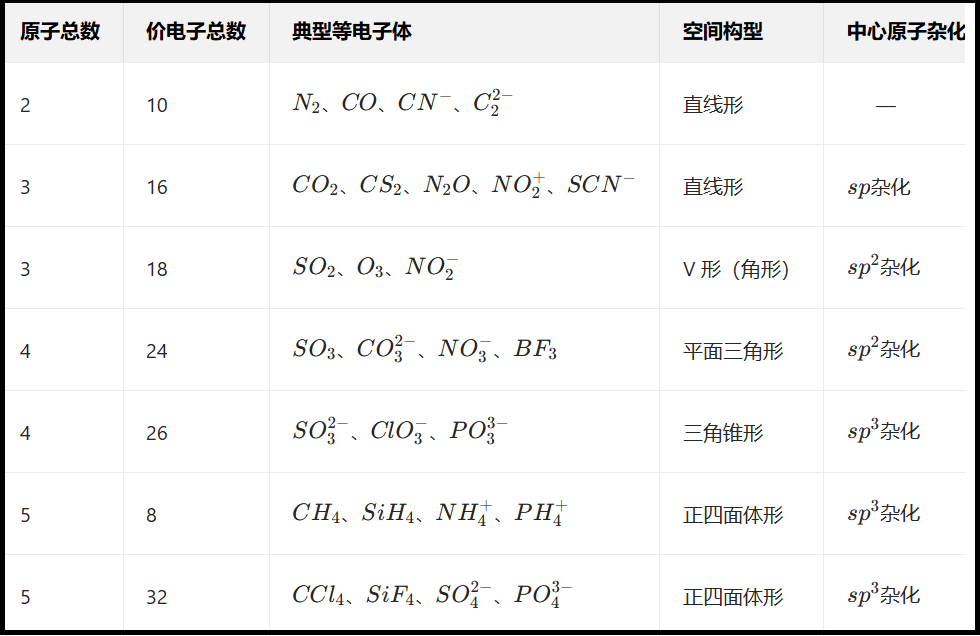
四、等电子体原理的核心应用(高考高频考点)
1. 预测分子或离子的空间构型
等电子体原理:互为等电子体的微粒具有相似的化学键特征和空间构型。
解题策略:遇到陌生微粒构型判断时,先找其等电子体,再根据熟悉微粒的构型推导。
示例:判断N2O构型 → 找等电子体CO2→ CO2是直线形 →N2O为直线形。
2. 分析化学键类型与强度
示例:N2和CO均含三键(1 个 σ 键 + 2 个 π 键),键能较大,化学性质相对稳定。
3. 解释物质的物理性质
等电子体的晶体类型相似,熔沸点、溶解性等物理性质可类比推导。
示例:CO2和CS2均为分子晶体,CS2相对分子质量更大,分子间作用力更强,熔沸点更高。
五、高考真题对接与解题策略
真题示例
(新课标卷)已知CO2是直线形分子,推测N2O的空间构型为______,理由是______。
答案:直线形;N2O 和CO2是原子总数相同、价电子总数相同的等电子体,等电子体具有相似的空间构型。
解题步骤
判断等电子体:明确目标微粒的原子总数和价电子总数;
寻找熟悉参照:匹配教材中常见的等电子体(如CO2、CH4等);
迁移构型与杂化:根据等电子体原理推导陌生微粒的结构与性质。
六、易错点辨析
混淆 “价电子总数” 与 “电子总数”
反例:CH4(电子总数 10)和NH3(电子总数 10)原子总数不同,不是等电子体;CH4和NH4+价电子总数均为 8,是等电子体。
忽略原子总数的前提
反例:SO42-(原子数 5)和PO43-(原子数 5)是等电子体,但SO42-和CO32-(原子数 4)不是。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
归纳 过二硫酸根 中的过氧键(—O—O—)与过氧化氢结构式(...
电子效应通过改变电子云分布(尤其是化学键的极性、电子离域程...
1、真题呈现: (2023山东--节选)ClO2中心原子为Cl,Cl2O中心原子...
一、螯合物的定义与特点 1. 定义 螯合物是由中心金属离子(或...
一、无机阴离子配体:铜配合物的基础“搭建模块” 无机阴离子...
...