
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
近几年的高考题中,在物质制备及化工流程题中有关物质的分离、提纯成为命题热点。其中,过滤、蒸馏、冷凝及洗气是常用的方法,因而也成为了高考命题的热点,尤其是对这些方法创新应用的考查,更是炙手可热。
一、基本含义
1、过滤
通过特殊装置将流体提纯净化的过程,过滤的方式很多,使用的物系也很广泛,固—液、固—气、大颗粒、小颗粒都可以。
过滤是在推动力或者其他外力作用下悬浮液(或含固体颗粒发热气体)中的液体(或气体)透过介质,固体颗粒及其他物质被过滤介质截留,从而使固体及其他物质与液体(或气体)分离的操作。
简言之,过滤就是用滤纸或其他多孔材料分离悬浮在液体或气体中的固体颗粒,中学阶段介绍的过滤是利用物质的溶解性差异,将液体和不溶于液体的固体分离开来的一种方法,如用过滤法除去粗食盐中少量的泥沙。
2、蒸馏
蒸馏是一种热力学的分离工艺,它利用混合液体或液—固体系中各组分沸点不同,使低沸点组分蒸发,再冷凝以分离整个组分的操作过程,是蒸发和冷凝两种单元操作的联合。与其它的分离手段,如萃取、过滤结晶等相比,它的优点在于不需使用系统组分以外的其它溶剂,从而保证不会引入新的杂质。
蒸馏有两层含义:蒸发或挥发,常温下不明显,加热到沸点后,可以明显观察到;遇冷后蒸汽又变为液体,俗称馏出液。也就是将液体加热至沸腾,再把产生的蒸气导入冷凝管,使之冷却凝结成液体的一种蒸发、冷凝的过程。
蒸馏是分离沸点相差较大的混合物的重要操作技术,尤其是对于液体混合物的分离有重要的实用意义。蒸馏条件有二:(1)液体混合物,(2)各组分沸点不同。
3、冷凝
冷凝是使热物体的温度降低而发生状态变化的过程,通常指物质从气态变成液态的过程。冷凝和蒸发是作用相反的两个操作。在化工生产中,实现冷却、冷凝的介质是冷水或者盐水。
中学阶段介绍的冷凝是与蒸馏相结合,二者联合使用的一种分离方法。
4、洗气
洗气是把混合气体中杂质气体除去的过程,中学阶段常分为干燥和除杂。比如用浓硫酸除去混在氧气中的水蒸气就是干燥,洗气的对象为水蒸气;再如除去氮气中含有的少量二氧化碳,可通过盛氢氧化钠溶液的洗气瓶,这就是除杂,洗气的对象为二氧化碳。
洗气的方式分为物理方式和化学方式。气体中需要被去除的杂质在洗液中溶解度较大,并且杂质气体仅仅是单纯的溶解于洗液,就选择物理方式,如:除去氧气中含有的少量氨气;杂质气体可以与水发生反应从而生成新的化合物溶解在洗液中或生成沉淀析出,就选择化学方式。如:除去氧气中含有的少量三氧化硫,杂质气体为三氧化硫,氯化钡溶液做洗液,生成硫酸钡沉淀。
二、创新应用
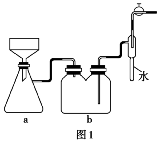
1.过滤装置的创新:抽滤(图1)
由于水流的作用,使装置A、B中气体的压强减小,故过滤速度加快。
2.蒸馏、冷凝装置的创新(图2、图3、图4)
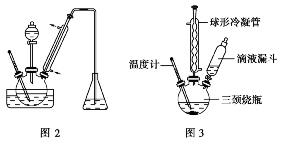
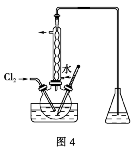
由于冷凝管竖立,使液体混合物能冷凝回流,若以此容器作反应容器,能使反应物循环利用,从而提高了反应物的转化率。
3.洗气的创新——双耳球吸收法(图5)
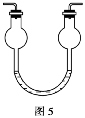
由于双耳球上端球形容器的容积较大,能有效地防止倒吸,故该装置既能除去气体中的气态杂质,又能防止倒吸。
典例剖析
环己酮是一种重要的化工原料,实验室常用下列原理和装置来制备(部分夹持仪器未画出):
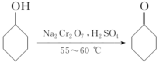
环己醇、环己酮和水的部分物理性质见下表(括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点):
| 物质 | 相对分子质量 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
环己醇 | 100 | 161.1(97.8) | 0.962 4 | 微溶于水 |
环己酮 | 98 | 155.6(95) | 0.947 8 | 微溶于水 |
水 | 18 | 100.0 | 0.998 2 |
据此回答下列问题:
(1)已知合成环己酮的反应是放热反应,反应剧烈将导致体系温度迅速上升,副反应增多。实验时,先在合成装置中加入5.2 mL (5 g)环己醇和几粒沸石,再加入酸性Na2Cr2O7溶液。酸性Na2Cr2O7溶液的加料方式为__________(填字母)。
A.一次性加入 B.缓慢加入 C.无所谓,怎样加入都可以
(2)若酸性Na2Cr2O7溶液的体积为35 mL,则应选取__________ (填“100 mL”或“250 mL”)的三颈烧瓶。
(3)反应完成后,加入适量水,蒸馏,收集95~97℃的馏分(设为A),其主要成分是__________的混合物;在馏分a中加入氯化钠固体至饱和,静置、分液,得有机层(设为B)。加入氯化钠固体的作用是__________;在有机层B中加入无水硫酸镁固体,充分作用后过滤,加入无水硫酸镁的作用是__________ ,然后进行蒸馏。
(4)合成装置中冷凝水应从__________(填“a”或“b”)口进入;精制装置中的两处错误是_________________。
(5)若最终得到环己酮的质量为3.43 g,则环己酮的产率是__________。
解析:(1)酸性Na2Cr2O7溶液应缓慢加入,防止剧烈反应,导致温度过高。
(2)反应液的总体积是40.2 mL,液体体积一般不能超过容器容积的1/2,所以应选择100 mL 三颈烧瓶。
(3)95℃时得到环己酮和水的恒沸溶液,所以95~97℃的馏分是环己酮和水的混合物;环己酮的密度与水接近,不容易分层。加入NaCl可增加水的密度,有利于分层;加入无水硫酸镁是为了除去残留在环己酮中少量的水。
(4)冷却剂应从A口进入。
(5)5 g 环己醇理论上得到4.9 g 环己酮,所以产率是3.43 g÷4·9 g×100%=70%。
答案: (1)B (2)100 mL (3)环己酮和水 增加水层的密度,有利于液体分层 除去残留在环己酮中的水 (4)a 温度计的水银球插入到溶液中;冷凝水进、出口方向颠倒 (5)70%
走近高考
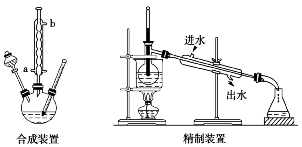
1.(2021·湖南选择考,13)1-丁醇、溴化钠和70%的硫酸共热反应,经过回流、蒸馏、萃取分液制得1-溴丁烷粗产品,装置如图所示:
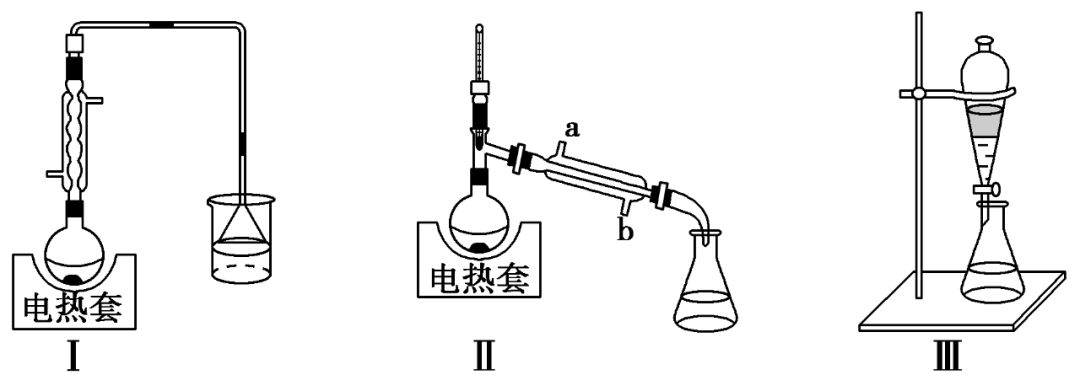
已知:CH3(CH2)3OH+NaBr+H2SO4(Δ)=CH3(CH2)3Br+NaHSO4+H2O
下列说法正确的是( )
A.装置Ⅰ中回流的目的是为了减少物质的挥发,提高产率
B.装置Ⅱ中a为进水口,b为出水口
C.用装置Ⅲ萃取分液时,将分层的液体依次从下放出
D.经装置Ⅲ得到的粗产品干燥后,使用装置Ⅱ再次蒸馏,可得到更纯的产品
答案:AD
解析:A.浓硫酸和NaBr会产生HBr,1-丁醇以及浓硫酸和NaBr产生的HBr均易挥发,用装置I回流可减少反应物的挥发,提高产率,A正确;B.冷凝水应下进上出,装置Ⅱ中b为进水口,a为出水口,B错误;C.用装置Ⅲ萃取分液时,将下层液体从下口放出,上层液体从上口倒出,C错误;D.由题意可知经装置Ⅲ得到粗产品,由于粗产品中各物质沸点不同,再次进行蒸馏可得到更纯的产品,D正确。
2.(2020·山东等级考,8)实验室分离Fe3+和Al3+的流程如下:
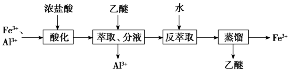
已知Fe3+在浓盐酸中生成黄色配离子[FeCl4]-,该配离子在乙醚(Et2O,沸点34.6℃)中生成缔合物Et2O·H+·[FeCl4]-。下列说法错误的是( )
A.萃取振荡时,分液漏斗下口应倾斜向下
B.分液时,应先将下层液体由分液漏斗下口放出
C.分液后水相为无色,说明已达到分离目的
D.蒸馏时选用直形冷凝管
答案:A
解析:A.萃取振荡时,分液漏斗下口应倾斜向上,A错误;B.分液时,密度大的液体在下层,密度小的液体在上层,下层液体由分液漏斗下口放出,下层液体放完后,密度小的上层液体从分液漏斗上口倒出,B正确;C.Fe3+在浓盐酸中生成黄色配离子,该离子在乙醚中生成缔合物,乙醚与水不互溶,故分液后水相为无色,则水相中不再含有Fe3+,说明已经达到分离目的,C正确;D.蒸馏时选用直形冷凝管,能使馏分全部转移到锥形瓶中,而不会残留在冷凝管中,D正确。
3.(2019·全国卷Ⅱ,28节选)咖啡因是一种生物碱(易溶于水及乙醇,熔点234.5℃,100℃以上开始升华),有兴奋大脑神经和利尿等作用。茶叶中含咖啡因约1%~5%、单宁酸(Ka约为10-6,易溶于水及乙醇)约3%~10%,还含有色素、纤维素等。实验室从茶叶中提取咖啡因的流程如图所示。
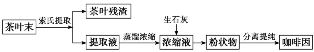
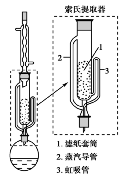
索氏提取装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与茶叶末接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对茶叶末的连续萃取。回答下列问题:
(1)提取过程不可选用明火直接加热,原因是_________________。
与常规的萃取相比,采用索氏提取器的优点是_________________。
(2)提取液需经“蒸馏浓缩”除去大部分溶剂。与水相比,乙醇作为萃取剂的优点是___________ 。“蒸馏浓缩”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管之外,还有___________(填标号)。
A.直形冷凝管 B.球形冷凝管C.接收瓶D.烧杯
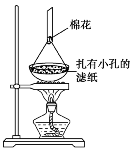
(3)可采用如图所示的简易装置分离提纯咖啡因。将粉状物放入蒸发皿中并小火加热,咖啡因在扎有小孔的滤纸上凝结,该分离提纯方法的名称是___________ 。
答案: (1)乙醇易挥发,易燃 使用溶剂量少,可连续萃取(萃取效率高)
(2)乙醇沸点低,易浓缩 AC
(3)升华
解析:(1)由于溶剂乙醇具有挥发性和易燃性,因此在提取过程中不可用明火直接加热。本实验中采用索氏提取器的优点是溶剂乙醇可循环使用,能减少溶剂用量,且萃取效率高。(2)提取液需经“蒸馏浓缩”除去大部分溶剂,与水相比,乙醇作为萃取剂具有沸点低和易浓缩的优点。“蒸馏浓缩”需选用的仪器除了所给仪器外,还有直形冷凝管和接收瓶(如锥形瓶)。(3)结合分离提纯咖啡因的装置及将粉状物放入蒸发皿并小火加热,咖啡因凝结在扎有小孔的滤纸上,可知该分离提纯的方法为升华。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、核心总纲(必背) 三者同源,均为物理变化(无新物质生成...
结晶与重结晶是高考实验题、工艺流程题必考分离提纯手段,命...
在高中化学的分离提纯板块,萃取与反萃取是实验操作和工艺流...
在高中化学实验中,固液分离是物质分离提纯的核心操作,而过...
在高中化学学习中,结晶是分离和提纯物质的核心操作之一。无...
1.过滤 原理:根据固体的溶解度不同,将不溶性固体从溶液中分离...