
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
分子的立体结构是指其原子在空间的排布,可以用现代实验手段测定。例如,通过分子或离子的振动光谱(红外或拉曼光谱)可确定分子或离子的振动模式,进而确定分子的立体结构;通过X-衍射、电子衍射、中子衍射、核磁共振等技术也可测定分子的立体结构。
实验证实,属于同一通式的分子或离子,其结构可能相似,也可能完全不同。例如,H2S和H2O属同一通式H2A,结构很相似,都是角形分子,仅夹角度数稍有差别;而CO32-和SO32-虽属同一通式AO32-,结构却不同:前者是平面形,后者是三角锥形,前者有p-pπ键而后者有d-pπ键。
早在1940年,希吉维克(Sidgwick)和坡维尔(Powell)在总结实验事实的基础上提出了一种简单的理论模型,用以预测简单分子或离子的立体结构。这种理论模型后经吉列斯比(R.J.Gillespie)和尼霍尔姆(Nyholm)在20世纪50年代加以发展,定名为价层电子对互斥模型,简称VSEPR(Valence Shell Electron Pair Repulsion)模型。我们不难学会用这种模型来预测分子或离子的立体结构。当然,我们不应忘记,这一模型绝不可能代替实验测定,也不可能没有例外。不过,统计表明,对于我们经常遇到的分子或离子,特别是以非金属原子为中心的单核(即单中心)分子或离子,用这一理论模型预言的立体结构很少与事实不符。
VSEPR模型的要点:
(1)用通式AXnEm来表示所有只含一个中心原子的分子或离子的组成,式中A表示中心原子,X表示配位原子(也叫端位原子),下标n表示配位原子的个数,E表示中心原子上的孤对电子对,下标m是电子对数。已知分子或离子的组成和原子的排列顺序时,m值可用下式确定。
m=(A的族价-X的化合价×X的个数+/-离子电荷相应的电荷数)/2
例如:

可以这样理解这个通式:中心原子的族价等于它的价电子总数,中心原子与端位原子键合用去的电子数取决于端位原子的个数和端位原子的化合价,如果是离子,正离子的电荷相当于中心原子失去的电子,负离子的电荷相当于中心原子得到的电子,因此,用上式计算得到的数值m就是中心原子未用于键合的孤对电子对数。(有时,计算出来的m值不是整数,如NO2,m=0.5,这时应当作m=1来对待,因为,单电子也要占据一个电子轨道。)
(2)通式AXnEm里的(n+m)的数目称为价层电子对数,令n+m=z,则可将通式AXnEm改写成另一种通式AYz;VSEPR模型认为,分子中的价层电子对总是尽可能地互斥,均匀地分布在分子中,因此,z的数目决定了一个分子或离子中的价层电子对在空间的分布,由此可以画出VSEPR理想模型:
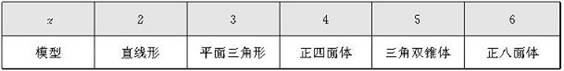
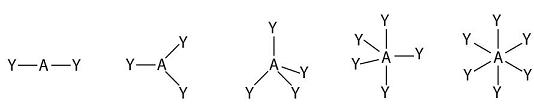
图2-2 VSEPR理想模型
由此可见,VSEPR模型的“价层电子对”指孤对电子对和σ键电子对,不包括π电子对,考虑到孤对电子和键合的σ电子对的电子云图像具有相同的对称性,我们不妨把它们合称为σ轨道,那么,价层电子对互斥模型就是分子中σ轨道的电子在三维空间中互相排斥,达到尽可能对称的图像。
(3)通常所说的“分子立体构型”是指分子中的原子在空间的排布,不包括孤对电子对,因此,在获得VSEPR理想模型后,需根据AXn写出分子立体构型,只有当AXnEm中的m=0时,即AYz=AXn时,VSEPR模型才是分子立体构型,否则,得到VSEPR模型后要略去孤对电子对,才得到分子立体构型,例如,H2O、NH3、CH4都是AY4,它们的分子立体构型如图2-3所示。

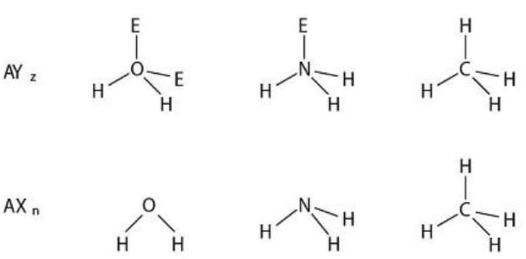
图2-3VSEPR理想模型与分子立体结构的关系(举例)
可见,对于AXn而言,分子的立体结构就不一定越对称越好了,否则会以为水分子应为直线分子,氨应为平面三角形分子,换句话说,只有把孤对电子对考虑在内才能得出正确的分子立体模型,这正是VSEPR理论的成功之处。
(4)AYz中的z个价层电子对之间的斥力的大小有如下顺序:
i. l-l>>l-b>b-b(l为孤对电子对;b为键合电子对)
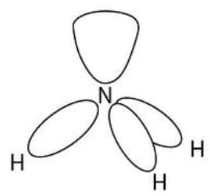
图2-4 孤对电子对与键合电子对的斥力不同使理想模型发生畸变
这一斥力顺序是经常要考虑的。可以这样来理解这一斥力顺序:键合电子对受到左右两端带正电的原子核的吸引,而孤对电子对只受到一端原子核吸引,相比之下,孤对电子对较“胖”,占据较大的空间,而键合电子较“瘦”,占据较小的空间(如图2-4)。
此外,有时还要考虑到如下几种顺序:
ii. t-t>t-d>d-d>d-s>s-s(t-三键,d-双键,s-单键)
iii. χw-χw>χw-χs>χs-χs(χ代表配位原子的电负性,下标w为弱,s为强)
iv. 处于中心原子的全充满价层里的键合电子之间的斥力大于处在中心原子的未充满价层里键合电子之间的斥力。
价层电子对之间的以上“斥力顺序”使分子或离子的立体构型偏离由AYz确立的理想模型而适当畸变;当理想模型不止一个时,还决定了哪种构型更为稳定。这些顺序规则中,最经常要考虑的,最重要的,是第一种斥力顺序。
[例2-1]试用VESPR模型预测H2O的立体构型。
[解](1)H2O属AX2E2=AY4
(2)VSEPR理想模型为正四面体,价层电子对间夹角均为109°28′。
(3)分子立体构型(指H2O而不是H2OE2)为角形(非线形分子)。
(4)根据斥力顺序(i),应有:∠l-O-l>∠l-O-H>∠H-O-H
结论:水分子的立体结构为角形,∠H-O-H小于109°28′。
[例2-2]用VESPR模型预测SO2Cl2的立体构型。
[解]SO2Cl2属AX4E0=AY4,VSEPR理想模型为正四面体,因S=O键是双键,S—Cl键是单键,据顺序(ii),分子立体模型应为:∠O-S-O>109°28′∠Cl-S-Cl<∠O-S-Cl<109°28′
结论:SO2Cl2的立体结构为正四面体畸变形——四面体形。
[例2-3]实测值:SO2f2中∠F-S-F为98°,SO2Cl2中∠Cl-S-Cl为102°,为什么后者角度较大?
[解]这种差别可以用斥力顺序(iii)来解释。
[例2-4]NH3和PH3都是AX3E=AY4,故分子(AX3)均为三角锥形。实测:氨分子中∠H-N-H为106.7°,膦分子中∠H-P-H为93.5°,为什么这两种分子的角度有这种差别?
[解]这种差别可以用斥力顺序(iv)来解释。

图2-5 SF4分子的可能立体结构
[例2-5]SF4属AX4E1=AY5,其VSEPR理想模型为三角双锥体,排除孤对电子的分子立体结构有两种可能的模型(由于孤对电子的位置不同):(Ⅰ)型为类似金字塔的三角锥体(孤对电子对占据AY5的三角双锥的一个锥顶,又叫极顶位置);(Ⅱ)型为跷跷板型(孤对电子对占据三角双锥的“赤面位置”)(如图2-5)。哪一种结构更合理呢?
[解]在(Ⅰ)型里有3个呈90°的∠l-S-F和3个呈90°的∠F-S-F,而在(Ⅱ)型里只有两个呈90°的∠l-S-F和4个呈90°的∠F-S-F,由于孤对电子的斥力较大,因而(Ⅱ)型比(Ⅰ)型稳定。需要指出的是:该分子中120°夹角的电子对间的斥力与90°夹角的电子对间的斥力相比小得可以忽略不计,故无须加以考虑。实测SF4分子呈(Ⅱ)型。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、先定框架:4步快速判定有没有大π键 1. 看结构 :必须是平...
目前高考试题对对映异构的考查主要集中在有机分子中手性碳原...
...
...
配合物的配位数是指直接同中心离子(或原子)配位的原子数目。...
分析: 依据价层电子对数计算公式分析, 可得价层电子对数=...