
|
学习小专题 |

|
学习小专题 |
 [探讨与扩展a] 什么是对角线规则? 作者:化学自习室 来源:未知 日期:2019-11-11 15:58:59 点击:18214 所属专题:对角线规则
[探讨与扩展a] 什么是对角线规则? 作者:化学自习室 来源:未知 日期:2019-11-11 15:58:59 点击:18214 所属专题:对角线规则
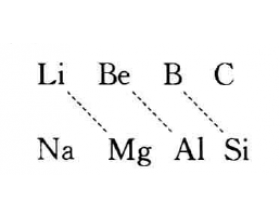
在周期表中某一元素的性质和它左上方或右下方的另一元素 性质的相似性,称对角线规则。这种相似性较明显地表现在Li和 Mg、Be和Al、B和Si三对元素之间。C和P、N和S、O和Cl 没有明显地存在这种关系。 (1) L i和Mg性质的相似性 ①Li和Mg在过量的氧气中燃烧,只能形成氧化物Li 2...
 [探讨与扩展b] 为什么原子核外电子最外层不超过8个,次外层不超过18个? 作者:化学自习室 来源:未知 日期:2021-12-17 09:36:05 点击:12774 所属专题:核外电子分层排布 构造原理
[探讨与扩展b] 为什么原子核外电子最外层不超过8个,次外层不超过18个? 作者:化学自习室 来源:未知 日期:2021-12-17 09:36:05 点击:12774 所属专题:核外电子分层排布 构造原理
原子核外的电子排布,最外层不超过8个,次外层不超过18 个,这种构型是由于电子能级发生交错而造成的。 由各亚层能量高低顺序:1s, 2s2p, 3s3p, 4s3d4f,5s4d5p, 6s4f5d6p……可知,如最外层是第四层,则在第五能层出现之前仅有4s和4p轨道可填充电子,最多也只为8个。同...
 [注解与辨疑d] 用电离能和电负性判断金属性和非金属性强弱哪种数据更可靠? 作者:化学自习室 来源:未知 日期:2019-06-10 21:00:59 点击:2432 所属专题:电离能 电负性
[注解与辨疑d] 用电离能和电负性判断金属性和非金属性强弱哪种数据更可靠? 作者:化学自习室 来源:未知 日期:2019-06-10 21:00:59 点击:2432 所属专题:电离能 电负性
用电离能和电负性判断金属性和非金属性强弱哪种数据更可靠? 答:电负性应用于判断金属性和非金属性强弱更可靠。 第二周期.. Be的第一电离能为899kJ/mol,B的第一电离能为800kJ/mol,原因是Be是2s轨道全满,B却多一个p电子,这个电子在p轨道里没有半满;N的第一电离能为142...
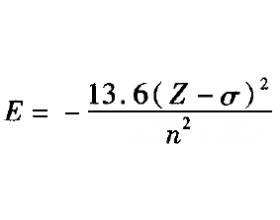 [注解与辨疑d] 按构造原理最后填充的电子在反应中是否最先失去? 作者:化学自习室 来源:未知 日期:2019-06-10 21:40:10 点击:1587 所属专题:构造原理
[注解与辨疑d] 按构造原理最后填充的电子在反应中是否最先失去? 作者:化学自习室 来源:未知 日期:2019-06-10 21:40:10 点击:1587 所属专题:构造原理
按构造原理最后填充的电子在反应中是否最先失去? 答:不一定。例如铜的电子排布式为1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 1 或[ Ar]3d 10 4s 1 ,电子先填入4s后再填入3d,在失去电子成为离子时却先失去4s电子。 定性分析 :原因是失去电子成为离子,核电荷数不变电子数减...
 [注解与辨疑d] Fe参加反应时,为什么先失去最外层电子,而非能量最高的电子? 作者:化学自习室 来源:未知 日期:2021-12-28 08:47:49 点击:4694 所属专题:铁的失电子
[注解与辨疑d] Fe参加反应时,为什么先失去最外层电子,而非能量最高的电子? 作者:化学自习室 来源:未知 日期:2021-12-28 08:47:49 点击:4694 所属专题:铁的失电子
基态 26 Fe原子的核外电子排布式是[Ar]3d 6 4s 2 ,Fe 2+ 的核外电子排布式是 [Ar]3d 6 ,学生不明白:Fe原子参与反应时,为什么先失去 4s上的电子,而不是根据“能量越低越稳定”原则,失去能量最高的3d上的电子? 多电子原子中,电子具有的能量 E 决定于主量子数 n ...
 [注解与辨疑d] 为什么钾的密度比钠小? 作者:化学自习室 来源:未知 日期:2019-04-06 16:05:30 点击:16008 所属专题:金属钠 金属钾 体心立方堆积
[注解与辨疑d] 为什么钾的密度比钠小? 作者:化学自习室 来源:未知 日期:2019-04-06 16:05:30 点击:16008 所属专题:金属钠 金属钾 体心立方堆积
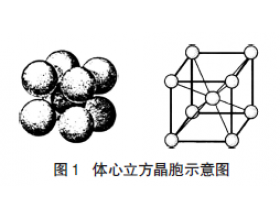
通常情况下,同主族的单质的密度随着序数的增大而增大。但在常温下,钠的密度为 0.971g·cm-3,钾为 0.86g·cm-3。为什么钾的密度反而比钠小? 钠、钾的晶胞属于体心立方堆积(如图 1),每个晶胞均含有 2 个原子。 根据晶胞结构可得出两种金属单质密度的计 算 公式: M 为...
 [注解与辨疑d] 与电子排布的有关概念辨析 作者:胡嘉谋 来源:未知 日期:2018-11-28 09:50:09 点击:3165 所属专题:核外电子排布
[注解与辨疑d] 与电子排布的有关概念辨析 作者:胡嘉谋 来源:未知 日期:2018-11-28 09:50:09 点击:3165 所属专题:核外电子排布
1.电子云。 它是电子在原子核外单位体积内出现概率的大小,是核外电子运动状态的形象化描述。电子云图中小黑点的疏密表示电子在原子核外单位体积内出现的概率大...
 [注解与辨疑d] 为什么第四周期钙以后过渡元素的首先失去4s电子而不是3d电子? 作者:化学自习室 来源:未知 日期:2021-12-29 09:56:58 点击:1789 所属专题:铁的失电子
[注解与辨疑d] 为什么第四周期钙以后过渡元素的首先失去4s电子而不是3d电子? 作者:化学自习室 来源:未知 日期:2021-12-29 09:56:58 点击:1789 所属专题:铁的失电子
...
 [注解与辨疑d] CN-作为配体,哪个原子来配位? 作者:化学自习室 来源:未知 日期:2017-10-07 22:16:16 点击:42541 所属专题:配体
[注解与辨疑d] CN-作为配体,哪个原子来配位? 作者:化学自习室 来源:未知 日期:2017-10-07 22:16:16 点击:42541 所属专题:配体
CN - 是一常见的强配体。从氰根离子的电子结构可以看出, 氰根离子与一氧化碳属等电子体, 结构颇为类似。尽管氮的电负性较大, 但碳氮间电子云偏向于碳原子, 致使碳原子更易提供孤对电子。故氰根离子作配体时, 碳在绝大多数情况下都是配位原子(只有极个别例子, 在...
 [探讨与扩展a] 原子的最外层电子数为什么不超过8个? 作者:章文 来源:未知 日期:2018-07-17 13:18:03 点击:5500 所属专题:核外电子排布 最外层电子
[探讨与扩展a] 原子的最外层电子数为什么不超过8个? 作者:章文 来源:未知 日期:2018-07-17 13:18:03 点击:5500 所属专题:核外电子排布 最外层电子
由于能级交错的原因,E(nd)E(n+1)s。当ns和np充满时(共4个轨道,最多容纳8个电子),多余电子不是填入nd,而是首先形成新电子层,填入(n+1)s轨道中,因此,最外层电子数不可能超过8个。...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、为啥杂化轨道s成分越大,电负性越强? 电负性不是固定不...
一、人教版 二、鲁科版 三、苏教版 四、沪科版 五、练习 (该...
电负性是描述元素原子在化合物中吸引键合电子能力的标度,是...
1.对角线规则 对比周期系中元素性质,发现: 左上~右下,对角线元...
一、为何氮不像磷,氧不像硫? 在元素周期表中,同族元素自上...
...
原子核外电子的真实运动状态是我们肉眼看不到的,但是可以通...
铜原子(Cu)的基态电子排布为[Ar] 3d4s,失去一个电子形成亚铜...