
|
学习小专题 |
 什么是第四周期反常?
日期:2026-02-25 21:24:40
点击:227
好评:0
什么是第四周期反常?
日期:2026-02-25 21:24:40
点击:227
好评:0
一、为何硒酸能氧化盐酸,而硫酸不能? 在元素周期表中,同族元素自上而下,含氧酸的氧化性通常呈现一定规律。然而,一些反常的现象: 1.H₂SeO₄(硒酸)能将 HCl 氧化为 Cl₂,表现出强...
 第二周期:小尺寸、高张力与多重键
日期:2026-02-25 21:24:15
点击:272
好评:0
第二周期:小尺寸、高张力与多重键
日期:2026-02-25 21:24:15
点击:272
好评:0
一、为何氮不像磷,氧不像硫? 在元素周期表中,同族元素自上而下通常呈现性质的渐变:原子半径增大、电负性减小、金属性增强。然而,第二周期元素(Li、Be、B、C、N、O、F) 却屡屡打破...
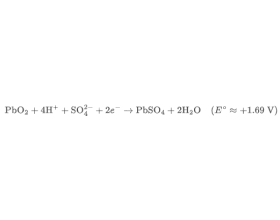 第六周期:惰性电子对效应
日期:2026-02-25 21:23:52
点击:376
好评:0
第六周期:惰性电子对效应
日期:2026-02-25 21:23:52
点击:376
好评:0
一、一个“懒惰”的电子对如何改写元素命运? 在元素周期表的底部,第六周期的 p 区元素——铊(Tl)、铅(Pb)、铋(Bi)、钋(Po)和砹(At)——展现出一种奇特的化学行为:它们似乎“...
 教材分析(物质结构与性质):原子结构与元素的性质
日期:2023-09-04 15:22:16
点击:634
好评:0
教材分析(物质结构与性质):原子结构与元素的性质
日期:2023-09-04 15:22:16
点击:634
好评:0
一、原子结构与元素周期表 1 、元素周期律、元素周期系和元素周期表 ( 1 )元素性质随着原子序数递增发生周期性的重复,这一规律被称作 元素周期律 。 原子序数:按相对原子质量(后来改为核电荷数)从小到大的顺序将元素排列起来,得到一个元素序列,并从最轻的元素氢...
 元素性质专题专练
日期:2021-03-08 09:31:48
点击:313
好评:0
元素性质专题专练
日期:2021-03-08 09:31:48
点击:313
好评:0
元素的性质专题专练...
 元素性质变化规律注解与扩展
日期:2021-01-18 09:56:33
点击:2082
好评:0
元素性质变化规律注解与扩展
日期:2021-01-18 09:56:33
点击:2082
好评:0
由于原子的电子层结构的周期性,与之相关的元素的基本性质如原子半径、电离能、电子亲和能、电负性等,也呈现明显的周期性。 1.原子半径 1)原子半径的概念 根据原子与原子间作用力的不同,原子半径一般可分为三种:共价半径、金属半径和范德华半径。 共价半径是指同种元素两个原...
 原子结构和元素性质方面特殊
日期:2020-11-03 08:58:24
点击:11226
好评:0
原子结构和元素性质方面特殊
日期:2020-11-03 08:58:24
点击:11226
好评:0
1. 原子一般由质子、中子和核外电子构成。但 只由质子和电子构成。 2. 金属元素的原子最外层电子数一般小于4,而非金属元素的原子最外层电子数一般大于或等于4。但H、He、B的原子最外层电子数均小于4,其中H、B为非金属元素,He为稀有气体元素;虽然Ge、Sn、Pb、Sb、Bi...
 有关元素性质的几个问题集
日期:2016-01-24 17:02:07
点击:6122
好评:0
有关元素性质的几个问题集
日期:2016-01-24 17:02:07
点击:6122
好评:0
1、元素的金属性和金属活动性有什么区别? 元素的金属性是元素固有的性质。它反映了元素的原子失去电子成为阳离子能力的大...
 第VIII族元素性质研究
日期:2013-03-11 17:13:15
点击:11700
好评:0
第VIII族元素性质研究
日期:2013-03-11 17:13:15
点击:11700
好评:0
第VIII族元素在周期表中位置的特殊性与它们之间性质的类似和递变关系相联系的。在九种元素中,虽然也存在着一般的垂直相似性,如铁、钌、锇,但水平相似性则更为突出。如铁、钴、镍。因此,为了便于研究,通常把这九种元素分成两组,把位于第4周期的铁、钴、镍三种元素称为...
 元素性质与单质性质的区别与联系
日期:2012-11-06 16:53:55
点击:3430
好评:0
元素性质与单质性质的区别与联系
日期:2012-11-06 16:53:55
点击:3430
好评:0
元索是构成物质的材料。它只能以游离态(单质)或化合态(化合物)存在于自然界中。研究元素的性质就是研究它的原子半径、化合价等基本性质及由此引起的它的游离态(单质)化合态(化合物)的各种性质。 单质是由同种元素构成的具体成品。它是客观存在的实体。元素的一些性质...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。