
|
ѧϰСר�� |

|
ѧϰСר�� |
 [ע�������e] �����ͬ���칹���С���ʽ���͡���ʽ����ʲô��˼? ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-04-20 08:21:59 �����2299 ����ר�⣺�����ṹ
[ע�������e] �����ͬ���칹���С���ʽ���͡���ʽ����ʲô��˼? ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-04-20 08:21:59 �����2299 ����ר�⣺�����ṹ
��������λ�İ�����������У��ر���d 3 ��d 6 �ṹ�Ľ��������γɵķdz��ȶ��������������ܣ� ����һ������λ�������������м��ֽṹ�أ� ���ȣ���������ʶһ���������塣 �������壬һ�� �������� ����Ϊ�������Σ�����Ϊ������ǣ� ������ �ĶԽ���Ϊ�����Σ���...
 [ע�������e] ΪʲôNH3���۷е��H2O���۷е�͵öࣿ ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-03-10 10:49:55 �����1531 ����ר�⣺���02 �۷е� ��
[ע�������e] ΪʲôNH3���۷е��H2O���۷е�͵öࣿ ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-03-10 10:49:55 �����1531 ����ר�⣺���02 �۷е� ��
Ϊʲô NH 3 ���۷е�� H 2 O ���۷е�͵öࣿ ˮ�͵���Ԫ���⻯����۵㡢�е����ݼ��� 1 ���ɱ� 1 ��֪�� NH3 ���۵�ͷе�����ڴ�ͬ��Ԫ���⻯���������Ƶõ�����ֵ�� �� 1 һЩ�⻯����۵㡢�е����� �������� NH3 ���Ӽ�����������Ե�ʡ����ǣ� NH3 ���۷�...
 [ע�������e] ���ۼ��������ܽ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-01-02 14:07:54 �����10934 ����ר�⣺���ۼ�����
[ע�������e] ���ۼ��������ܽ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-01-02 14:07:54 �����10934 ����ר�⣺���ۼ�����
��ԭ�ӷ��� ����������ԭ�ӵķ��ӡ� ��ԭ�ӷ��ӵĻ�ѧ�� �������������˫���ļ����ҡ��У���������������ļ� �� ���ۼ������� �Ŧ� �����ɼ�ʱ��ԭ�ӹ���ؼ��ᣨ�ɼ�������ԭ�Ӽ�����߳�Ϊ���ᣩ������У��� �� ͷ��ͷ �� �ķ�ʽ����ͬ���ص����ص���ԭ�ӹ���Ƽ�...
 [̽������չa] Ϊʲô�Ȼ����ǹ��ۻ���� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-01-01 19:22:25 �����6702 ����ר�⣺�Ȼ��� ���ۻ�����
[̽������չa] Ϊʲô�Ȼ����ǹ��ۻ���� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-01-01 19:22:25 �����6702 ����ר�⣺�Ȼ��� ���ۻ�����
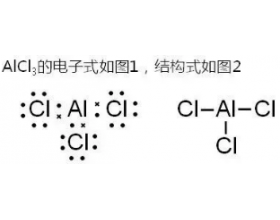
�Ȼ���(AlCl 3 )����������±�������AlBr 3 ��AlI 3 ��Ϊ���ۻ������AlF 3 �������ӻ���� �ڸ��л�ѧ֪ʶ����ǽ�����ѧ�����͵�ʱ��Ҳ���ᵽ����Ȼ��������ý����ͷǽ���֮�䣬�������Ӽ���ϵģ������Ȼ��������Թ��ۼ���ϵģ��������Dz��ܹ�ͨ���õ�...
 [ע�������e] ����λ���ۼ��йصļ������� ����:������ ��Դ:δ֪ ���ڣ�2021-11-07 18:19:41 �����2321 ����ר�⣺��λ��
[ע�������e] ����λ���ۼ��йصļ������� ����:������ ��Դ:δ֪ ���ڣ�2021-11-07 18:19:41 �����2321 ����ר�⣺��λ��
���ۼ���ָ�ɼ���ԭ�Ӽ�ͨ������1�Ի� ���Ӷ��γɵĻ�ѧ����ͨ������Щ���Ӷ����ɳɼ���ԭ��˫����ͬ�ṩ�ģ���H 2 ��HCl��H 2 O�еĹ��ۼ� ������ˣ���ô����û�������Ĺ��� �� ���乲�õ��Ӷ����ɲ���ɼ���ԭ�ӵ������ṩ���أ� ���ȣ�����������һ�� NH 4 �� ����...
 [ע�������e] ���»���������������������ʵ�Ӱ������Щ���ɣ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-08-23 20:29:44 �����2055 ����ר�⣺��������
[ע�������e] ���»���������������������ʵ�Ӱ������Щ���ɣ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-08-23 20:29:44 �����2055 ����ר�⣺��������
���»�����������Ƿ��Ӽ�����������ɲ��֡���ɺͽṹ���� �ķ��ӣ���Է�������Խ��ʱ���»���Խǿ������Է������������� �ȣ�����Ӽ���Խǿʱ���»���Խǿ����������е����Ե���ԭ���� �縺�Խ�ǿ��F��O��N��ԭ�Ӽ���һ���̶ȵĹ���ص����ã��������һ��ȷ��»���...
 [ע�������e] ��Щ���ʷ��Ӽ���Բ�������� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-08-23 20:07:05 �����13407 ����ר�⣺���02
[ע�������e] ��Щ���ʷ��Ӽ���Բ�������� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-08-23 20:07:05 �����13407 ����ר�⣺���02
��ν�����ָ��������ߵ縺��ԭ��X�Թ��ۼ�������Hԭ�ӣ� ����һ��������һ���ߵ縺��ԭ��Y֮������ľ������ú�һ���� �ȵ�ԭ�ӹ���ص����ã���ʾΪX��H��Y�� �ڷ����У��ܹ��ﵽ�㹻�{�ĵ縺�Ե�ԭ��ֻ��F��O��Nԭ�ӣ��� X��Y������F��O��Nԭ�ӡ��γ����ʱX��Y������ͬ...
 [ע�������e] ԭ�ӹ��ΪʲôҪ�����ӻ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-07-18 20:08:27 �����4632 ����ר�⣺�ӻ��������
[ע�������e] ԭ�ӹ��ΪʲôҪ�����ӻ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-07-18 20:08:27 �����4632 ����ר�⣺�ӻ��������
ԭ�ӹ��ΪʲôҪ�����ӻ��� �ӻ���ָ���γɷ���ʱ�� ����ԭ�ӵ��Ӱ�죬 ���ɲ�ͬ�������������ԭ�ӹ����������� ������ϳ�һ���¹���� ���ֹ��������ϵĹ��̽��ӻ��� ���γɵ��¹���ͳ�Ϊ�ӻ�������ӻ����������Ϊ���γɷ���ʱ��ͨ�����ڼ������ӻ�����ص�...
 [ע�������e] �������Ҽ��ͦм����ȶ��ԣ� ����:Է���� ��Դ:Ѱ��ѧ�����ı�Դ ���ڣ�2021-07-08 16:21:52 �����8302 ����ר�⣺�Ҽ� �м�
[ע�������e] �������Ҽ��ͦм����ȶ��ԣ� ����:Է���� ��Դ:Ѱ��ѧ�����ı�Դ ���ڣ�2021-07-08 16:21:52 �����8302 ����ר�⣺�Ҽ� �м�
�ۼ�������Ϊ���Ҽ���2��ԭ�ӹ���ԡ�ͷ��ͷ����ʽ����������ص����γɵĹ��ۼ����м���2������ƽ�е�ԭ�ӹ������2��py������ԡ��粢�硱��ʽ�Ӳ�������ص����γɵĹ��ۼ�������ͨ�������ص�������Զ���ڲ����ص������� ͬʱ�м��ĵ����Ʋ���Ҽ��ĵ�����������������...
 [ע�������e] �м�һ���ȦҼ�����С�� ����:«�� ��Դ:һ��«��ʦ ���ڣ�2021-06-15 08:54:22 �����2480 ����ר�⣺�м�
[ע�������e] �м�һ���ȦҼ�����С�� ����:«�� ��Դ:һ��«��ʦ ���ڣ�2021-06-15 08:54:22 �����2480 ����ר�⣺�м�
�� ��һ���� �� ������С����һ ������������������ѧ���������ģ� ����һ��ѡ�� 2 ���ʽṹ�����ʣ����� C ԭ���ڳɼ�ʱ������ C ԭ�ӵ� 2p x �����ͷ��ͷ�γ� �� �������� C ԭ�ӵ� 2p y �����ͷ��ͷ�γ� �� ���� ��������ѡ�� 3 �л������������ CH 2 =CH 2 �� ...
 ��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ�
��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ� ��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�
��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�[2025�����°�У2�¾�] 8 . �����ӽ�̽�����ʽṹ��������ѧϰ��ѧ����Ч����������...
������N�����ӻ���������ָ��ԭ��ͨ������ӻ��γɻ�ѧ���Ļ������ԭ�ӵĵ��ӹ���...
�ڻ�ѧ�о��Ѻ������ǹ��ۼ��Ķ��ѵ�������Ҫ��ʽ����������ز�ͬ��������Ҫ�ɼ��ܾ�...
ͨ�����ԣ�ͬ����Ԫ���γɵ�X-X�������϶��£����������������͡� ����Ԫ��...
����ѧʵ����һ��������ѧ���ۿ�������ϵĿγ̡�ʵ���û�ѧ��ʵ��ʵ�����ۿε�ѧ...
�ܷ��γ�����ġ��ӵ㡱��һ�����縺��...
1mol ��������������� һ������γɻ��� NH���ӽṹ Hԭ����Ϊ�������(����ߵ縺��...
��������(NO)�е�ԭ�ӵ��ӻ�����Ϊ sp�ӻ�������������£� 1.���� n (�ļ۲���Ӷ���...