
|
学习小专题 |

|
学习小专题 |
 [探讨与扩展j] 缓冲溶液解读 作者:化学自习室 来源:未知 日期:2019-11-15 10:58:19 点击:2469 所属专题:缓冲溶液
[探讨与扩展j] 缓冲溶液解读 作者:化学自习室 来源:未知 日期:2019-11-15 10:58:19 点击:2469 所属专题:缓冲溶液
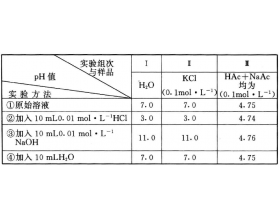
例 :取纯水、KCl溶液、HAc与NaAc的混合液各 90 mL 进行实验,实验做法和结果见下表。 问:(1)从实验结果可得出什么结论? (2) 试解释第I组实验的实验结果? (3) 试推测哪类溶液可具有第I组溶液的性质? [解析](1)实验结果表明,加入少量酸或碱后,纯水和KCl 溶液的pH值发生...
 [探讨与扩展j] 强电解质有无“强”、“弱”之分? 作者:化学自习室 来源:未知 日期:2019-11-11 16:49:07 点击:783 所属专题:弱电解质
[探讨与扩展j] 强电解质有无“强”、“弱”之分? 作者:化学自习室 来源:未知 日期:2019-11-11 16:49:07 点击:783 所属专题:弱电解质
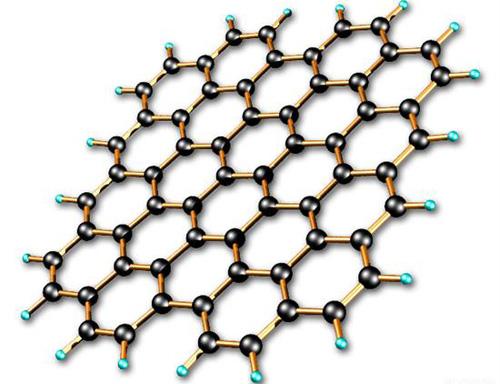
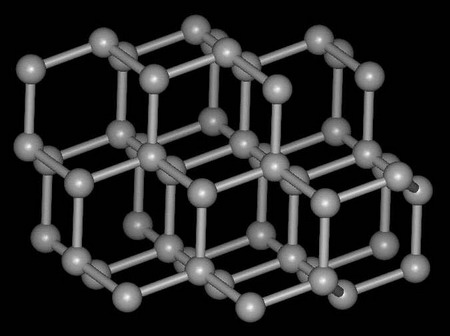
高中化学教材指出“HClO 4 是已知酸中最强的一种酸”,这表 明不同的强电解质仍有强度的差别。从酸分子结构的分析确实可以得出这个结论。 但是为什么这些强酸在水溶液中都几乎完全电 离呢?这是因为按照酸喊的质子理论,和HClO 4 、HNO 3 、HX等 强酸的共轭碱Cl O 4 - 、N...
 [探讨与扩展j] 各个价态的铬的化合物或离子的颜色 作者:化学自习室 来源:未知 日期:2019-09-20 11:18:57 点击:17099 所属专题:重铬酸钾 颜色
[探讨与扩展j] 各个价态的铬的化合物或离子的颜色 作者:化学自习室 来源:未知 日期:2019-09-20 11:18:57 点击:17099 所属专题:重铬酸钾 颜色
Cr[铬]:蓝白色金属 Cr(2+)[二价铬离子]:蓝色离子 Cr(OH) 4 (-)[四氢氧化铬离子]:亮绿色离子 CrO 4 (2-)[铬酸根离子]:橙黄色离子 Cr(3+)[三价铬离子]:紫色离子 CrO 2 (-)[二氧化铬离子]:绿色离子 Cr 2 O 3 [三氧化二铬]:绿色固体 Cr 2 O 7 (2-)[重铬酸根离子...
 [探讨与扩展j] 常见盐溶液中离子浓度的精准算法(定量) 作者:尚凡朋 来源:未知 日期:2019-07-30 10:10:55 点击:1225 所属专题:离子浓度大小比较
[探讨与扩展j] 常见盐溶液中离子浓度的精准算法(定量) 作者:尚凡朋 来源:未知 日期:2019-07-30 10:10:55 点击:1225 所属专题:离子浓度大小比较
...
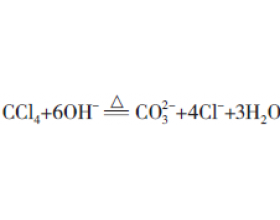 [探讨与扩展j] 为什么SiCl4极易水解,而CCl4却不易水解? 作者:化学自习室 来源:未知 日期:2020-11-17 17:38:11 点击:9315 所属专题:四氯化碳 非盐水解反应
[探讨与扩展j] 为什么SiCl4极易水解,而CCl4却不易水解? 作者:化学自习室 来源:未知 日期:2020-11-17 17:38:11 点击:9315 所属专题:四氯化碳 非盐水解反应
室温下,SiCl 4 遇水会强 烈水解:SiCl 4 +4H 2 O=H 4 SiO 4 +4HCl。而CCl 4 却不容易水解,故实验室可用CCl 4 萃取溴水中的溴单质。为什么? 共价型化合物水解的必要条件是电正性原子要有空轨道。硅原子不仅有可供成键的 3s 和 3p轨道,而且还有空的 3d 轨道。当 SiCl 4...
 [探讨与扩展j] 什么是酸、碱? 作者:吴星 来源:未知 日期:2018-08-02 11:36:39 点击:4807 所属专题:酸碱理论
[探讨与扩展j] 什么是酸、碱? 作者:吴星 来源:未知 日期:2018-08-02 11:36:39 点击:4807 所属专题:酸碱理论
在中学化学教学中,经常听到化学教师这样问学生:什么称酸不是酸?什么叫碱不是碱?教师给出的答案是:石碳酸(苯酚)不是酸,纯碱不是碱。其 实,在中学化学教学中,对酸碱的认识还存在着许多问题。如: 盐酸是不是酸? H 3 BO 3 是不是酸? HClO 4 是不是最强酸? 这类问题...
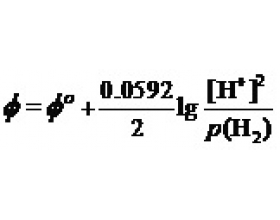 [探讨与扩展j] 用标准电极电势定量计算各种平衡常数 作者:黄瑞 来源:未知 日期:2022-08-25 16:25:25 点击:45472 所属专题:电极电势 水的离子积 电离平衡常数 溶度积
[探讨与扩展j] 用标准电极电势定量计算各种平衡常数 作者:黄瑞 来源:未知 日期:2022-08-25 16:25:25 点击:45472 所属专题:电极电势 水的离子积 电离平衡常数 溶度积
一、水的离子积计算 水的离子积( K w )是一个使用频率较高的化学数据。而一个电极反应只要其中有H + 离子或OH - 离子,在用能斯特方程讨论其酸性介质及碱性介质中的标准电极电势间的关系时,其中就必然会有 K w 项。就都可以用来计算 K w 值。当然,最为简单(涉及的数...
 [探讨与扩展j] 如何定量判断二元弱酸酸式强碱盐(NaHA)溶液的酸碱性? 作者:爱莉 来源:未知 日期:2016-04-22 23:40:43 点击:2753 所属专题:酸碱性
[探讨与扩展j] 如何定量判断二元弱酸酸式强碱盐(NaHA)溶液的酸碱性? 作者:爱莉 来源:未知 日期:2016-04-22 23:40:43 点击:2753 所属专题:酸碱性
怎样判断NaHCO 3 、.NaHSO 3 等弱酸式盐溶液的酸碱性?除了计算这种酸式盐对应的应的酸的二级电离常数和二级水解平衡常数,是否还有其他更简便的方法? 按照酸碱质子理论,酸碱反应中,酸失去质子,碱得到质子,且碱得到质子数 与酸失去的质子子数必定相等。根据溶液中得...
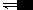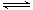 [探讨与扩展j] 如何定量判断盐能否发生彻底水解? 作者:熊振典 来源:未知 日期:2016-04-22 22:57:38 点击:3201 所属专题:双水解反应
[探讨与扩展j] 如何定量判断盐能否发生彻底水解? 作者:熊振典 来源:未知 日期:2016-04-22 22:57:38 点击:3201 所属专题:双水解反应
对于CH 3 COONH 4 、NH 4 F等弱酸弱碱盐,它们的阴、阳离子都会发生水解导致水解相互促进。一般情况下,如CH 3 COONa、NH 4 F的水解程度虽然较大,但其溶液中主要还是以盐的形式存在,水解未进行彻底。 对于Al 2 S 3 、(NH 4 ) 2 S等弱酸弱碱盐,它们的阴、阳离子都会发生水...
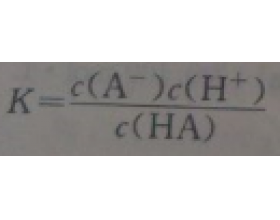 [探讨与扩展j] 如何定量判断弱酸与强碱弱酸盐混合后的酸碱性? 作者:谢文芳 来源:未知 日期:2016-04-22 22:53:58 点击:4914 所属专题:酸碱性
[探讨与扩展j] 如何定量判断弱酸与强碱弱酸盐混合后的酸碱性? 作者:谢文芳 来源:未知 日期:2016-04-22 22:53:58 点击:4914 所属专题:酸碱性
等物质的量的CH 3 COOH与CH 3 COONa的混合溶液呈酸性,等物质的量的 NH 3 H 2 O与NH 4 Cl的混合溶液呈减性,等物质的量的HCN与NaCN的混合溶 液呈碱性。这其中有什么规律?如何判断H a 弱酸和相应的Na a 以等物质的量混 合后溶液酸碱性? 设某弱酸HA的电离常数为K,与等...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
莫尔法和佛尔哈德法是分析化学中沉淀滴定法的两种经典方法,...
...
所谓缓冲溶液,是指能维持溶液的酸度,使溶液的pH不因外加少...
...
什么是PH?PH是拉丁文“Pondushydrogenii”一词的缩写(Pondus=压强、压...
一、水的离子积计算 水的离子积( K w )是一个使用频率较高的化...
多元弱酸在水中是分步电离的,因此,计算时应考虑电离 / 反应...
强酸溶液氢离子浓度: HCl 溶液中,完全电离,因此 [H + ]=[ Cl ...