
|
学习小专题 |

|
学习小专题 |
 [探讨与扩展j] 电解质相对强弱的定量判断 作者:许雁祥 来源:未知 日期:2016-04-22 22:30:29 点击:1214 所属专题:弱电解质判断
[探讨与扩展j] 电解质相对强弱的定量判断 作者:许雁祥 来源:未知 日期:2016-04-22 22:30:29 点击:1214 所属专题:弱电解质判断
通常情况下,强电解质是指电离度在30%以上的电解质,如强酸、强碱和大部分 盐。弱电解质是指电离度在30%以下的电解质,如弱酸和弱碱。 通常认为某酸或碱的电离常数K(25 °C) >1则为强酸或强碱,即强电解质;电 离常数K=10 -4 <K<1为中强电解质;电离常数K<10 -4 为弱...
 [探讨与扩展j] 浅析非水溶剂中的自耦电离及相关命题 作者:林夕 来源:未知 日期:2021-11-29 19:35:38 点击:7450 所属专题:自耦电离
[探讨与扩展j] 浅析非水溶剂中的自耦电离及相关命题 作者:林夕 来源:未知 日期:2021-11-29 19:35:38 点击:7450 所属专题:自耦电离
有关自偶电离特别是非水溶剂中自偶电离的试题不断涌现,逐渐成为了各类考试特别是高中化学竞赛的命题热点。 1、自偶电离的概念 自偶电离是指液态极性共价分子化合物(不一 定是水)电负性强的部分与电负性弱的部分相互作 用,自发电离产生液态极性共价分子合一组分的阴离...
 [探讨与扩展j] Kw为什么只适合稀溶液? 作者:王欣华 来源:未知 日期:2018-07-19 17:04:34 点击:3778 所属专题:水的离子积常数
[探讨与扩展j] Kw为什么只适合稀溶液? 作者:王欣华 来源:未知 日期:2018-07-19 17:04:34 点击:3778 所属专题:水的离子积常数
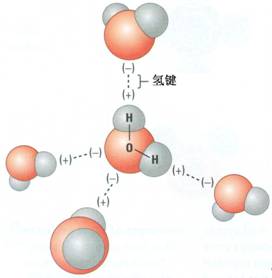
【一般情况】 水是一种极弱的电解质,可以发生微弱的电离,其电离方程式为:H 2 O+H 2 O≒H 3 O + + OH - ,简写为H 2 O≒H + + OH - ,是一个吸热过程.水的电离是水分子与水分子之间的相互作用而引起的,因此极难发生,大约55.5×10 8 个水分子中只有1个水分子...
 [探讨与扩展j] 自耦电离:碳酸氢钠能和氯化钙反应分析 作者:康建峰 来源:未知 日期:2021-11-29 19:38:32 点击:6572 所属专题:自偶电离 碳酸氢钠01
[探讨与扩展j] 自耦电离:碳酸氢钠能和氯化钙反应分析 作者:康建峰 来源:未知 日期:2021-11-29 19:38:32 点击:6572 所属专题:自偶电离 碳酸氢钠01
碳酸氢钠能和氯化钙反应的道理可以用碳酸氢根离子的“自偶”电离来解释以上现象;碳酸氢根离子的“自偶”电离解释,很好理解。是的,对学生来说,很难,没有足够的信息,难以书写有关化学用语。...
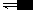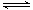 [探讨与扩展j] 某些水解为什么能“进行到底” 作者:袁建标 来源: 日期:2015-06-09 22:43:30 点击:3219 所属专题:双水解反应
[探讨与扩展j] 某些水解为什么能“进行到底” 作者:袁建标 来源: 日期:2015-06-09 22:43:30 点击:3219 所属专题:双水解反应
一.水解平衡常数小,无法进行到底 例1.关于醋酸铵溶液——不能进行到底 Ac - + H 2 O = HAc + OH - NH 4 + + H 2 O = NH 3 ·H 2 O + H + 由于生成的H + 和OH - 会结合生成水,所以促进醋酸铵的水解,两式相加得醋酸铵总的水解方程: Ac - + NH 4 + + H...
 [探讨与扩展j] 等浓度、等体积的HA与NaA混合,溶液一定显酸性吗? 作者:陈爱玉 来源: 日期:2015-05-26 19:12:17 点击:1693 所属专题:酸碱性
[探讨与扩展j] 等浓度、等体积的HA与NaA混合,溶液一定显酸性吗? 作者:陈爱玉 来源: 日期:2015-05-26 19:12:17 点击:1693 所属专题:酸碱性
1.若HA为强酸,则等浓度、等体积的HA与NaA混合当然为酸性。 2.若HA为弱酸酸,则等浓度、等体积的HA与NaA混合可能为酸性,可能为碱性,理论上说,也可以为中性。 假设浓度为c mol/L的HA和NaA等体积混合,其中HA的电离常数为K,若混合后溶液为酸性,则必须满足以下关系: c...
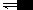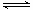 [探讨与扩展j] 同离子效应和盐效应 作者:秦文鑫 来源:未知 日期:2015-02-02 22:48:34 点击:11784 所属专题:同离子效应 盐效应
[探讨与扩展j] 同离子效应和盐效应 作者:秦文鑫 来源:未知 日期:2015-02-02 22:48:34 点击:11784 所属专题:同离子效应 盐效应
一.同离子效应 离子浓度的改变,对弱酸、弱碱电离程度的影响极为显著。 例如在氨水中,加入一些NH 4 Ac时,由于NH 4 Ac是强电解质,它们在溶液中完全电离,这样,溶液中 NH 4 + 离子浓度就会大大增加。使NH 3 +H 2 O NH 4 + + OH - 电离平衡向左移动,从而降低了氨水的...
 [探讨与扩展j] 酸性及碱性的缓冲溶液的PH计算 作者:朱照鹰 来源:未知 日期:2015-01-28 21:04:23 点击:7496 所属专题:缓冲溶液 ph计算
[探讨与扩展j] 酸性及碱性的缓冲溶液的PH计算 作者:朱照鹰 来源:未知 日期:2015-01-28 21:04:23 点击:7496 所属专题:缓冲溶液 ph计算
1.已知25℃时,CH 3 COOH的电离常数为1.8×10 -5 。 则25℃时,0.1mol/L 的CH 3 COOH和0.1mol/L 的CH 3 COONa按体积比1:1混合后,所得混合液的pH是多少?请计算说明。 2.已知25℃时,NH 3 ·H 2 O的电离常数为1.8×10 -5 。 则25℃时,0.1mol/L 的氨水和0.1mol/L 的NH 4 C...
 [探讨与扩展j] 常用的酸碱理论 作者:樊会武 来源:未知 日期:2014-10-15 17:09:39 点击:6662 所属专题:酸碱理论
[探讨与扩展j] 常用的酸碱理论 作者:樊会武 来源:未知 日期:2014-10-15 17:09:39 点击:6662 所属专题:酸碱理论
1.Arrhenius理论,----------“酸碱电离理论” 定义:凡是水溶液中产生H + 离子的物质就叫酸,产生OH - 离子的就叫碱。 重要性及优点:是建立在电离理论之上,大众最熟知的经典酸碱理论。建立了对酸碱强度的定量描述;适用于pH计算、电离度计算、缓冲溶液计算、溶解度计算...
 [探讨与扩展j] 为什么有的弱电解质电离时是放热的? 作者:陈女婷 来源:未知 日期:2018-07-19 16:36:22 点击:4953 所属专题:弱电解质 电解质电离
[探讨与扩展j] 为什么有的弱电解质电离时是放热的? 作者:陈女婷 来源:未知 日期:2018-07-19 16:36:22 点击:4953 所属专题:弱电解质 电解质电离
为什么有的弱电解质电离时是放热的。例如,1 mol氢氟酸电离时放出10.4 kJ/mol热量。当它跟1 mol NaOH溶液反应时,中和热是67.7 kJ/mol。 离子水合时,由于离子与水分子的电子层有斥力,所以放出能量就能减少斥力,从而使水合离子趋于稳定,HF在水中的电离比一般弱电解质...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
莫尔法和佛尔哈德法是分析化学中沉淀滴定法的两种经典方法,...
...
所谓缓冲溶液,是指能维持溶液的酸度,使溶液的pH不因外加少...
...
什么是PH?PH是拉丁文“Pondushydrogenii”一词的缩写(Pondus=压强、压...
一、水的离子积计算 水的离子积( K w )是一个使用频率较高的化...
多元弱酸在水中是分步电离的,因此,计算时应考虑电离 / 反应...
强酸溶液氢离子浓度: HCl 溶液中,完全电离,因此 [H + ]=[ Cl ...