
|
ѧϰСר�� |

|
ѧϰСר�� |
 [���������e] ���ӵĿռ乹�͵�ȷ������ͼ ����:֣��ǿ ��Դ:δ֪ ���ڣ�2016-01-30 12:30:26 �����1269 ����ר�⣺�ռ�ṹ
[���������e] ���ӵĿռ乹�͵�ȷ������ͼ ����:֣��ǿ ��Դ:δ֪ ���ڣ�2016-01-30 12:30:26 �����1269 ����ר�⣺�ռ�ṹ
...
 [���������e] ����ԭ���ӻ����͵��ж� ����:�ַ� ��Դ:δ֪ ���ڣ�2014-10-15 16:20:20 �����11195 ����ר�⣺�ӻ������ж�
[���������e] ����ԭ���ӻ����͵��ж� ����:�ַ� ��Դ:δ֪ ���ڣ�2014-10-15 16:20:20 �����11195 ����ר�⣺�ӻ������ж�
�ӿ���˵���в��ѿ���������Ҫ���Ǽ��ӻ������жϣ���d��������ӻ��IJ���Ҫ��������sp��sp 2 ��sp 3 �������͵��жϣ��ʹ������ӻ����͵��жϷ��������¹��ɡ� 1��ȡ���� ����ѧ�����ġ���Ϥ�Ļ������ʷ���Ϊԭ�ͣ�������ԭ�ӻ�ԭ����ȡ��ԭ�ͷ����еIJ���ԭ��...
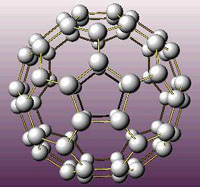 [���������e] �۲���ӶԻ�������Ԥ��ķ��ӿռ�ṹ�� ����:���� ��Դ:δ֪ ���ڣ�2020-01-02 09:01:08 �����9251 ����ר�⣺�۲���ӶԻ�������
[���������e] �۲���ӶԻ�������Ԥ��ķ��ӿռ�ṹ�� ����:���� ��Դ:δ֪ ���ڣ�2020-01-02 09:01:08 �����9251 ����ר�⣺�۲���ӶԻ�������
�۲���ӶԻ�������Ԥ��ķ�����״�� ���Ӷ��� �ӻ����ͣ�������ͣ� �����״ �����Ӷ������µ��Ӷԣ� ������״ �� 2 sp ֱ���� 0 ֱ���� BeCl 2 ��CO 2 1 sp 2 ƽ���������� 0 ƽ���������� BCl 3 1 sp 2 V���Σ����Ρ������Σ� SO 2 4 sp 3 �������� 0 �������� CH 4...
 [���������e] ���ӣ����ӣ��ļ��ι��͵��жϷ��� ����:���� ��Դ:δ֪ ���ڣ�2022-07-29 10:22:15 �����40000 ����ר�⣺���ӿռ�ṹ�ж�
[���������e] ���ӣ����ӣ��ļ��ι��͵��жϷ��� ����:���� ��Դ:δ֪ ���ڣ�2022-07-29 10:22:15 �����40000 ����ר�⣺���ӿռ�ṹ�ж�
1��ȷ������ԭ�Ӽ۲����������������ʽ����õ��� �۲���Ӷ�����������ԭ�Ӽ۵�����+ ��λԭ���ṩ������-���������������/2 ��ʽ����λԭ���ṩ�������ļ��㷽���ǣ����±��ԭ�Ӿ��ṩ1���۵��ӣ�������ԭ���ṩ����Ϊ�㡣��Ϊ������۵�����Ϊ6����������ԭ�ӳɼ�...
 [���������e] ��������ṹ���жϷ������ ����:���� ��Դ:δ֪ ���ڣ�2022-07-29 10:20:04 �����21589 ����ר�⣺���ӿռ�ṹ�ж�
[���������e] ��������ṹ���жϷ������ ����:���� ��Դ:δ֪ ���ڣ�2022-07-29 10:20:04 �����21589 ����ר�⣺���ӿռ�ṹ�ж�
һ���۲���ӶԻ���ģ�ͣ� VSEPRmodels �� �ѷ��ӷֳ������ࣺһ��������ԭ���ϵļ۵��Ӷ������γɹ��ۼ����� CO 2 �� CH 2 O �� CH 4 �ȷ����е� C ԭ�ӡ����ǵ�����ṹ��������ԭ����Χ��ԭ������Ԥ�⣬�������£� ��һ��������ԭ�����й¶Ե��ӣ�δ�����γɹ��ۼ���...
 [���������e] ����Ʋ���ӵĿռ乹�ͣ� ����:ʯ�� ��Դ:δ֪ ���ڣ�2013-04-03 09:33:04 �����10785 ����ר�⣺�ռ�ṹ
[���������e] ����Ʋ���ӵĿռ乹�ͣ� ����:ʯ�� ��Դ:δ֪ ���ڣ�2013-04-03 09:33:04 �����10785 ����ר�⣺�ռ�ṹ
��������ԭ�ӹµ��Ӷ�����m �� ���þ�����ɣ� ���� AX n a�� ����ʾֻ��һ������ԭ�ӵķ��ӻ����ӵ���ɡ� �����ź��壺 A���� ����ԭ�� X���� ����ԭ�ӽ�ϵ�ԭ�ӣ�������һ�֣�Ҳ�����Ƕ��֣� n���� ����ԭ�ӽ�ϵ�ԭ�ӵ����� ��ʽ�� m �� A �ļ۵��������� X �Ļ���...
 [���������e] ����ԭ���ӻ�������͵��жϷ��� ����:���� ��Դ:δ֪ ���ڣ�2014-06-13 11:31:06 �����21368 ����ר�⣺�ӻ������ж�
[���������e] ����ԭ���ӻ�������͵��жϷ��� ����:���� ��Դ:δ֪ ���ڣ�2014-06-13 11:31:06 �����21368 ����ר�⣺�ӻ������ж�
һ�����ݷ��ӵĿռ乹���ж� �����ӻ�������ۣ�����ԭ�ӹ����ȡһ�����ӻ���ʽ����ռ乹�ͺͼ������£� �ӻ�������� �ӻ�����ռ乹�� ���� sp ֱ���� 180�� sp2 ƽ�������� 120�� sp3 �������� 109.5�� �ɴˣ����Ը��ݷ��ӵĿռ乹�ͻ�������ж����� ԭ�ӹ����...
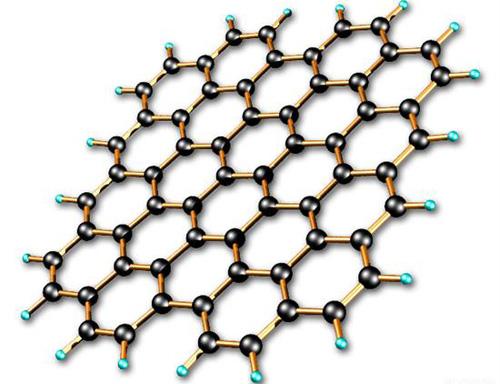 [���������e] ����ԭ���ӻ���������㷽�� ����:���� ��Դ:δ֪ ���ڣ�2014-06-13 11:33:18 �����47658 ����ר�⣺�ӻ������ж�
[���������e] ����ԭ���ӻ���������㷽�� ����:���� ��Դ:δ֪ ���ڣ�2014-06-13 11:33:18 �����47658 ����ר�⣺�ӻ������ж�
������̣� 1�������۷���(������)��ʾΪHmABn������H��ʾ��ԭ�ӣ�AΪ����ԭ�ӣ�BΪ���塣 2���ӻ���������㹫ʽ��G��V/2��3n ������G��ʾ����ԭ��A���ӻ��������V���ӻ����ӵ��ܼ۵�����������۵�������Ϊ�������٣�1����n��ʾ������ 3��G��2��SP�ӻ���ֱ���ͣ�G��3...
 [���������e] ��������ǿ���Ƚ� ����:��˫�� ��Դ:δ֪ ���ڣ�2019-11-13 15:00:32 �����25853 ����ר�⣺������ ������ ����
[���������e] ��������ǿ���Ƚ� ����:��˫�� ��Դ:δ֪ ���ڣ�2019-11-13 15:00:32 �����25853 ����ר�⣺������ ������ ����
һ������������ǿ���仯���� ����ͨʽHxROy��ʾ�����ᣬ��������ǿ����RԪ�صķǽ����Լ���ԭ�ӵİ뾶�йء�RԪ�صķǽ�����Խǿ������ԭ�Ӻ˶Ժ���õ��ӶԵ�������Խǿ��R-O ��Ĺ��õ��Ӷ�Խƫ��Rԭ�ӵ�һ����RԪ��ԭ�ӵİ뾶ԽС����R-O��Ĺ��õ��Ӷ�ҲԽƫ��Rԭ...
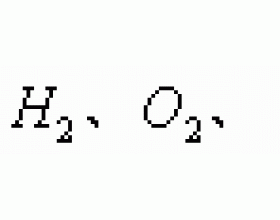 [���������e] ���Ӽ��Լ����жϹ��� ����:���� ��Դ:δ֪ ���ڣ�2013-03-27 16:58:15 �����13066 ����ר�⣺���Ӽ���
[���������e] ���Ӽ��Լ����жϹ��� ����:���� ��Դ:δ֪ ���ڣ�2013-03-27 16:58:15 �����13066 ����ר�⣺���Ӽ���
һ�����ࣺ���շ��ӵļ��ԣ��ɰѷ��ӷ�Ϊ���ࡣ 1. �Ǽ��Է��ӣ�������������غϣ����Ӷ��ⲻ��ʾ�縺�Եķ��ӡ����磺 �ȡ� 2. ���Է��ӣ�����������IJ��غϣ����Ӷ�����ʾ�縺�Եķ��ӡ����� HCl��H 2 O 2 �ȡ� �������ճ������Ӽ��Լ���ռ乹�ͣ��������Ӽ��Լ���...
 ��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ�
��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ� ��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�
��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�˳���칹�У����ӵĶԳ��ԡ������Լ��۵�ͷе�������²��죺 1.�Գ��ԱȽ� ��ʽ�칹...
01 �� ���� �ڶ�ԭ�ӷ��ӣ������������������ϵ�ԭ�ӹ��ɵķ��ӣ��У������ƽ�е�p...
���й��ۼ�����������������֮��ļнdz�Ϊ���ǡ������Ǿ������ʷ��ӿռ乹�͵���Ҫ��...
1.�ǻ�״С���Ӻ������еĴ�м������������AB n �ͣ����Լ����ӻ����͡� ���ȣ�����...
1.�Ҽ���м� �Ҽ���ԭ�ӹ�����Ź���Գ���ķ���ͷ��ͷ���ص��γɵĹ��ۼ��� �м�...
��λ������Ŀռ乹�ͣ� ����λ��ֱ���ͣ�����λ�����������ͻ�ƽ�������Σ�����λ(��...
1������������(��ԭ��)�����������ʱ����λ�����Ե�ͬ����λԭ�ӵ���Ŀ����������...
һ�� ֪ʶ���� 1�� ���� ���� �� chirality �� һ��ָһ�����岻�����侵�����غ� �� ...